Инсулиннезависимый сахарный диабет основы патогенеза и терапии
Инсулиннезависимый сахарный диабет (СД 2 типа): причины, диагностика, лечениеЭтиология и встречаемость инсулиннезависимого сахарного диабета (ИНСД). Сахарный диабет — разнородная болезнь, подразделяемая на диабет I типа (ИЗСД) и II типа (ИНСД) (см. табл. С-30). ИНСД (MIM № 125853) составляет от 80 до 90% всех случаев сахарного диабета и встречается в США у 6-7% взрослых. По неизвестным пока причинам существует поразительно высокая встречаемость болезни среди американских индейцев из племени пима в Аризоне, составляющая почти 50% к возрасту 35-40 лет. Приблизительно 5-10% пациентов с инсулиннезависимым сахарным диабетом имеют сахарный диабет взрослого типа в молодости (MODY, MIM №606391); 5-10% — редкие генетические заболевания; остальные 70-85% — «типичную форму» инсулиннезависимого сахарного диабета II типа, характеризующуюся относительным недостатком инсулина и повышенной резистентностью к нему. Молекулярная и генетическая основы типичного инсулиннезависимого сахарного диабета остаются недостаточно выясненными. Патогенез инсулиннезависимого сахарного диабета (ИНСД)Инсулиннезависимый сахарный диабет (ИНСД) вызван нарушением секреции инсулина и резистентностью к его действию. В норме основная секреция инсулина происходит ритмично, в ответ на нагрузку глюкозой. У больных инсулиннезависимым сахарным диабетом (ИНСД) нарушено базальное ритмическое выделение инсулина, ответ на нагрузку глюкозой неадекватный, а базальный уровень инсулина повышен, хотя относительно ниже гипергликемии. Сначала появляется устойчивая гипергликемия и гиперинсулинемия, инициирующая развитие инсулиннезависимого сахарного диабета (ИНСД). Устойчивая гипергликемия снижает чувствительность b-клеток островков, приводя к уменьшению выброса инсулина для данного уровня глюкозы крови. Аналогично хронически повышенный базальный уровень инсулина подавляет инсулиновые рецепторы, увеличивая их резистентность к инсулину. Кроме того, так как чувствительность к инсулину снижена, увеличивается секреция глюкагона; в результате избытка глюкагона возрастает выброс глюкозы из печени, что усиливает гипергликемию. В конце концов, этот порочный круг и приводит к инсулиннезависимому сахарному диабету. Типичный инсулиннезависимый сахарный диабет возникает вследствие комбинации генетической предрасположенности и факторов влияния окружающей среды. Наблюдения, поддерживающие генетическую предрасположенность, включают различия в конкордантности между монозиготными и дизиготными близнецами, семейное накопление и различия в распространенности в разных популяциях.
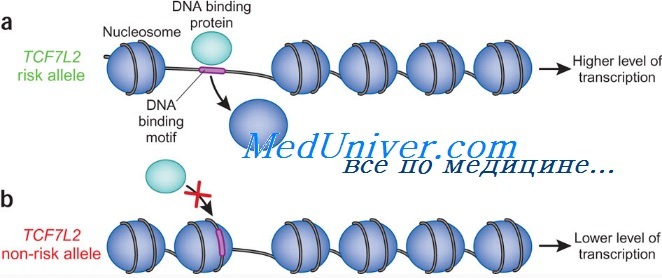
Хотя тип наследования расценивают как многофакторный, идентификация главных генов, затрудненная влиянием возраста, пола, этнической принадлежности, физического состояния, рациона питания, курения, ожирения и распределения жира, достигла некоторых успехов. Полногеномный скрининг показал, что в исландской популяции с инсулиннезависимым сахарным диабетом тесно сцеплены полиморфные аллели коротких тандемных повторов в интроне фактора транскрипции TCF7L2. Гетерозиготы (38% популяции) и гомозиготы (7% популяции) имеют повышенный относительно неносителей риск по ИНСД приблизительно в 1,5 и 2,5 раза соответственно. Повышенный риск у носителей варианта TCF7L2 также обнаружен в датской и американской когортах больных. Риск ИНСД, соотнесенный с этим аллелем, составляет 21%. TCF7L2 кодирует фактор транскрипции, участвующий в экспрессии гормона глюкагона, повышающего концентрацию глюкозы крови, действуя противоположно действию инсулина, снижающего уровень глюкозы крови. Скринирование финских и мексиканских групп выявило другой вариант предрасположенности, мутацию Рго12А1а в гене PPARG, очевидно, специфическую для этих популяций и обеспечивающую вплоть до 25% попу-ляционного риска ИНСД. Более частый аллель пролина встречается с частотой 85% и вызывает незначительное увеличение риска (в 1,25 раза) сахарного диабета. Ген PPARG — член семейства ядерных рецепторов гормонов и важен для регуляции функции и дифференцировки жировых клеток. Подтверждение роли факторов окружающей среды включает конкордантность менее 100% у монозиготных близнецов, различия в распространении в генетически сходных популяциях и ассоциации с образом жизни, питанием, ожирением, беременностью и стрессом. Экспериментально подтверждено, что хотя предварительным условием для развития инсулиннезависимого сахарного диабета является генетическая предрасположенность, клиническая экспрессия инсулиннезависимого сахарного диабета (ИНСД) сильно зависит от влияния факторов окружающей среды. Фенотип и развитие инсулиннезависимого сахарного диабета (ИНСД)Обычно инсулиннезависимый сахарный диабет (ИНСД) встречается у полных людей в среднем возрасте или старше, хотя число больных детей и молодых лиц становится все большим в связи с увеличением числа полных и недостаточной подвижностью среди молодежи. Сахарный диабет 2 типа имеет постепенное начало и обычно диагностируется по повышенному уровню глюкозы при стандартном обследовании. В отличие от больных с сахарным диабетом 1 типа, у пациентов с инсулиннезависимым сахарным диабетлм (ИНСД) обычно кетоацидоз не развивается. В основном развитие инсулиннезависимого сахарного диабета (ИНСД) подразделяется на три клинических фазы. Сначала концентрация глюкозы крови остается нормальной, несмотря на повышенный уровень инсулина, указывая, что ткани-мишени инсулина остаются сравнительно устойчивыми к влиянию гормона. Затем, несмотря на повышенную концентрацию инсулина, развивается гипергликемия после нагрузки. Наконец, ухудшение секреции инсулина вызывает голодную гипергликемию и клиническую картину сахарного диабета. Кроме гипергликемии, метаболические расстройства, вызванные дисфункцией b-клеток островков и резистентностью к инсулину, вызывают атеросклероз, периферическую нейропатию, почечную патологию, катаракты и ретинопатию. У одного из шести пациентов с инсулиннезависимым сахарным диабетом (ИНСД) разивается почечная недостаточность или тяжелая сосудистая патология, требующая ампутации нижних конечностей; один из пяти слепнет вследствие развития ретинопатии. Развитие этих осложнений обусловливается генетическим фоном и качеством метаболического контроля. Хроническую гипергликемию можно выявлять определением уровня гликозилированного гемоглобина (НbА1c). Строгое, как можно более близкое к норме, поддержание концентрации глюкозы (не более 7%), с определением уровня HbA1c, уменьшает риск осложнений на 35-75% и может продлить средний ожидаемый срок жизни, составляющий в настоящее время в среднем 17 лет после установления диагноза, на несколько лет. Особенности фенотипических проявлений инсулиннезависимого сахарного диабета: Лечение инсулиннезависимого сахарного диабета (ИНСД)Снижение массы тела, повышение физической активности и изменения диеты помогают большинству больных инсулиннезависимым сахарным диабетом (ИНСД) заметно улучшить чувствительность к инсулину. К сожалению, множество пациентов не в состоянии или не склонны радикально изменить свой образ жизни, чтобы добиться улучшения, и требуют лечения с перо-ральными гипогликемическими препаратами, например сульфонилуреатами и бигуанидами. Третий класс препаратов — тиазолидиндионы — уменьшают резистентность к инсулину, связываясь с PPARG. Можно также использовать четвертую категорию лекарственных средств — ингибиторы а-глюкозидазы, действующие путем замедления внутрикишечного всасывания глюкозы. Каждый из этих классов лекарств одобрен как монотерапия для инсулиннезависимого сахарного диабета (ИНСД). Если один из них не останавливает развитие болезни, может быть добавлен препарат из другого класса. Пероральные гипогликемические препараты не так эффективны в достижении контроля уровня глюкозы, как снижение массы тела, повышение физической активности и изменения диеты. Чтобы добиться контроля уровня глюкозы и уменьшить риск осложнений, некоторым больным требуется инсулинотерапия; тем не менее она усиливает резистентность к инсулину, увеличивая гиперинсулинемию и ожирение. Риски наследования инсулиннезависимого сахарного диабета (ИНСД)Популяционный риск инсулиннезависимого сахарного диабета (ИНСД) очень зависит от изучаемой популяции; в большинстве популяций этот риск составляет от 1 до 5%, хотя в США он равен 6-7%. Если пациент имеет больного сибса, риск возрастает до 10%; наличие больного сибса и другого родственника первой степени родства повышает риск до 20%; если болен монозиготный близнец, риск поднимается до 50-100%. Кроме того, поскольку некоторые формы инсулиннезависимого сахарного диабета (ИНСД) пересекаются с сахарным диабетом 1 типа, дети родителей с инсулиннезависимым сахарным диабетом (ИНСД) имеют эмпирический риск 1 к 10 по развитию сахарного диабета 1 типа. Пример инсулиннезависимого сахарного диабета. М.П., здоровый мужчина 38 лет, американский индеец племени пима, консультируется в связи с риском развития инсулиннезависимого сахарного диабета (ИНСД). Оба его родителя страдали инсулиннезависимым сахарным диабетом; отец умер в 60 лет от инфаркта миокарда, мать — в 55 лет от почечной недостаточности. Дед по отцу и одна из старших сестер также болели инсулиннезависимым сахарным диабетом, но он и его четыре младших сибса здоровы. Данные медицинского осмотра оказались нормальными, за исключением незначительного ожирения; уровень глюкозы крови натощак в норме, однако обнаружено повышение уровня инсулина и глюкозы в крови после пероральной нагрузки глюкозой. Эти результаты соответствуют ранним проявлениям метаболического состояния, вероятно, ведущего к инсулиннезависимому сахарному диабету. Его врач посоветовал пациенту изменить образ жизни, похудеть и увеличить физическую активность. Пациент резко уменьшил употребление жира, начал ездить на работу на велосипеде и бегать три раза в неделю; его масса тела уменьшилась на 10 кг, а толерантность к глюкозе и уровень инсулина в крови пришли в норму. – Также рекомендуем “Недостаточность орнитинтранскарбамилазы (ОТК): причины, диагностика, лечение” Оглавление темы “Наследственные болезни”:
|
Источник
Сахарный диабет 2-го типа, он же инсулиннезависимый, — эндокринное заболевание, гораздо более распространенное, чем диабет 1-го типа. Если раньше его диагностировали в основном у пожилых людей, то сейчас в группе риска люди от 40 лет, а так же дети, подростки и молодежь.
Главные факторы риска этого нарушения обмена веществ — неправильное питание и избыточная масса тела.
Что такое сахарный диабет 2-го типа?
С инсулинозависимым диабетом все более-менее понятно: поджелудочная железа не продуцирует инсулин, и человеку приходится получать его извне — при помощи уколов. Без него нельзя, потому что именно он способствует расщеплению сахаров до такого состояния, чтобы они могли беспрепятственно проникнуть в клетки. Кроме того, инсулин размягчает клеточные мембраны, что улучшает их пропускную способность.
С сахарным диабетом 2-го типа все немного сложнее. Инсулин вырабатывается, но не хватает либо его количества, либо активности, поэтому сахара медленнее и хуже расщепляются, а клеточные мембраны остаются плотными и не пропускают их внутрь.
В этом и есть их основное отличие.
Первые признаки диабета 2-го типа
Поскольку инсулиннезависимый диабет стремительно молодеет, очень важно знать, какие для него присущи признаки, чтобы можно было их своевременно распознать и обратиться к специалисту.
Сильная жажда и сухость во рту
Человек с начальной стадией сахарного диабета 2-го типа обычно обращает внимание именно на этот признак. Жажда и сухость во рту объясняются повышенной нагрузкой на почки, которым нужно избавляться от излишков сахара. Для этого почкам нужна вода, которую им приходится “забирать” из клеток.
По этой же причине могут возникать ложные позывы к мочеиспусканию, а также человек часто хочет в туалет.
Усталость, раздражение, головокружение
Глюкоза — основной источник энергии, и когда ее не хватает тканям, человек это явно ощущает. Страдает, в первую очередь, головной мозг, поэтому симптомы будут связаны с деятельностью ЦНС, откуда и появляется повышенная утомляемость, частые перепады настроения, головокружения и головные боли.
Снижение остроты зрения
Практически всех людей с диабетом поджидает диабетическая ретинопатия — заболевание, связанное с нарушением кровоснабжения глаз. Сосуды глазных яблок начинают работать хуже, и следовательно — хуже питать глаза.
Результатом недостатка питательных веществ становится ухудшение зрения и появление оптических явлений: “мушек”, “тумана” и различных пятен перед глазами.
Постоянное чувство голода
В организме человека есть гормон лептин. Он синтезируется жировой тканью и отвечает за чувство насыщения, но, что самое важное, напрямую связан с инсулином. Инсулин увеличивает производство лептина, а поскольку при диабете его мало, то и лептина не хватает: организм практически всегда “голодный”.
Этот признак чаще беспокоит людей с лишним весом.
Снижение мышечной массы тела
Поскольку организму не хватает энергии, он черпает ее из других источников. Наилучшим вариантом для него становится мышечная ткань, именно поэтому ее объем постепенно будет уменьшаться.
Кожный зуд и высыпания
На ранних стадиях сахарного диабета зачастую появляются различные высыпания, которые нередко зудят. Это объясняется несколькими причинами:
- капилляры не поставляют к клеткам кожи нужное количество энергии, поэтому ухудшается состояние кожи и ослабевают ее защитные функции;
- сыпь провоцируется активностью молекул глюкозы;
- на фоне общего снижения иммунитета кожа становится более уязвимой, поэтому чаще в ее клетки проникают различные инфекции.
У больных часто появляется грибок ногтей, который тоже является одним из первых признаков сахарного диабета.
Профилактика
Чтобы сахарный диабет не дал о себе знать, нужно соблюдать меры профилактики.
- Следить за весом и не допускать его чрезмерного набора.
- Правильно питаться, избегая большого количества быстрых углеводов.
- Регулярно сдавать кровь для проверки уровня глюкозы в ней.
- Обеспечить нормальную двигательную активность.
- Больше дышать свежим воздухом и меньше подвергать себя стрессам.
Особенно внимательно следует относиться к своему здоровью тем людям, у кого в семье были зафиксированы случаи сахарного диабета (у бабушек, дедушек, мамы, папы, братьев, сестер, дяди и тети).
И не забудьте обращаться к врачу при первых же тревожных признаках и ни в коем случае занимайтесь самолечением.
Источник
Т.Ю. Демидова, А.С. Аметов — кафедра эндокринологии и диабетологии Российской медицинской академии последипломного образования, Москва.
I.Yu. Demidova, A.S. Ametov — Department of Endocrinology and Diabetology, Russian Medical Academy of Postgraduate Training, Moscow
Инсулиннезависимый сахарный диабет – проявление гетерогенных нарушений углеводного обмена. Патогенез заболевания все еще остается предметом исследований. В статье рассмотрены вопросы одного из самых противоречивых разделов патогенеза диабета II типа – секреция инсулина b-клетками.
Non-insulin-dependent diabetes mellitus is a manifestation of heterogeneous disorders of carbohydrate metabolism. The pathogenesis of the disease is still the subject of studies. The paper considers B-cell secretion of insulin, one of the most contradictory aspects of the pathogenesis of type 2 diabetes mellitus.
Инсулиннезависимый сахарный диабет (ИНСД) или сахарный диабет II типа представляет собой группу гетерогенных нарушений углеводного обмена. И это объясняет, в первую очередь, отсутствие единой общепринятой теории патогенеза данного заболевания, хотя достижения современной мировой науки во многом прояснили патофизиологию этого распространенного заболевания.
В настоящее время патогенез ИНСД все еще остается предметом интенсивных исследований. Тот факт, что в развитии этой патологии задействованы три основных механизма (изменение функции b-клеток, нарушение инсулинопосредованного захвата глюкозы тканями-мишенями и продукции глюкозы печенью) уже не вызывает сомнений. Однако вопрос о том, какое звено играет главенствующую роль, а какие являются лишь следствием, хотя и очень важным, и сейчас остается дискуссионным.
Одним из самых противоречивых разделов патогенеза ИНСД остается вопрос о секреции инсулина b-клетками. С одной стороны, многочисленные публикации свидетельствуют о наличии у больных ИНСД, особенно с избыточной массой тела, гиперинсулинемии, которая может рассматриваться как предвестник и/или фактор риска развития ИНСД в различных популяциях. Результаты недавно проведенных исследований подтвердили, что способность b-клеток продуцировать инсулин может повышаться задолго до нарушений гомеостаза глюкозы. Было установлено, что стимулирующим влиянием на островковые клетки обладает не только глюкоза, а также и целый ряд нейротрансмиттеров – ацетилхолина (АХ), нейрогуморального агониста холецистокинина (НАХ) и других гормонов желудочно-кишечного тракта, таких как глюкагоно-подобный пептид-1 (ГПП), ингибитор желудочного полипептида (ИЖП) при различных состояниях (например, при вагусной стимуляции). Эти нейрогуморальные стимуляторы способны значительно увеличивать инсулинсекреторную способность островков даже при нормальном уровне глюкозы в крови и чувствительности к инсулину. Более того, так как b-клетка имеет целый комплекс сигнальных систем, необходимый для быстрого и адекватного снабжения инсулином периферических тканей, то при повышении уровня глюкозы в крови, даже в физиологических пределах (от 6 до 8 ммоль/л) их действие может еще больше увеличиваться. Такой синергизм эффектов с течением времени приводит к хронической гиперинсулинемии, ответственной за специфические изменения в тканях-мишенях, снижающие их чувствительность к инсулину и развитие инсулинорезистентности.
С другой стороны, существует немало работ, показавших снижение секреторной активности b-клеток еще до развития явного сахарного диабета. Например, оценка инсулинового ответа b-клеток у нормогликемических лиц с НТГ, в популяции “худых” с неизмененной толерантностью к глюкозе и чувствительностью к инсулину, а также у детей без отягощенной наследственности выявило его достоверное снижение, особенно первой фазы. Данные о снижении секреторной функции у преддиабетиков и больных ИНСД подтвердили работы Hales и Cerasy. Снижение инсулинпродуцирующей функции островковых клеток не может быть объяснено феноменом “глюкозотоксичности”, развивающейся на фоне инсулинорезистентности. Результаты исследования природы ИРИ плазмы у больных ИНСД показали значительный процент проинсулиноподобных компонентов, что также ставит под сомнение наличие истинной гиперинсулинемии у таких больных.
В то же время нельзя не отметить генетические аспекты в развитии ИНСД, не вызывающие сегодня сомнений. Установлено, что и инсулинсекреторный ответ поджелудочной железы и чувствительность тканей к инсулину контролируются генетически и/или подвержены воздействию внутриутробных и неонатальных факторов. Уже известно не менее двух генетических дефектов, способствующих снижению инсулинового ответа. С одной стороны, возможная мутация инсулинового гена приводит к синтезу молекулы инсулина со сниженной биологической активностью. С другой стороны, мутация гена гликокеназы нарушает глюкозочувствительный механизм b-клеток, что также ведет к снижению продукции инсулина. Таким образом, по-видимому, существуют категории лиц со значительно сниженной функцией b-клеток и соответственно повышенной чувствительностью к инсулину, либо с изначально сниженной чувствительностью к инсулину и соответственно повышенной секрецией инсулина, что до определенного времени компенсируется. Однако возможно и одновременное снижение обоих показателей, такая группа имеет самый высокий риск заболеть сахарным диабетом II типа. У лиц с изначально сниженным секреторным ответом b-клеток через 5 – 10 лет было обнаружено в 4,5 раза больше случаев нарушения толерантности к углеводам и ИНСД. Присоединение дополнительных факторов риска, таких как возраст, токсическое воздействие окружающей среды, отложение амилина, ожирение, “глюкозотоксичность” и других, также способствует развитию ИНСД. Это еще раз доказывает, что сахарный диабет II типа является многофакторным заболеванием, представляющим собой целый комплекс нарушений, образующихся в результате различных причин.
Однако, несмотря на достаточно убедительные доказательства сторонников теории первичности дисфункции b-клеток, с точки зрения современных данных все большее значение имеет ранняя инсулинорезистентность периферических тканей, ее расценивают главным и первичным звеном в цепи нарушений, ведущих к развитию ИНСД. Еще 20 лет назад Reaven и коллеги определили тканевую инсулинорезистентность, следствием которой является нарушение инсулинопосредованной утилизации глюкозы у больных ИНСД и НТГ. Последующие исследования с помощью эугликемического, гиперинсулинемического кламп-метода и минимальной модели подтвердили резистентность большинства тканей-мишеней таких больных к действию не только эндогенного, но и экзогенно вводимого инсулина. Кроме того, тот факт, что гиперинсулинемия, установленная у лиц с НТГ и в группе с повышенным риском развития ИНСД, не вызывает у них гипогликемии, косвенно свидетельствует об устойчивости тканей к действию инсулина, продуцируемого поджелудочной железой.
Таким образом, у больных с инсулинорезистентностью периферических тканей поддержание нормальной толерантности к глюкозе зависит от способности b-клеток продуцировать инсулин. В таком случае инсулиновый ответ компенсаторно повышается, что подтверждают многочисленные работы. Однако, с течением времени инсулинпродуцирующая способность b-клеток истощается и от степени нарушения этой функции зависит скорость нарастания гипергликемии. В дополнение к этому хроническая гипергликемия, сама по себе, может также вызывать структуральные изменения островковых клеток и снижать секрецию инсулина, а также уменьшать его способность стимулировать периферическую утилизацию глюкозы – феномен “глюкозотоксичности”.
Известно, что инсулинорезистентность может развиваться на уровне различных тканей-мишеней: скелетной мускулатуры, печени и жировой ткани. В литературе описано несколько возможных механизмов развития инсулинорезистентности: за счет уменьшения числа рецепторов к инсулину, изменения структуры и функции их отдельных субъединиц, нарушения активности белков-переносчиков глюкозы, а также в результате изменения активности фосфодиэстэразы и внутриклеточной цАМФ. Кроме того, инсулинорезистентность может быть обусловлена либо продукцией измененной молекулы инсулина, либо феноменом неполной конверсии проинсулина в инсулин.
Было установлено, что основным локусом инсулинорезистентности является мышечная ткань, в которой клетка может стать резистентной на 2 уровнях: рецептора и пострецепторных путей. Инсулиновый рецептор функционирует как погранично-мембранный фермент с регуляторной a-субъединицей и каталитической b-субъединицей. Инсулин связывается с a-субъединицей, в результате чего происходят конформационные изменения в рецепторе и повышение киназной активности в b-субъединице. Таким образом, действие инсулина, по сути, является каскадом процессов фосфорилирования/дефосфорилирования, которые являются важнейшим звеном в видоизменении сигнала и обеспечении множества заключительных биологических эффектов инсулина. У больных ИНСД было выявлено 50% снижение количества инсулиновых рецепторов, 80% уменьшение фосфорилирования инсулин рецепторного субстрата – 1 в печени и в мышцах, и 70% снижение фосфатидил-иноситол 3 киназной активности и ее количества на 25 – 34%. Более того, у больных ИНСД и лиц с избыточной массой тела активность тирозинкиназы снижена на 50 %.
В основе нарушения захвата глюкозы периферическими тканями более чем на 55%, с одной стороны, лежат указанные выше процессы, с другой – уменьшение числа транспортеров глюкозы – белков, расположенных на внутренней поверхности клеточных мембран и обеспечивающих транспорт глюкозы внутрь клетки. В настоящее время выделяют 2 класса транспортеров глюкозы – GluT: Na+ – контранспортеры, осуществляющие перенос глюкозы против градиента концентрации путем сопряжения захвата Na+ и глюкозы; и облегченные транспортеры, осуществляющие перенос глюкозы путем усиления механизмов пассивного транспорта. За последние годы удалось расшифровать ДНК транспортеров глюкозы и определить их функцию. Было описано 5 белков-транспортеров глюкозы с чутким распределением их на уровне различных органов и тканей. В частности GluT.1 и GluT.3 отвечают за основной или учредительный захват глюкозы, GluT.2 – за транспорт глюкозы к гепатоциту и, частично, к эпителиальным клеткам кишечника и почек, GluT.4 – за инсулинстимулированный захват глюкозы мышечной и жировой тканью, GluT.5 – за межклеточный транспорт к эпителиальным клеткам.
Другие потенциальные механизмы, позволяющие объяснить невосприимчивость к инсулину, включают усиление окисления липидов, изменения в плотности капилляров скелетных мышц, нарушение транспорта инсулина через сосудистый эндотелий, увеличение уровня амилина.
Рекомендуемая литература по данной проблеме может быть получена в редакции “Русского медицинского журнала”.
Источник
