Многоцентровые исследования по сахарному диабету
Сахарный диабет – это хроническое заболевание, которое характеризуется острой нехваткой гормона инсулина. Диабет приводит к нарушению обмена веществ, а также к повышению уровня глюкозы и сахара в крови. Последние исследования по сахарному диабету показывает, что болезнь опасна своими осложнениями.
Самые распространёнными, принято считать, инфаркты и инсульты. Также поражается и репродуктивная система человека. У мужчин наступает импотенция, а женщины начинают страдать бесплодием. На поздних стадиях диабет может привести к потере зрения.
Типы сахарного диабета и причины его возникновения
В медицине принято различать диабет I и II типа.
Диабет I типа наиболее часто встречается у детей и является инсулинозависимой формой.
Провоцируют заболевание в основном вирусные инфекции (краснуха) и наследственность.
Диабет II типа не так опасен для человека. Инсулин продолжает вырабатываться, однако, он не вступает во взаимодействие с клетками тела.
Причиной может стать ожирение и безглютеновые диеты.

Сахарный диабет – глобальная проблема всего мира.
На сегодняшний день им страдают около 422 млн человека, что составляет 6,028 % от всего населения планеты.
Причины этого заболевания до конца не изучены. Однако ученые полагают, что основной источник такой тенденции является малоподвижный образ жизни и негативная экологическая обстановка. Статистика заболеваемости диабетом ежегодно растет. По подсчетам «The Nation» к 2030 году сахарный диабет станет причиной каждой седьмой смерти на планете.
Страны-лидеры по числу носителей диагноза «Сахарный диабет». Данные ВОЗ 2017г.;
Индия (50,8 млн),
Китай (43,2)
США (26,8 млн),
Российская Федерация(5,6 млн)
Бразилия (7,6 млн)
Если сравнить с 1980 когда число заболевших не превышало 100 млн человек, то уже к 2016 это число возросло в более чем в 4 раза и составило 422 млн жителей Земли. Почти в 90 % случаев наблюдается именно диабет второго типа.
Особенности проблемы сахарного диабета в России.
Россия на сегодняшний день занимает четвертую строчку в этом рейтинг. Каждый год от диабета в нашей стране умирает около 200 тысяч человек.
По официальной статистике в России за 18 лет (2000-2018 года) число людей с этим диагнозом возросло на 2,5 млн человек!
В 2000 году насчитывалось 2,043 млн зарегистрированных диагнозов, а по итогам 2006 года уже 2,534 млн. За шесть лет количество граждан, страдающих диабетом возросло на миллион и составило 3,549 млн человек.
На 2016 число диабетиков увеличилось еще на миллион и стало 4,35 млн человек. И наконец, в 2018 году зарегистрировано 4 574 575 человек.
Из общего числа сахарный диабет второго типа у взрослых составил 4 237 291, у детей 913, у подростков 299.
Сахарный диабет первого типа у взрослых 219 857, детей 26 373, подростков 9 975. Такими ускоренными темпами, как и во всем мире, растет именно сахарный диабет второго типа. В то время как заболеваемость диабетом I типа почти не изменилась. Отсюда можно сделать вывод, что главной причиной распространения болезни – диаметральное изменение образа жизни всего человечества.
По подсчетам статистиков, если ситуация будет развиваться теми же темпами, то к 2025 году количество диабетиков возрастет в два раза, а то в 3 раза!

Современные исследования сахарного диабета в России.
К несчастью, универсального средства против сахарного диабета еще не изобрели. Но из-за растущей эпидемии, ученые всего мира предлагают свои методы лечения этой болезни.
Россия также не отстает, а во многом и опережает западных коллег. Ежегодно страна выделяет 375 млрд рублей на исследования сахарного диабета.
Стволовые клетки в лечении диабета.
Появилось абсолютно новое направление в лечении сахарного диабета – восстановление клеток поджелудочной железы. На конференции «Биомедицина-2016» в г. Новосибирске заявили, что ученым удалось получить клетки, производящие инсулин поджелудочной железы с помощью стволовых клеток. Так же медики отметили, что стволовые клетки способны полностью заменить пораженные клетки без вреда для организма.
ДНК вакцина.
Успешна, испытана и ДНК вакцина. Люди, страдающие сахарным диабетом первого типа, смогут забыть о постоянных инъекциях. Следует заметить, что эта вакцина уже успешна, испытана на человеке, а это означает, что уже в скором времени ее начнут массово применять среди населения нашей страны.
Естественное восстановление клеток поджелудочной железы.
Настоящей научной сенсацией стали российские исследования, которые проводились в Уральском университете. Исследователи (УрО РАН) научным путем выявили регенерирующие процессы в поджелудочной железе при сахарном диабете первого типа. Результаты полученных данных помогут разработать современные методы лечения сахарного диабета. Кроме того медикам уже удалось полностью восстановить поджелудочную железу крысе, страдающей этим заболеванием.
Пептидная иммунотерапия.
Есть и другие направления лечения сахарного диабета в России. Например, Пептидная иммунотерапия, которая позволяет перейти к клеточной технологии лечения. За основу взять принцип замещения поврежденных клеток, другими телами. С помощью особых связей, они будут производить инсулин вместо тех клеток, которые утратили такую функцию. В этом методе лечения будут использоваться стволовые клетки.
Инсулиновые помпы.
Если предыдущие методы лечения сахарного диабета напоминают фантастику то, этот уже внедрен и совершенствуется до сих пор. Речь идет, об инсулиновых помпах. Это медицинское устройство весом всего 50 грамм с системой контроля уровня сахара в крови.
По данным этого прибора врач может следить за течением болезни в режиме реального времени. Благодаря чему, отпадает постоянная необходимость визита к врачу. Инсулиновая помпа является хорошей альтернативой постоянным инъекциям и уколом гормона. В качестве резервуара для хранения инсулина применяется одноразовый картридж.
Пока инсулиновые помпы недоступны большей части населения из-за своей дороговизны. Стоимость одного устройства около 200 тысяч рублей. Также с ними нельзя заниматься активными видами спорта, прибор может выйти из строя. В настоящий момент ученые борются за то, чтобы система сама рассчитывала время и точное количество подачи инсулина. Тогда появится реальная альтернатива работы поджелудочной железы.

Разработки в области прогнозирования сахарного диабета.
Российскими научными сотрудниками внесен немалый вклад и в прогнозирование сахарного диабета. Ученые создали устройство способное на ранних стадиях выявить предрасположенность к этому заболеванию. Ими предложено сканирование ладоней рук для получения дермотоглифических данных, которые и определяют риск развития сахарного диабета.
По мнению министра здравоохранения Вероники Скворцовой, наиболее перспективным направлением являются клеточные технологии. Их использования успешно продолжаются с 2018 года.
Источники:
Федеральный источник больных сахарного диабета ФГБУ «НМИЦ Эндокринологии»
Подписаться на Дзен-канал «Социальный Авторитет»
Сахарный диабет: болезнь или неправильный способ жизни
Источник
[40-489] Развернутая диагностика сахарного диабета
2090 руб.
Исследование уровня основных клинико-лабораторных маркеров сахарного диабета (глюкозы крови, гликированного гемоглобина, С-пептида и инсулина), используемое для диагностики этого заболевания.
Синонимы русские
Анализы для диагностики сахарного диабета (СД).
Синонимы английские
Diabetes Mellitus (DM) Laboratory Panel; Laboratory Tests for Diabetes Diagnosis.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Диагностика сахарного диабета (СД) основывается на результатах лабораторного исследования метаболизма глюкозы. В настоящее время для диагностики СД используются следующие критерии (рекомендации Американской диабетической ассоциации, ADA, 2014 г.):
- глюкоза плазмы крови натощак ≥ 126 мг/дл (7,0 ммоль/л);
- – или глюкоза плазмы крови ≥ 200 мг/дл (11,1 ммоль/л) через 2 часа после нагрузки глюкозой (75 г глюкозы);
- – или глюкоза плазмы крови ≥ 200 мг/дл (11,1 ммоль/л) в случайном анализе при наличии классических признаков гипергликемии;
- – или гликированный гемоглобин HbA1C ≥ 6,5 %.
Хотя исследование на HbA1C давно применяется в клинике сахарного диабета, в качестве диагностического критерия этот маркер введен относительно недавно. Следует отметить, что некоторые клиницисты рекомендуют использовать HbA1C в качестве дополнительного критерия диагностики СД. Во избежание ошибок анализы на глюкозу и HbA1C рекомендуется повторить. Также исследование обязательно повторяют, если результаты отдельных тестов не согласуются между собой.
В большинстве случаев дифференциальную диагностику СД 1 и 2 типов проводят на основании клинической картины, возраста наступления болезни и данных наследственного анамнеза без каких-либо дополнительных объективных тестов, дифференцирующих два состояния. С другой стороны, единственным прямым методом оценки функции поджелудочной железы является исследование уровня инсулина в крови.
Исследование концентрации инсулина, однако, имеет некоторые ограничения, связанные с особенностями его метаболизма в норме и при патологии поджелудочной железы. Так, после секреции инсулин с током портальной крови направляется в печень, которая аккумулирует значительную его часть (эффект первого прохождения), и лишь затем поступает в системный кровоток. В результате этого концентрация инсулина в венозной крови не отражает уровень его секреции поджелудочной железой. Кроме того, концентрация инсулина значительно меняется при многих физиологических состояниях (например, прием пищи стимулирует выработку инсулина, а при голодании его уровень снижен). При наличии сахарного диабета измерение его концентрации становится менее точным. При появлении аутоантител к инсулину проведение химических реакций для его определения весьма затруднительно.
Более удобным маркером для оценки функции поджелудочной железы является С-пептид. С-пептид (от англ. сonnecting peptide – связующий, соединительный пептид) назван так потому, что соединяет α- и β-пептидные цепи в молекуле проинсулина. Благодаря тому, что С-пептид вырабатывается в равных (эквимолярных) инсулину концентрациях, этот лабораторный показатель можно использовать для оценки уровня эндогенного инсулина. С-пептид не подвергается эффекту первого прохождения в печени, а его концентрация в крови не зависит от изменения уровня глюкозы крови и относительно постоянна. Эти фармакокинетические особенности позволяют считать С-пептид наилучшим методом оценки выработки инсулина в поджелудочной железе.
На основании результатов исследования на инсулин и С-пептид можно провести более точную дифференциальную диагностику сахарного диабета. Для СД 2 типа характерна повышенная концентрация инсулина и С-пептида в начале заболевания и ее постепенное снижение с течением болезни. Для СД 1 типа типичен очень низкий или неопределяющийся уровень инсулина и С-пептида.
Развернутая диагностика сахарного диабета включает все четыре компонента: уровень глюкозы, гликированного гемоглобина, инсулина и С-пептида. Это исследование проводят при наличии клинических признаков диабета (жажда, полиурия, слабость, нарушение зрения, парестезии), но также и без каких-либо явных признаков этого заболевания пациентам с избытком массы тела (индекс массы тела, ИМТ ≥ 25 кг/м2) при наличии у них одного или нескольких следующих дополнительных факторов риска:
- малоподвижный образ жизни;
- наличие близкого родственника с СД;
- диабет беременных в анамнезе;
- артериальная гипертензия;
- ХС-ЛПВП менее 35 мг/дл и/или триглицериды более 250 мг/дл;
- синдром поликистозных яичников;
- нарушение толерантности к глюкозе или нарушение гликемии натощак в анамнезе;
- черный акантоз;
- заболевания сердца в анамнезе.
При подтверждении диагноза “СД” могут потребоваться дополнительные тесты, в том числе для оценки функции почек. Результат анализа оценивают с учетом всех значимых клинических, лабораторных и инструментальных исследований.
Для чего используется исследование?
- Для диагностики сахарного диабета;
- для дифференциальной диагностики 1 и 2 типов сахарного диабета.
Когда назначается исследование?
- При наличии клинических признаков диабета (жажда, полиурия, слабость, нарушение зрения, парестезии);
- при обследовании пациента с ИМТ ≥25 кг/м2 с одним или несколькими дополнительными факторами риска СД (малоподвижный образ жизни, артериальная гипертензия, дислипидемия и другие).
Что означают результаты?
Референсные значения
- Гликированный гемоглобин (HbA1c): https://helix.ru/kb/item/06-014#subj12
- [06-015] Глюкоза в плазме: https://helix.ru/kb/item/06-015#subj12
- [06-039] С-пептид в сыворотке: https://helix.ru/kb/item/06-039#subj12
- [08-026] Инсулин: https://helix.ru/kb/item/08-026
Критерии диагностики СД:
- глюкоза плазмы крови натощак ≥ 126 мг/дл (7,0 ммоль/л);
- – или глюкоза плазмы крови ≥ 200 мг/дл (11,1 ммоль/л) через 2 часа после нагрузки глюкозой (75 г глюкозы);
- – или глюкоза плазма крови ≥ 200 мг/дл (11,1 ммоль/л) в случайном анализе при наличии классических признаков гипергликемии;
- – или HbA1C ≥ 6,5 %.
Критерии дифференциальной диагностики 1 и 2 типов СД:
СД 1 тип | СД 2 тип | |
Инсулин и С-пептид | Снижен или не определяется | Повышен или норма (в начале болезни) Снижен (при прогрессировании болезни) |
Что может влиять на результат?
- Прием пищи;
- физическая активность;
- стресс;
- наличие в крови аутоантител к инсулину (для анализа на инсулин);
- введение эндогенного инсулина или секретогенов, например препаратов сульфонилмочевины (для анализа на инсулин и С-пептид).
Важные замечания
- Для получения точного результата необходимо следовать рекомендациям по подготовке к тесту;
- результат анализа оценивают с учетом всех значимых клинических, лабораторных и инструментальных исследований.
Также рекомендуется
[40-505] Альбумин-креатининовое соотношение (альбуминурия в разовой порции мочи)
[06-114] Альбумин в моче (микроальбуминурия)
[06-021] Креатинин в сыворотке (с определением СКФ)
[13-008] Антитела к инсулину
[06-115] Глюкоза в моче
[06-134] С-пептид в суточной моче
[13-016] Антитела к островковым клеткам поджелудочной железы
[42-014] Генетический риск развития гипергликемии
Кто назначает исследование?
Терапевт, врач общей практики, педиатр, эндокринолог.
Литература
- American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care. 2014 Jan;37 Suppl 1:S81-90.
- Handelsman Y. et al. American Association of Clinical Endocrinologists Medical Guidelines for Clinical Practice for developing a diabetes mellitus: comprehensive care plan.Endocr Pract. 2011 Mar-Apr;17 Suppl 2:1-53.
Источник
В обзоре рассматриваются изучаемые в рамках клинических исследований способы подавления аутоиммунной реакции при стрессовом повреждении бета-клеток у больных сахарным диабетом 1 типа.
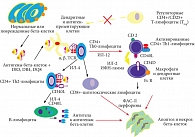
Рисунок. Иммунопатогенез СД 1 типа
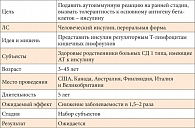
Таблица 1. Пероральный инсулин

Таблица 2. DiaPep277

Таблица 3. Нейласта (Neulasta)
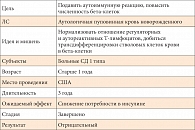
Таблица 4. Аутологичная пуповинная кровь
От идеи создания нового лекарственного средства до его выхода на рынок и широкого применения на практике в лучшем случае проходит 3 года, в худшем – 10-12 лет. Процесс вывода на рынок нового фармпрепарата выглядит примерно так: сначала рождается идея, затем разрабатываются технологии производства, потом продукт проходит доклинические испытания (раньше только на животных, теперь и на клеточных культурах в моделях in vitro), после этого – клинические исследования (КИ) и, наконец, выход на рынок. После этого на новом уровне проводятся дополнительные КИ.
Особенности проведения клинических испытаний
Как известно, существуют 4 фазы КИ. Нулевая и первая проводятся на здоровых добровольцах. На этих этапах прежде всего оцениваются безопасность препарата, а также различные фармакокинетические и фармакодинамические его параметры (объем распределения, скорость элиминации). Специфическая эффективность в отношении какого-либо заболевания оценивается во второй фазе КИ (при участии больных, в сравнении с плацебо или другими препаратами). Третья и четвертая фазы проводятся после выхода препарата на рынок, когда появляется возможность исследовать его эффективность на больших группах разных больных.
С учетом не только текущих испытаний, но и недавно закончившихся с тем или иным успехом, а также КИ, которые были прекращены по тем или иным причинам, на конец прошлого года в базе данных ClinicalTrials.Gov было зарегистрировано 135 975 КИ. На территории Российской Федерации в 2012 г. их число составило 2493, что немного меньше, чем в Японии (2534). Лидируют США (65 248), в Европе проведено 36 419 КИ. На долю сахарного диабета (СД) из общего количества (135 975) приходилось всего 9 тыс. испытаний (примерно 7%) – по 4 500 КИ в отношении лечения пациентов с СД 1 и 2 типа. С участием детей и подростков проведено КИ, касающихся СД 1 типа – 653, 2 типа – 586.
Актуальные вопросы профилактики и лечения СД 1 типа
Известно, что при этой патологии происходит аутоиммунное повреждение бета-клеток, в результате их количество, а также число других островковых клеток поджелудочной железы резко уменьшается. В результате формируется абсолютный дефицит инсулина. В соответствии с этими этапами патогенеза определяются мишени и цели проведения профилактики и лечения СД 1 типа: предупреждение аутоиммунной реакции, ее подавление, восстановление численности островковых клеток и нормализация секреции инсулина. Большое значение имеют коррекция метаболических нарушений (не только гипергликемии, но и дислипидемии, а также нарушений обмена других веществ), профилактика и лечение поздних осложнений СД. Согласно схеме иммунопатогенеза СД 1 типа (рис.), антигены нормальных или поврежденных бета-клеток представляются антиген-презентирующим клеткам. К ним, в частности, относятся дендритные клетки и др. Для представления антигенов, выходящих из бета-клеток, необходимы молекулы DR3, DR4, DQ8, которые мы обычно типируем для того, чтобы оценивать предрасположенность к СД.
Антиген-презентирующая клетка процессирует в себе антиген и через особые рецепторы представляет его CD4+ Th0-лимфоцитам. Эта популяция активируется под влиянием интерлейкина 12 (ИЛ-12) и превращается в активированные CD4+ Th1-лимфоциты. Другая часть Th0 под действием ИЛ-4+ превращается в CD4+ Тh2-лимфоциты, которые в дальнейшем будет стимулировать и вырабатывать ИЛ-4 и поверхностный антиген СD40L и стимулировать пролиферацию плазматических клеток, вырабатывающих специфические антитела уже к антигенам клеток. Основная роль в развитии дальнейшей аутоиммунной реакции разрушения бета-клеток принадлежит СD4+ Th0-лимфоцитам и СD4+ Th1-лимфоцитам. Первые за счет выработки ИЛ-4 стимулируют СD8-цитотоксические лимфоциты, а вторые – образование макрофагов и дендритных клеток, у которых возникла потеря толерантности по отношению к антигену бета-клеток. В цитотоксических лимфоцитах вырабатываются ФАС-лиганды (ФАС-Л) и перфорины – ферменты, которые играют ключевую роль в апоптозе и некрозе бета-клеток. Интерлейкин (ИЛ-1), фактор некроза опухоли (ФНО), оксид азота (NO), простагландин (ПГЕ-2) имеют тоже большое значение в гибели бета-клеток.На рисунке отражена лишь мизерная часть от общего числа молекул, участвующих в аутоиммунной реакции и разрушении бета-клеток при СД. И все же усилия ученых (иммунологов, иммуногенетиков, клеточных биологов, фармакологов), изучающих эти сложные процессы, постепенно начинают приносить плоды.
Проведенные КИ
Перечислю несколько, на мой взгляд, самых интересных КИ, три из которых уже доказали свою эффективность, а один вариант я специально привожу как пример неэффективного испытания.
Пример 1 Использование перорального инсулина для индукции толерантности к антигенам бета-клеток (табл. 1). Пероральный инсулин как средство профилактики начали применять в 1994 г. Это было первое и самое знаменитое в США исследование в области профилактики СД. Оно проводилось на сипсах больных с СД 1 типа и не дало никаких результатов. Частота заболеваемости не снизилась при лечении пероральным инсулином. В середине 2000-х гг. при ретроспективном анализе данных этого исследования выяснилось, что пероральный инсулин в определенных подгруппах пациентов все же снижает заболеваемость. Речь идет о тех пациентах, у которых в самом начале доклинического периода были антитела к инсулину, но не было других видов антител. Исследователи, организовавшие и проводившие КИ в 1990-х гг., все-таки получили разрешение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (United es Food and Drug Administration, FDA) на проведение повторного КИ уже на несколько измененных контингентах людей. Субъектами этого исследования являются здоровые родственники больных СД 1 типа (лица без каких-либо метаболических нарушений, характерных для СД). Эти люди имеют антитела к инсулину, но не имеют других видов антител. Их возраст составлял от 3 до 45 лет. В исследовании участвуют США, Канада, Австралия, Финляндия, Италия и Великобритания. Другие страны в исследование не принимаются. Ожидаемый эффект – снижение заболеваемости в 1,5-2 раза.
Пример 2 Это целая группа – 6 клинических многоцентровых испытаний, в которых исследуется синтетический белок теплового шока, точнее, его фрагмент DiaPeр277 (табл. 2). Что собой представляет белок теплового шока? Это антиген бета-клеток, который начинает на них экспрессироваться в условиях физиологического стресса (например, окислительный стресс при длительной перегрузке высокоуглеводной пищей у экспериментальных животных). Идея исследователей заключается в том, что если этот антиген будет вводиться путем подкожных инъекций к дендритным клеткам периферических лимфоузлов, то можно попытаться индуцировать толерантность к этому антигену и таким образом блокировать в самом зародыше аутоиммунную реакцию при стрессовом повреждении бета-клеток. В пилотных испытаниях уже было показано, что DiaPeр277 усиливает секрецию С-пептида у взрослых с впервые выявленным СД при длительности заболевания не более 6 месяцев. Эти результаты были встречены с большим интересом. В исследования включились 25 стран, в том числе Россия. В Москве они проводились в 4 исследовательских центрах: Эндокринологическом научном центре (проф. О.М. Смирнова), на кафедре эндокринологии и диабетологии Российской медицинской академии последипломного образования (проф. А.С. Аметов) и еще в 2 больших клиниках, причем только у взрослых. Официальные критерии включения – возраст от 18 до 66 лет, но в России в это исследование отбираются лица старше 22 лет.
Пример 3 КИ нацелено на подавление аутоиммунной реакции, но по другому принципу. В качестве лекарственного средства используется рекомбинантный фактор роста гранулоцитов (табл. 3). Идея такова: если мы будем вводить фактор роста гранулоцитов, он будет стимулировать размножение и дифференцировку гемопоэтических стволовых клеток в определенных направлениях, за счет этого удастся сбалансировать число регуляторных и аутореактивных Т-лимфоцитов. Если вернуться к схеме иммунопатогенеза СД 1 типа, то нужно отметить, что регуляторные Т-лимфоциты с фенотипом СD4+ и СD25+ играют очень важную роль в блокировании распознавания антиген-презентирующими клетками бета-клеточных антигенов. При срыве толерантности к антигенам бета-клеток этот блок перестает действовать. Препарат пэгфилграстим действительно приводит к увеличению относительного числа регуляторных Т-лимфоцитов и подавлению многих аутоиммунных процессов. Например, он эффективен при аутоиммунном ревматоидном артрите, системной красной волчанке, у некоторых пациентов с бронхиальной астмой. Именно на этом основании его пытаются использовать для подавления аутоиммунной реакции при СД 1 типа.
Пример 4 Провальное КИ (табл. 4). В Университете Флориды (Гейнсвилл, США) один научный сотрудник предложил использовать стволовые клетки (аутологичная пуповинная кровь) для того чтобы: 1) нормализовать отношения регуляторных и цитотоксических Т-лимфоцитов и 2) добиться трансдифференцировки введенных аутологичных стволовых клеток в бета-клетки. В этом исследовании участвовали дети (начиная от 1 года) с впервые выявленным СД 1 типа. Ожидался эффект снижения потребности в инсулине, но он не был достигнут. Более того, потребность в инсулине даже повысилась, а секреция С-пептида – снизилась. Примерно в 30% случаев результаты КИ оказываются не только не эффективными, но и приводят к ухудшению ситуации.
Каковы перспективы?
Родители пациентов – детей с первые выявленным СД 1 типа часто спрашивают: «Неужели нужна только инсулинотерапия?» На протяжении 10 лет я им говорю: «В самое ближайшее время появятся принципиально новые средства лечения СД 1 типа, которые будут подавлять аутоиммунную реакцию и, вероятно, вы когда-нибудь сможете избавиться от инсулинотерапии». 10 лет назад я в это свято верил, 5 лет назад у меня возникли в этом сомнения. А сейчас я абсолютно уверен в том, что через 4-5 лет на рынке появится альтернатива инсулину – достаточно специфичные иммуносупрессоры, направленные на подавление аутоиммунной реакции при СД 1 типа.
Источник

