Прорыв в области лечения диабета 1 типа
Сахарный диабет первого типа, который обычно развивается у детей и подростков, является хроническим заболеванием. Последние два года в Израиле и других странах ведутся интенсивные исследования этого заболевания, результаты которых заставляют ученых полностью пересмотреть традиционный подход к лечению сахарного диабета.
Считается, что сахарный диабет первого типа является аутоиммунным заболеванием, при котором происходит разрушение бета-клеток поджелудочной железы, ответственных за выработку инсулина — гормона, с помощью которого сахар (глюкоза) проникает в клетки организма. При разрушении бета-клеток количество выделяемого инсулина уменьшается и уровень сахара в крови повышается, что приводит к поражению кровеносных сосудов и другим пагубным последствиям для организма.

Несмотря на долгие годы исследований, ученые пока что не могут объяснить, почему организм разрушает собственные бета-клетки. Одна из теорий гласит, что причиной является вирусное заражение, при котором на молекулярном уровне вирусы похожи на бета-клетки, таким образом защитная реакция организма может быть ошибочно направлена на данный вид клеток. Согласно другой теории, причиной аутоиммунной атаки организма является излишняя стерильность, в которой растут дети, что приводит к повышенной чувствительности иммунной системы к собственным бета-клеткам поджелудочной железы.
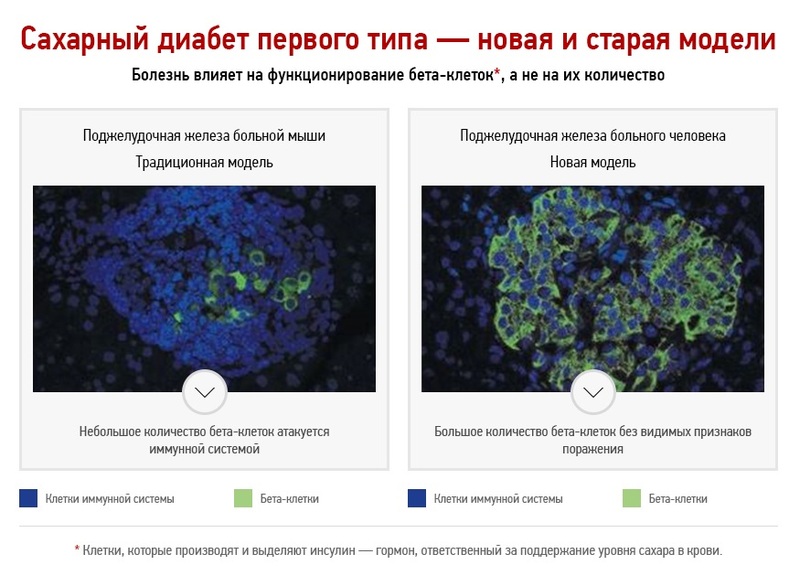
Классическая модель развития сахарного диабета первого типа
Принятая на сегодня теория развития сахарного диабета первого типа гласит, что первая стадия заболевания продолжается от нескольких месяцев до нескольких лет, в течение которых происходит постепенное разрушение бета-клеток поджелудочной железы. Заболевание не диагностируется на начальной стадии, потому что оставшиеся клетки начинают выделять больше инсулина, чтобы скомпенсировать его недостаток в крови. Сахарный диабет первого типа диагностируется, когда остается только 10 % бета-клеток, уже не способных выделять достаточно инсулина для поддержания требуемого уровня сахара в крови. На этом этапе пациент получает лечение — иньекции инсулина, параллельно с этим происходит полное уничтожение организмом оставшихся бета-клеток. Так как разрушение бета-клеток является необратимым процессом, пациент вынужден получать лечение на протяжении всей жизни.
Данная модель на протяжении многих лет оказывала огромное влияние на исследование сахарного диабета первого типа. Основным предположением было то, что на момент диагностики у пациента практически не остается бета-клеток поджелудочной железы. Старая модель основывалась на исследованиях, проведенных на одном виде мышей, развивающих болезнь, похожую на сахарный диабет первого типа у людей, а также на наблюдениях онкологических пациентов, у которых была удалена часть поджелудочной железы.
Новые исследования
В последние два года, благодаря значительным логическим усилиям, ученые получили возможность изучать десятки образцов тканей поджелудочной железы пациентов, страдающих сахарным диабетом первого типа, которые умерли незадолго после диагностики заболевания. Речь идет о редких и трагических случаях, когда пациенты (в основном дети) погибали при несчастных случаях, а семьи соглашались пожертвовать их органы для исследований.
Анализ образцов ткани этих пациентов показал неожиданные результаты. Оказалось, что в тканях поджелудочной железы имеется большое количество бета-клеток без видимых признаков поражения со стороны иммунной системы, а их количество значительно выше, чем 10 % здоровых клеток (согласно классической модели). Таким образом, ученые пришли к выводу, что на этапе диагностики сахарного диабета у человека имеется большое количество незатронутых иммунной системой бета-клеток.
Данное открытие проливает свет на известный в медицине эффект при начале лечения сахарного диабета первого типа с помощью инсулина, при котором в течение первых месяцев происходит временное «выздоровление», когда бета-клетки начинают вырабатывать инсулин в достаточном количестве. Классическая модель не может объяснить, каким образом такое небольшое количество бета-клеток выделяет достаточно инсулина. Новое исследование утверждает, что происходит функциональное поражение клеток, и при «разгрузке» с помощью инъекций инсулина их функции временно восстанавливаются, что было бы невозможно, если бы клетки были разрушены.
Важно отметить, что в организме происходит аутоиммунная реакция, направленная на разрушение бета-клеток поджелудочной железы. Однако, согласно новым исследованиям, происходит не уничтожение бета-клеток, а нарушение их функционирования, поэтому можно надеяться, что поражение такого рода может быть обратимым.
Какие последствия будет иметь данное открытие?
Теперь, когда известно, что на момент диагностики сахарного диабета первого типа имеется достаточно бета-клеток, пациент должен получать лекарства, нейтрализующие иммунную систему с целью предотвращения нарушения функционирования этих клеток. Разработка таких лекарств уже ведется. Другим направлением будут лекарства, которые смогут вернуть способность вырабатывать инсулин пораженным клеткам или обеспечить достаточную выработку инсулина оставшимися клетками. Ученые пока что далеки от создания подобных препаратов, но главное, что результаты последних исследований показали верный путь для лечения этого заболевания.
12895 просмотров
Источник
Российские исследователи разработали вещества, из которых можно сделать препарат для восстановления и поддержания здоровья поджелудочной железы при диабете первого типа.
 Новое вещество, синтезированное российскими учеными, способно восстанавливать поврежденную диабетом поджелудочную железу
Новое вещество, синтезированное российскими учеными, способно восстанавливать поврежденную диабетом поджелудочную железу
В поджелудочной железе есть особые участки под название Островки Лангерганса – именно они синтезируют в организме инсулин. Этот гормон помогает клеткам усваивать глюкозу из крови, а его нехватка — частичная или тотальная – вызывает повышение уровня глюкозы, что приводит к диабету.
Избыток глюкозы нарушает биохимическое равновесие в организме, происходит окислительный стресс, и в клетках образуется слишком много свободных радикалов, которые нарушают целостность этих клеток, вызывая их повреждения и гибель.
Также в организме происходит гликирование, при котором глюкоза соединяется с белками. У здоровых людей этот процесс тоже идет, но гораздо медленнее, а при диабете ускоряется и повреждает ткани.
Своеобразный замкнутый круг наблюдается у людей с диабетом первого типа. При нем клетки Островков Лангерганса начинают отмирать (врачи считают, что это происходит из-за аутоиммунной атаки самого организма), и, хотя они умеют делиться, восстановить свое изначальное количество не могут, так как из-за гликирования и окислительного стресса, вызванного избытком глюкозы, гибнут слишком быстро.
На днях журнал Biomedicine & Pharmacotherapy опубликовал статью о результатах нового исследования ученых из Уральского федерального университета (УрФУ) и Института иммунологии и физиологии (ИИФ УрО РАН). Специалисты обнаружили, что вещества, произведенные на основе 1,3,4-тиадиазина, подавляют упомянутую выше аутоиммунную реакцию в виде воспаления, губящего инсулиновые клетки, и, одновременно, устраняют последствия гликирования и окислительного стресса.
У мышей с диабетом первого типа, на которых испытывали производные 1,3,4-тиадиазина, значительно уменьшался уровень воспалительных иммунных белков в крови и пропадал гликированный гемоглобин. Но самое главное, у животных в три раза возрастало количество синтезирующих инсулин клеток в поджелудочной железе и повышался уровень самого инсулина, что снижало концентрацию глюкозы в крови.
Вполне вероятно, что созданные на базе названных выше веществ новые препараты совершат переворот в лечении диабета первого типа и подарят миллионам больных гораздо более радужные перспективы на будущее.
Будьте осторожны
По данным ВОЗ каждый год в мире от сахарного диабета и вызванных им осложнений умирает 2 миллиона человек. При отсутствии квалифицированной поддержки организма диабет приводит к различного рода осложнениям, постепенно разрушая организм человека.
Из осложнений чаще всего встречаются: диабетическая гангрена, нефропатия, ретинопатия, трофические язвы, гипогликемия, кетоацидоз. Диабет может приводить и к развитию раковых опухолей. Практически во всех случаях диабетик или умирает, борясь с мучительной болезнью, или превращается в настоящего инвалида.
Что же делать людям с сахарным диабетом? Эндокринологическому научному центру РАМН удалось сделать средство полностью вылечивающее сахарный диабет.
В настоящее время проходит Федеральная программа “Здоровая нация”, в рамках которой каждому жителю РФ и СНГ данный препарат выдается БЕСПЛАТНО. Подробную информацию, смотрите на официальном сайте МИНЗДРАВА.
Делаем выводы
Если вы читаете эти строки, можно сделать вывод, что Вы или Ваши близкие больны сахарным диабетом.
Мы провели расследование, изучили кучу материалов и самое главное проверили большинство методик и препаратов от сахарного диабета. Вердикт таков:
Все препараты если и давали, то лишь временный результат, как только прием прекращался – болезнь резко усиливалась.
Единственный препарат, который дал значительный результат – это Дифорт.
На данный момент это единственный препарат, который способен полностью излечить сахарный диабет. Особенно сильное действие Дифорт показал на ранних стадиях развития сахарного диабета.
Мы обратились с просьбой в Министерство Здравоохранения:
И для читателей нашего сайта теперь есть возможность
получить Дифорт БЕСПЛАТНО!
Внимание! Участились случаи продажи поддельного препарата Дифорт.
Делая заказ по ссылкам выше, вы гарантированно получите качественный продукт от официального производителя. Кроме того, заказывая на официальном сайте, вы получаете гарантию возврата средств (включая транспортные расходы), в случае если препарат не окажет лечебного действия.
Источник
Сахарный диабет – заболевание, приводящее к пожизненным инъекциям инсулина, инвалидности и фатальным осложнениям. Ученые из Приволжского исследовательского медицинского университета (ПИМУ) приступили к разработке принципиально нового метода лечения этого недуга.
Чтобы понять механизм технологии, нужно сказать о том, как работает поджелудочная железа, отчего возникает диабет. В этом органе есть так называемые бета-клетки, объединенные в островки, которые автоматически продуцируют инсулин в ответ на повышение уровня глюкозы в крови. При ряде аутоиммунных или хронических болезней общая их масса снижается, появляются функциональные нарушения в виде недостаточной выработки инсулина. Результат – повышение уровня глюкозы в сыворотке крови.
– Это инсулинопотребный сахарный диабет. Он возникает, если число островков уменьшилось на 80 процентов, – рассказывает заведующий кафедрой факультетской хирургии и трансплантологии, главный внештатный трансплантолог минздрава Нижегородской области Владимир Загайнов.
Ученый подчеркивает, что метод лечения диабета только один – трансплантация поджелудочной железы. Потребность в этой операции в России удовлетворяется на тысячные доли процента, что связано с дефицитом донорских органов. Во всех остальных случаях речь идет о компенсации заболевания с помощью инсулина. Однако даже пересадка сопряжена с необходимостью иммуносупрессивной терапии, чтобы организм пациента не отторгал донорский орган. А у нее есть свои минусы, особенно в отдаленном периоде.
Главная идея проекта – пересадка не всей поджелудочной железы, а только островков, состоящих из тех самых бета-клеток.
– Островки будут выделяться из донорской железы специальным способом. Даже если целая железа не годится для трансплантации, из нее можно попытаться выделить островки и пересадить их, – поясняет Владимир Загайнов.
В мире эту идею пытаются реализовать разными способами и с разной степенью успешности. Введение островков от донора требует все той же небезопасной иммуносупрессивной терапии. В ПИМУ ученые разрабатывают вариант пересадки клеток, заключенных в специальные пористые капсулы. В теории клетки приживаются и начинают вырабатывать инсулин. Человек излечивается от диабета. А поры капсулы достаточно малы, чтобы предотвратить атаку иммунных клеток организма, поэтому никакой иммуносупрессивной терапии не требуется. Важно, что речь идет о малоинвазивных операциях, а не о сложной трансплантации. Возможных вариантов несколько: введение в брюшную полость путем пункции либо введение в печень по воротной вене.
Первые эксперименты ученых из НИИ экспериментальной онкологии и биомедицинских технологий ПИМУ вместе с Институтом металлоорганической химии РАН оказались успешными.
– В отдаленной перспективе планируем проработать выращивание бета-клеток из стволовых, – говорит Владимир Загайнов. – Параллельно вместе с коллегами из Национального медицинского исследовательского центра трансплантологии и искусственных органов имени Шумакова занимаемся легитимизацией технологии. Раньше в России за это никто не брался, поэтому трансплантация островков бета-клеток поджелудочной пока не вошла в список разрешенных, хотя в мире это уже существует. Надеемся, что в ближайшее время вопрос будет решен.
Планируем проработать выращивание бета-клеток из стволовых
В 2022 году проект, выполняемый по госзаданию Минздрава России, завершится. Можно будет испытывать метод на животных, а затем заниматься регистрацией. На мой вопрос, когда лечение будет доступно российским пациентам, профессор Загайнов ответил кратко:
– Деклараций в жизни хватает, давайте заниматься делом.
Комментарий
Ольга Занозина, доктор медицинских наук, заведующая отделением эндокринологии Нижегородской областной больницы имени Семашко:
– Наряду с совершенствованием самих инсулинов, способов их введения в организм пациента, улучшением терапевтического обучения больных сахарным диабетом развивается и другое направление – трансплантационные технологии, позволяющие вводить бета-клетки островков поджелудочной железы, которые вырабатывают инсулин, в организм больного человека.
Положительный эффект достигается при виртуозном заборе, хранении и введении островковых клеток больному человеку. При успешном результате – почти полный контроль за гликемией, отсутствие гипогликемий и потребности в экзогенном инсулине. Вся эта работа требует ювелирного мастерства.
Источник
Ученые Гарвардского университета сообщили о том, что им удалось разработать способ массового получения в лабораторных условиях нормально функционирующих, зрелых, вырабатывающих инсулин бета-клеток поджелудочной железы. Авторы метода утверждают, что теперь человечество находится в шаге от реализации мечты миллионов больных и их близких – полному излечению от диабета 1 типа.
В пятницу стало известно о прорыве в поиске эффективных методов лечения диабета 1 типа. Ученые Гарвардского университета сообщили о том, что им удалось разработать способ массового получения в лабораторных условиях из столовых клеток нормально функционирующих, зрелых, вырабатывающих инсулин бета-клеток поджелудочной железы. Причем в количествах, достаточных для трансплантации пациентам, чьи бета-клетки убиты собственной иммунной системой.
Авторы метода утверждают, что теперь человечество находится буквально в шаге от реализации мечты миллионов больных и их близких – полному излечению от диабета 1 типа. Среди них – и ведущий автор опубликованной в журнале Cell работы, биолог, специалист по стволовым клеткам Дуглас Мелтон (Douglas Melton). После того, как около 20 лет тому назад его маленькому сыну, а позже и дочери, был поставлен диагноз «диабет 1 типа», ученый посвятил свою жизнь и научную карьеру поиску средств лечения и уверен, что добился своего.
{#vrez.58707}
Клетки на замену
Как известно, поджелудочная железа в течение дня регулирует уровень глюкозы в крови с помощью секреции бета-клетками, расположенными в так называемых островках Лангерганса, гормона инсулина. При сахарном диабете 1 типа клетки собственной иммунной системы организма, по невыясненным пока причинам, проникают в островки Лангерганса и уничтожают бета-клетки. Недостаток инсулина приводит к таким тяжелым последствиям, как нарушение сердечной функции, потеря зрения, инсульт, почечная недостаточность и другим. Больным приходится пожизненно несколько раз в день делать себе инъекции подобранных доз инсулина, однако абсолютно точного соответствия естественному процессу выброса гормона в кровь добиться все же невозможно.
Ученые всего мира уже в течение десятилетий ищут способы замены утраченных из-за аутоиммунного процесса бета-клеток. В частности, был разработан метод трансплантации инсулоцитов (клеток островков Лангерганса), выделенных из донорских поджелудочных желез. Однако этот метод остается экспериментальным, доступным из-за нехватки донорских органов лишь небольшому числу пациентов. Кроме того, трансплантация донорских клеток, для предотвращения их отторжения, требует постоянного приема мощных иммуноподавляющих препаратов со всеми сопутствующими негативными побочными эффектами.
После изоляции в 1998 году эмбриональных стволовых клеток, потенциально способных превращаться в любые клетки организма, целью многих научных групп стали поиски методов получения функционирующих бета-клеток именно из них. Нескольким командам удалось in vitro (вне живого организма) трансформировать эмбриональные клетки в клетки-предшественники (прекурсоры) инсулоцитов, которые затем дозревают, будучи помещенными в организмы специально выведенной линии лабораторных животных и начинают вырабатывать инсулин. Процесс созревания занимает около шести недель.
В частности, такого успеха добились специалисты из Калифорнийского университета (Сан-Диего). 9 сентября они, совместно с местной биотехнологической компанией ViaCyte, объявили о начале первых в своем роде клинических испытаний экспериментального препарата VC-01, представляющего собой выращенные из эмбриональных стволовых клеток прекурсоры бета-клеток, помещенные в полупроницаемую оболочку. Предполагается, что первая фаза испытаний, призванная оценить эффективность, переносимость и безопасность различных доз препарата, продлится два года, в ней примут участие примерно 40 пациентов. Исследователи ожидают, что многообещающие результаты, полученные в ходе экспериментов на животных, удастся повторить на людях и имплантированные под кожу прекурсоры бета-клеток созреют и начнут производить нужное организму количество инсулина, что позволит пациентам отказаться от инъекций.
Помимо эмбриональных стволовых клеток, источником для получения инсулоцитов могут быть и индуцированные плюрипотентные стволовые клетки (iPSC) – незрелые клетки, перепрограммированные из зрелых и потенциально способные специализироваться в клетки всех типов, присутствующих во взрослом организме. Однако эксперименты показали, что этот процесс очень сложен и долог, а получающиеся бета-клетки лишены многих характеристик «родных» клеток.
Поллитра бета-клеток
Тем временем группа Мелтона заявила, что разработала метод, позволяющий избежать всех недостатков – источником инсулоцитов могут быть как эмбриональные стволовые клетки, так и iPSC, весь процесс происходит in vitro, а на выходе уже через 35 дней получается полулитровый сосуд с 200 миллионами зрелых, нормально функционирующих бета-клеток, что, теоретически, достаточно для трансплантации одному пациенту. Сам Мелтон назвал получившийся протокол «воспроизводимым, но очень кропотливым». «Никакого волшебства, только десятилетия упорной работы», – цитирует его журнал Science. Протокол включает поэтапное введение в очень точно подобранной комбинации пяти различных факторов роста и 11 молекулярных факторов.
{#vrez.58708}
Пока метод Мелтона показал отличные результаты в экспериментах на мышиной модели диабета 1 типа. Через две недели после трансплантации в организм больных диабетом мышей, полученные из стволовых клеток человеческие бета-клетки поджелудочной железы начали вырабатывать достаточное количество инсулина для того, чтобы вылечить животных.
Однако, прежде, чем перейти к испытаниям на людях, Мелтону и его коллегам необходимо решить еще одну проблему – как защитить трансплантат от атаки иммунной системы. Тот же самый аутоиммунный процесс, ставший причиной болезни, может затронуть новые бета-клетки, полученные из собственных iPSC пациента, а инсулоциты, полученные из эмбриональных стволовых клеток, могут стать мишенью для нормального иммунного ответа, как чужеродные агенты. В настоящее время группа Мелтона в сотрудничестве с другими научными центрами работает над тем, как наиболее эффективно решить эту проблему. Среди вариантов – помещение новых бета-клеток в некую защитную оболочку либо их модификация с тем, чтобы они могли не поддаваться атаке иммунных клеток.
Мелтон не сомневается, что эта трудность будет преодолена. По его мнению, клинические испытания его метода начнутся в течение ближайших нескольких лет. «Нам сейчас остается всего один шаг до финиша», – считает он.
Источник
