Биохимические механизмы нарушения обмена углеводов при сахарном диабете
Страница 1 из 3
Сахарный диабет (СД) – полиэтиологическое заболевание, связанное:
- со снижением количества β клеток островков Лангерганса,
- с нарушениями на уровне синтеза инсулина,
- с мутациями, приводящими к молекулярному дефекту гормона,
- со снижением числа рецепторов к инсулину и их аффинности в клетках-мишенях,
- с нарушениями внутриклеточной передачи гормонального сигнала.
Выделяют два основных типа сахарного диабета:
1. Инсулинзависимый сахарный диабет (ИЗСД, диабет 1 типа) – диабет детей и подростков (ювенильный), его доля составляет около 20% от всех случаев СД.
2. Инсулиннезависимый сахарный диабет (ИНЗСД, диабет 2 типа) – диабет взрослых, его доля – около 80%.
Подразделение типов СД на взрослый и ювенильный не всегда корректно, так как встречаются случаи развития ИНЗСД в раннем возрасте, также ИНЗСД может переходить в инсулинзависимую форму.
Причины сахарного диабета
Недостаточный синтез инсулина
Развитие ИЗСД (СД 1 типа) обусловлено недостаточным синтезом инсулина в β-клетках островков Лангерганса поджелудочной железы. Среди причин этого в настоящее время на первый план выдвигаются аутоиммунные поражения и инфицирование β-тропными вирусами (вирусы Коксаки, Эпштейна-Бар, эпидемического паротита).
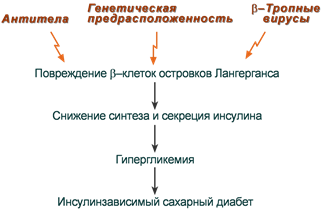
Причины инсулинзависимого сахарного диабета
Помним, что проницаемость стенки кишечника у младенцев выше, чем у взрослых, и это позволяет в первые дни и месяцы жизни сформировать у него пассивный иммунитет за счет перехода антител матери в кровь ребенка.
В связи с этим при использовании коровьего молока или молочных смесей для вскармливания младенцев имеется риск развития ИЗСД из-за возможного развития иммунного ответа на молочный альбумин и переключения иммунной атаки на β-клетки поджелудочной железы.
Происходит это в результате того, что некоторые пептидные участки альбумина коровьего молока и человеческого инсулина схожи между собой. Поэтому при проникновении их через кишечный барьер у детей-носителей антигенов главного комплекса гистосовместимости D3/D4 может возникнуть перекрестная иммунная реактивность и, как следствие, аутоиммунный ответ против собственных β-клеток, что приводит к инсулинзависимому сахарному диабету.
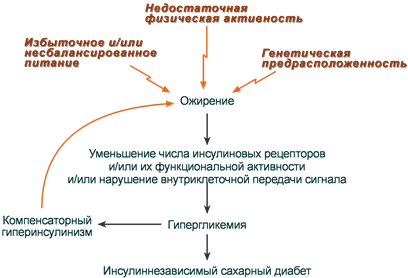
Нечувствительность клеток к инсулину
Для ИНЗСД (СД 2 типа) ведущей причиной является инсулинорезистентность из-за снижения чувствительности клеток-мишеней к гормону. Здесь выделяют две глобальные причины:
- снижение активности рецепторов (рецепторные механизмы),
- нарушение проведения сигнала от рецептора к внутриклеточным ферментам (пострецепторные механизмы).
Рецепторные механизмы
Функциональные нарушения рецепторов – замедляют связывание инсулина и ответ на него:
- увеличение диаметра и площади поверхности жировых клеток (ожирение) – снижение скорости образования рецепторных микроагрегатов,
- повышенная вязкость мембран (снижение доли ненасыщенных жирных кислот в фосфолипидах, увеличение содержания холестерина),
- блокирование инсулиновых рецепторов антителами,
- нарушение мембран в результате активации процесов ПОЛ.
Структурные нарушения рецепторов – не позволяют связываться с гормоном или отвечать на его сигнал.
- изменение конформации рецепторов инсулина при воздействии свободных радикалов (продуктов окислительного стресса).
Пострецепторные механизмы
Пострецепторные механизмы сопровождаются ослаблением проведения сигнала через фосфатидилинозитол-4,5-дифосфат-3-киназный путь (ФИ-3-киназный).
В настоящее время ослабление проведения сигнала через IRS-ФИ-3-киназный путь считают главной причиной инсулинорезистентности.
В результате развиваются снижение активации белков этого сигнального пути, отсутствие быстрых эффектов инсулина, а именно активации трансмембранных переносчиков глюкозы (ГлюТ4) и метаболических ферментов утилизации глюкозы.
Предложено два механизма нарушения ФИ-3-киназного пути:
- Фосфорилирование серина (но не тирозина) в составе IRS уменьшает его способность связываться с ФИ-3-киназой и ослабляет ее активирование. Данный процесс катализируется множеством серин-треониновых киназ, активность которых повышается при воспалении, стрессе, гиперлипидемиях, ожирении, переедании, дисфункции митохондрий.
- Нарушение баланса между количеством субъединиц ФИ-3-киназы (p85 и p110), т.к. эти субъединицы могут конкурировать за одни и те же участки связывания с белком IRS. Этот дисбаланс меняет активность фермента и снижает передачу сигнала. Причиной патологического повышения отношения p85/p110 предполагают высококалорийное питание.

Причины развития инсулиннезависимого сахарного диабета
Развивающуюся при беременности инсулинорезистентность связывают с увеличенной экспрессией в клетках скелетных мышц субъединицы p85, вызванной повышением концентрации человеческого плацентарного гормона роста. Соответственно, изменяется соотношение p85/p110 и ухудшается развертывание быстрых эффектов инсулина.
Главное место в организме принадлежит глюкозе, это самый распространенный углевод. Углеводы, простые и сложные сахара входят в состав АТФ, АДФ, в форме гликозаминогликановони являются составной частью мембран клеток и субклеточных структур, а также межклеточного вещества. На долю углеводов приходиться 2% от массы животного. Сахара участвуют в дезинтоксикации организма (глюкуроновая кислота). Углеводы являются важнейшим субстратом, из которого синтезируется энергия в форме АТФ.
Нарушение обмена углеводов может происходить на всех его этапах – от расщепления и всасывания в пищеварительном тракте до усвоения простых сахаров в тканях и клетках. Одна их важнейших функций печени состоит в поддержании нормального уровня глюкозы в крови (4,6 – 5,2 ммоль/л). При снижении этого уровня клетки печени повышают его за счет расщепления гликогена, а при увеличении уровня глюкозы в крови они утилизируют ее. Эта регуляция осуществляется с помощью 2 процессов: распада гликогена до глюкозы (гликогнолиз) и синтеза гликогена из глюкозы (гликогенез).Из крови простые сахара (глюкоза) поступают в различные ткани и клетки, где они могут депонироваться в форме гликогена (за исключением мозга), использоваться в различных пластических процессах или расщепляться в анаэробном гликолизе до молочной кислоты, а в тканевом дыхании – до двуокиси углерода и воды.
Нарушения углеводного обмена проявляются гипер-илигипогликемией (повышением или понижением концентрации глюкозы в крови).
Причинами гипогликемии может бытьалиментарная гипогликемия(при длительном голодании); чрезмерная и длительная физическая нагрузка; повреждение клеток печени; увеличение уровня инсулина в крови, рвота и диарея. Гипогликемические состояния чрезвычайно опасны, поскольку могут привести кгипогликемической коме(мышечная слабость, потливость, потеря координации движений).
Причины гипергликемии разнообразны: прием кормов с повышенным содержанием углеводов, возбуждение, активизация симпатической нервной системы. Уменьшение образования инсулина в организме может приводить к развитию сахарного диабета. При этом отмечается гипергликемия (содержания сахара в 5 -6 раз превышает норму), глюкоза, как пороговое вещество, начинает выводиться почками, а клетки испытывают углеводное голодание. Увеличиваетсяглюконеогенез, глюкозурия, кетонемия, развивается диабетическая кома.
Практически невозможно встретить полное отсутствие питательных веществ в рационе животного (белков, жиров, углеводов); поэтому чаще говорят об их недостатке (качественное голодание) или избытке.
Сахарный диабет.
Сахарный диабет (Diabetes mellitus)-хроническое нарушение углеводного обмена с явлениями гипергликемии глюкозурии.
Болезнь возникает вследствие недостаточной секреции инсулина, а также гиперфункции передней доли гипофиза. Длительные стрессы, переутомления на фоне перекармливания углеводами, ожирение, дисфункции эндокринной системы, воспаления поджелудочной железы, инфекционные болезни – наиболее частые причины сахарного диабета.
При недостатке инсулина моно- и дисахариды недостаточно переводятся в гликоген, отчего растет их содержание в крови. Накапливаясь выше нормы, сахар начинает выделяться с мочой, где его концентрация может увеличиваться до 4-16 мг%. Глюкозурия может нарастать под влиянием гиперсекреции глюкагона, глюкокортикоидов и гормонов передней доли гипофиза. Это приводит к эксикозу, полидипсии. Нарушается промежуточный обмен (гиперкетонемия, ацидоз). Болезнь может привезти к диабетической коме и гибели животного. Болезнь неизлечима.
Наблюдаются полидипсия, полиурия, булимия, бледность сухость слизистых, вялость, утомляемость, угасание половой потенции и двигательной активности, гипергликемия, глюкозурия, кетоз, ацидоз, диабетическая кома, тахисистолия, гипотермия. Это – основные признаки болезни для постановки диагноза. При этом следует исключить другие формы глюкозурии (физиологической – при переедании сахара, токсической – при отравлении свинцом, мышьяком).
Соседние файлы в предмете Патологическая физиология
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Сахарный диабет
Сахарный диабет (Diabetes mellitus) – широко распространенное заболевание, которое наблюдается при абсолютном или относительном дефиците инсулина. Нехватка этого пептидного гормона (см. сс. 78, 82) отражается главным образом на обмене углеводов и липидов. Сахарный диабет встречается в двух формах. При диабете I типа (инсулинзависимом сахарном диабете) уже в раннем возрасте происходит гибель инсулинсинтезирующих клеток в результате аутоиммунной реакции. Менее тяжелый диабет II типа (инсулиннезависимая форма) обычно проявляется в более пожилом возрасте. Он может быть вызван различными причинами, например пониженной секрецией инсулина или нарушением рецепторных функций.
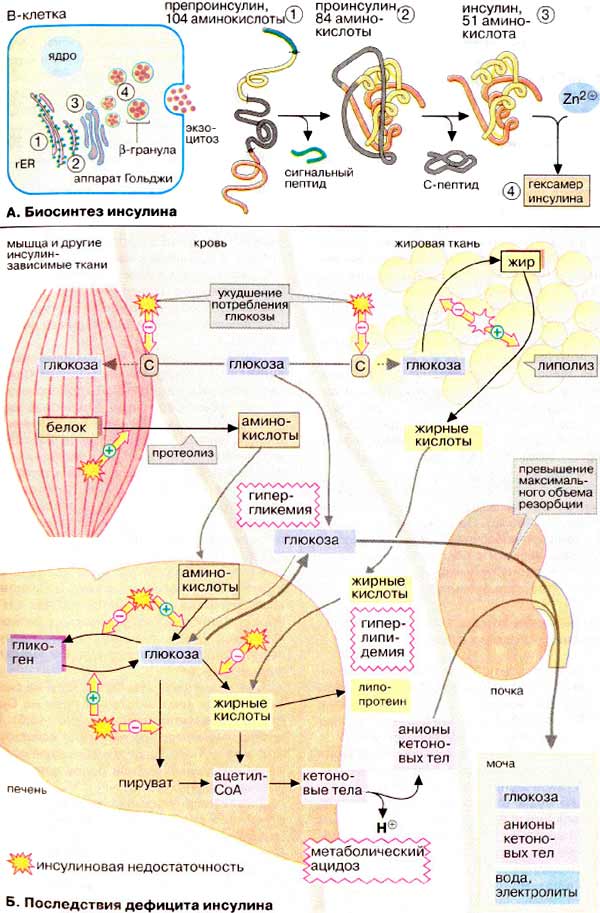
А. Биосинтез инсулина
Инсулин синтезируется в β-клетках островков Лангерганса поджелудочной железы. Как и многие секреторные белки, предшественник гормона (препроинсулин) содержит сигнальный пептид, который направляет пептидную цепь внутрь эндоплазматического ретикулума (см. с. 226), где после отщепления сигнального пептида и замыкания дисульфидных мостиков образуется проинсулин. Последний поступает в аппарат Гольджи и депонируется в клеточных везикулах, β-гранулах. В этих гранулах путем отщепления С-пептида образуется зрелый инсулин, который сохраняется в форме цинксодержащего гексамера (см. с. 82) вплоть до секреции.
Б. Последствия дефицита инсулина
Воздействие инсулина на обмен углеводов рассмотрено на с. 160. Его механизм сводится к усилению утилизации глюкозы и подавлению ее синтеза de novo. К этому следует добавить, что транспорт глюкозы из крови в большинство тканей также является инсулинзависимым процессом (исключения составляют печень, центральная нервная система и эритроциты).
Инсулин влияет также на липидный обмен в жировой ткани: он стимулирует синтез жирных кислот из глюкозы, что связано с активацией ацетил-КоА-карбоксилазы (см. с. 164), и усиливает генерацию НАДФН + Н+ в ГМП (см. с. 154). Другая функция инсулина – торможение расщепления жиров и деградации белков в мышцах. Таким образом, недостаточность инсулина ведет к глубоким нарушениям промежуточного метаболизма, что и наблюдается у больных сахарным диабетом.
Характерный симптом заболевания – повышение концентрации глюкозы в крови с 5 мМ (90 мг/дл) до 9 мМ (160 мг/дл) и выше (гипергликемия, повышенный уровень глюкозы в крови). В мышцах и жировой ткани, двух наиболее важных потребителях глюкозы, нарушаются усвоение и утилизация глюкозы. Печень также утрачивает способность использовать глюкозу крови. Одновременно повышается глюконеогенез и вместе с тем усиливается протеолиз в мышцах. Это еще более увеличивает уровень глюкозы в крови. Нарушение реабсорбции глюкозы в почках (при концентрации в плазме 9 мМ и выше), приводит к ее выведению с мочой (глюкозурия).
Особенно серьезные последствия имеет повышенная деградация жиров. Накапливающиеся в больших количествах жирные кислоты частично используются в печени в синтезе липопротеинов (гиперлипидемия), остальные распадаются до ацетил-КоА. Избыточные количества ацетил-КоА, возникающие в результате неспособности цитратного цикла полностью его утилизировать, превращаются в кетоновые тела (см. с. 304). Кетоновые тела – ацетоуксусная и 3-гидроксимасляная кислоты – повышают концентрацию протонов и влияют на физиологическую величину рН. Вследствие этого может возникать тяжелый метаболический ацидоз (диабетическая кома, см. с. 280). Образующийся ацетон придает дыханию больных характерный запах. Кроме того, в моче увеличивается содержание анионов кетоновых тел (кетонурия).
При неадекватном лечении сахарный диабет может приводить к долгосрочным осложнениям: изменению состояния кровеносных сосудов (диабетические ангиопатии), повреждению почек (нефропатии), нервной системы и глаз, например хрусталика (катаракта).
При некоторых состояниях можно наблюдать повышение содержания глюкозы в крови – гипергликемию, а также понижение концентрации глюкозы – гипогликемию. Гипергликемия является довольно частым симптомом различных заболеваний, прежде всего связанных с поражением эндокринной системы.
Сахарный диабет. В регуляции гликолиза и глюконеогенеза большую роль играет инсулин. При недостаточности содержания инсулина возникает заболевание, которое носит название «сахарный диабет»: повышается концентрация глюкозы в крови (гипергликемия), появляется глюкоза в моче (глюкозурия) и уменьшается содержание гликогена в печени. Мышечная ткань при этом утрачивает способность утилизировать глюкозу крови. В печени при общем снижении интенсивности биосинтетических процессов: биосинтеза белков, синтеза жирных кислот из продуктов распада глюкозы – наблюдается усиленный синтез ферментов глюконеогенеза. При введении инсулина больным диабетом происходит коррекция метаболических сдвигов: нормализуется проницаемость мембран мышечных клеток для глюкозы, восстанавливается соотношение между гликолизом и глюко-неогенезом. Инсулин контролирует эти процессы на генетическом уровне как индуктор синтеза ключевых ферментов гликолиза: гексокиназы, фос-фофруктокиназы и пируваткиназы. Инсулин также индуцирует синтез гли-когенсинтазы. Одновременно инсулин действует как репрессор синтеза ключевых ферментов глюконеогенеза. Следует отметить, что индукторами синтеза ферментов глюконеогенеза служат глюкокортикоиды. В связи с этим при инсулярной недостаточности и сохранении или даже повышении секреции кортикостероидов (в частности, при диабете) устранение влияния инсулина приводит к резкому повышению синтеза и концентрации ферментов глюконеогенеза, особенно фосфоенолпируват-карбоксикиназы, определяющей возможность и скорость глюконеогенеза в печени и почках.
Развитие гипергликемии при диабете можно рассматривать также как результат возбуждения метаболических центров в ЦНС импульсами с хе-морецепторов клеток, испытывающих энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда тканей. Роль системы фруктозо-2,6-бисфосфата в регуляции метаболизма углеводов, а также нарушения ее функционирования при сахарном диабете см. главу 16.
Гипергликемия может возникнуть не только при заболевании поджелудочной железы, но и в результате расстройства функции других эндокринных желез, участвующих в регуляции углеводного обмена. Так, гипергликемия может наблюдаться при гипофизарных заболеваниях, опухолях коркового вещества надпочечников, гиперфункции щитовидной железы. Иногда гипергликемия появляется во время беременности. Наконец, гипергликемия возможна при органических поражениях ЦНС, расстройствах мозгового кровообращения, болезнях печени воспалительного или дегенеративного характера. Поддержание постоянства уровня глюкозы в крови, как отмечалось,- важнейшая функция печени, резервные возможности которой в этом отношении весьма велики. Поэтому гипергликемия, обусловленная нарушением функции печени, выявляется обычно при тяжелых ее поражениях.
Большой клинический интерес представляет изучение реактивности организма на сахарную нагрузку у здорового и больного человека. В связи с этим в клинике довольно часто исследуют изменения во времени уровня глюкозы в крови, обычно после приема per os 50 г или 100 г глюкозы, растворенной в теплой воде,- так называемая сахарная нагрузка. При оценке построенных гликемических кривых обращают внимание на время максимального подъема, высоту этого подъема и время возврата концентрации глюкозы к исходному уровню. Для оценки гликемических кривых введено несколько показателей, из которых наиболее важное значение имеет коэффициент Бодуэна:
где А – уровень глюкозы в крови натощак; В – максимальное содержание глюкозы в крови после нагрузки глюкозой. В норме этот коэффициент составляет около 50%. Значения, превышающие 80%, свидетельствуют о серьезном нарушении обмена углеводов.
Гипогликемия. Нередко гипогликемия связана с понижением функций тех эндокринных желез, повышение функций которых приводит, как отмечалось, к гипергликемии. В частности, гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой болезни, гипотиреозе. Резкое снижение уровня глюкозы в крови отмечается при аденомах поджелудочной железы вследствие повышенной продукции инсулина β-клетками панкреатических островков. Кроме того, гипогликемия может быть вызвана голоданием, продолжительной физической работой, приемом β-ганглиоблока-торов. Низкий уровень глюкозы в крови иногда отмечается при беременности, лактации.
Гипогликемия может возникнуть при введении больным сахарным диабетом больших доз инсулина. Как правило, она сопровождает почечную глюкозурию, возникающую вследствие снижения «почечного порога» для глюкозы.
Глюкозурия. Обычно присутствие глюкозы в моче (глюкозурия) является результатом нарушения углеводного обмена вследствие патологических изменений в поджелудочной железе (сахарный диабет, острый панкреатит и т.д.). Реже встречается глюкозурия почечного происхождения, связанная с недостаточностью резорбции глюкозы в почечных канальцах. Как временное явление глюкозурия может возникнуть при некоторых острых инфекционных и нервных заболеваниях, после приступов эпилепсии, сотрясения мозга.
Отравления морфином, стрихнином, хлороформом, фосфором также обычно сопровождаются глюкозурией. Наконец, необходимо помнить о глюкозурии алиментарного происхождения, глюкозурии беременных и глюкозурии при нервных стрессовых состояниях (эмоциональная глюкозурия).

Изменение углеводного обмена при гипоксических состояниях. Отставание скорости окисления пирувата от интенсивности гликолиза наблюдается чаще всего при гипоксических состояниях, обусловленных различными нарушениями кровообращения или дыхания, высотной болезнью, анемией, понижением активности системы тканевых окислительных ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозах, а также в результате относительной гипоксии при чрезмерной мышечной работе.
При усилении гликолиза происходит накопление пирувата и лактата в крови, что сопровождается обычно изменением кислотно-основного равновесия, уменьшением щелочных резервов крови. Увеличение содержания лактата и пирувата в крови может наблюдаться также при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т.п.) в результате торможения процессов глюконеогенеза в печени.
Гликогенозы. Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с дефицитом или полным отсутствием ферментов, катализирующих процессы распада или синтеза гликогена, и характеризуются избыточным его накоплением в различных органах и тканях (табл. 10.2).
Гликогеноз I типа (болезнь Гирке) встречается наиболее часто, обусловлен наследственным дефектом синтеза фермента глюкозо-6-фосфатазы в печени и почках. Болезнь наследуется по аутосомно-рецессивному типу. Патологические симптомы появляются уже на первом году жизни ребенка: увеличена печень, нередко увеличены почки. В результате гипогликемии появляются судороги, задержка роста, возможен ацидоз. В крови – повышенное количество лактата и пирувата. Введение адреналина или глюка-гона вызывает значительную гиперлактатацидемию, но не гипергликемию, так как глюкозо-6-фосфатаза в печени отсутствует и образования свободной глюкозы не происходит.
