Диабет 1 прорыв в лечении
Главная » 1-med-fact, лучшее, самое-самое
⇐ ⇒
Сахарный диабет — одна из самых прогрессирующих болезней человечества. Введение инсулина для человека с сахарным диабетом 1 типа пока ничем не заменимая процедура. Но благодаря новым методам лечения, возможно, в скором времени удастся освободить людей из плена этой тяжелой болезни.
Новейшие исследования показали, что введение минимального числа заключенных в микрокапсулы клеток поджелудочной железы нормализовало уровень глюкозы в крови подопытных животных на 17 недель и более. Сахарный диабет без инсулина (без его самостоятельного введения) становится достижимой реальностью.
Число людей, живущих с сахарным диабетом, уже 425 миллионов. К 2045 году таких людей в мире станет более 630 миллионов.
Если человек с сахарным диабетом не борется с ним — не следит за состоянием уровня глюкозы в крови, не соблюдает диету и норму физической нагрузки, не использует необходимые лекарства, а при необходимости — инсулин, то его ждут крайне тяжелые осложнения, лишение нормального образа жизни и ранняя смерть.
Наиболее тяжелая форма болезни — сахарный диабет 1 типа. В этом случае у человека погибают бета-клетки в его поджелудочной железе и его организм теряет возможность производить собственный гормон инсулин. Без инсулина клетки организма не в состоянии нормально существовать, в частности, получать глюкозу из крови — в результате человек погибает.
Сахарный диабет I типа составляет до 10% всех случаев диабета.
Среди детей наиболее распространенным является именно сахарный диабет 1 типа. Всего на данный момент им страдают более 1 миллиона детей по всему миру.
Единственным опробованным, массовым и надежным способом жизни с сахарным диабетом 1 типа на сегодняшний день является инсулинотерапия. Только постоянный мониторинг уровня сахара в крови (с помощью глюкометра или систем постоянного мониторинга, вроде Freestyle Libre или Dexcom ), постоянные инъекции инсулина с помощью шприц-ручек или инсулиновых помп и учет съеденного — дают шанс человеку на полноценную жизнь.
Если человек с сахарным диабетом успешно осуществляет самоконтроль и ему удается проводить успешную инсулинотерапию, то его качество жизни ничем не отличается от обычной, и он сможет реализоваться наравне со всеми — чему свидетельствуют многие очень успешные люди — политики, ученые, спортсмены и актеры с сахарным диабетом.
.
Однако инсулинотерапия не восстанавливает физиологическую саморегуляцию, требует постоянных усилий со стороны человека и его близких и сохраняет постоянный риск опасных состояний — гипогликемии и сопутствующих сахарному диабету осложнений.
Уже несколько десятилетий ведется поиск альтернативных решений проблемы сахарного диабета 1 типа. Одно из них — создание «искусственной поджелудочной железы», которая самостоятельно контролирует уровень сахара в крови и вводит необходимые дозы инсулина (1,2).
Второй путь — пересадка донорской поджелудочной железы или её фрагментов; пересадка островков поджелудочной железы (с бета-клетками) от человека или животных а также попытки искусственного выращивания инсулин-продуцирующих клеток из стволовых клеток для их последующего ввода в организм.
Но этот путь до сих пор сталкивался с существенными сложностями. Пересадки от человека — из-за крайне малого числа донорского материала по сравнению с требуемым, высокой стоимости и большого числа иммунных реакций организма на пересажанный материал.
Пересадки островков поджелудочной железы от животных также сталкиваются с большим числом трудностей. Главные из которых: нефункционирование должным образом пересаженных клеток, иммунный ответ организма и опасность заражения человека (и человеческой популяции в целом) болезнями животных-доноров.
В частности, чтобы сохранить эффективность пересаженных клеток, человеку приходится принимать сильные иммуннодепрессанты, тем самым существенно снижая собственную защитную систему и подвергая свою жизнь большому риску.
Крайне недостаточное число материала для пересадки от человека (донорами могут быть только погибшие люди) и серьезная (к счастью, пока гипотетическая) опасность заразить человечество зооинфекцией в случае пересадки клеток от животных стимулируют разработку технологий создания тканеинженерных конструкций, замещающих работу островков поджелудочной железы. Клетки, которые должны выполнять функцию погибших бета-клеток человека, либо выделяются из донорского материала, либо выращиваются из различного типа стволовых клеток и «закрепляются» в специальных биокаркасах.
К сожалению, попытки выращивания работающих островковых клеток из различного типа стволовых клеток пока не привели к тому уровню успешности, когда полученные клетки можно было бы использовать для лечения сахарного диабета. Биоинженерные же работы с клетками доноров вполне успешны.
Например, решением части проблем клеточной трансплантации является технология заключения островков поджелудочной железы в микрокапсулы, которые и вводятся больному сахарным диабетом 1 типа. Технология микрокапсулирования помогает изолировать клетки островков поджелудочной железы доноров от иммунной системы пациента. При этом сами клетки должны как можно дольше сохранять жизнедеятельность (осуществлять свободный обмен питательными веществами и кислородом) и эффективно выполнять свою основную функцию — производить инсулин в ответ на повышение уровня глюкозы в крови.
Современные технологии позволяют производить такие микрокапсулы из биосовместимых и нетоксичных материалов. Различные группы ученых во многих странах пытаются усовершенствовать данный метод.
Одна из недавно решенных задач – это уменьшение числа вводимых микрокапсул. Дело в том, что ранее, в процессе микрокапсулирования островков поджелудочной железы, большая часть микрокапсул оставалась пустыми. Из-за этого значительно увеличился объем имплантируемого материала, что сильно увеличивало иммунную реакцию после имплантации.
Для разделения микрокапсул использовались магнитные наночастицы и созданный с помощью 3D-печати чип с микроканалами, который и разделял полученные ранее микрокапсулы на пустые и те, в которых находились островки поджелудочной железы. В результате общий объем имплантата снизился почти на 80%.
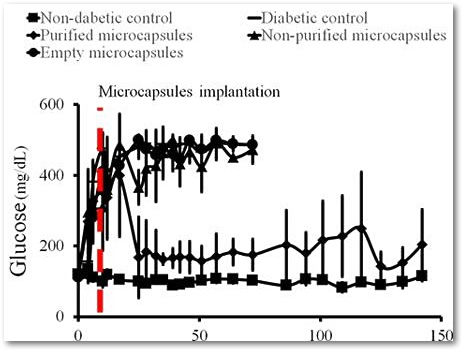
Очищенные имплантаты вводились подкожно крысам с сахарным диабетом 1 типа — в результате в течение более 17 недель уровень глюкозы в крови животных восстанавливался до нормогликемии (<200 мг / дл).
Уровень глюкозы в крови у подопытных крыс. Вверху: графики животных с введенными пустыми микрокапсулами (большие точки); с несортированными микрокапсулами (треугольники). Внизу: график животных с отобранными микрокапсулами (маленькие точки) и контрольный график уровня глюкозы у животных без сахарного диабета (квадраты).
Этот и подобные эксперименты дарят надежду миллионам больным сахарным диабетом на то, что в скором времени удастся совершить прорыв лечении одной из самых массовых болезней человечества.
Пока же больные сахарным диабетом 1 типа должны особо тщательно соблюдать процедуры инсулинотерапии, чтобы сохранить своё здоровье до массового внедрения новых технологий.
Поделиться информацией из статьи:
.
ТЕМЫ: Биология Здоровье Медицина Человек Болезни Диета Продолжительность жизни Сахарный диабет
ЧИТАЙТЕ ТАКЖЕ:
Ученые Гарвардского университета сообщили о том, что им удалось разработать способ массового получения в лабораторных условиях нормально функционирующих, зрелых, вырабатывающих инсулин бета-клеток поджелудочной железы. Авторы метода утверждают, что теперь человечество находится в шаге от реализации мечты миллионов больных и их близких – полному излечению от диабета 1 типа.
В пятницу стало известно о прорыве в поиске эффективных методов лечения диабета 1 типа. Ученые Гарвардского университета сообщили о том, что им удалось разработать способ массового получения в лабораторных условиях из столовых клеток нормально функционирующих, зрелых, вырабатывающих инсулин бета-клеток поджелудочной железы. Причем в количествах, достаточных для трансплантации пациентам, чьи бета-клетки убиты собственной иммунной системой.
Авторы метода утверждают, что теперь человечество находится буквально в шаге от реализации мечты миллионов больных и их близких – полному излечению от диабета 1 типа. Среди них – и ведущий автор опубликованной в журнале Cell работы, биолог, специалист по стволовым клеткам Дуглас Мелтон (Douglas Melton). После того, как около 20 лет тому назад его маленькому сыну, а позже и дочери, был поставлен диагноз «диабет 1 типа», ученый посвятил свою жизнь и научную карьеру поиску средств лечения и уверен, что добился своего.
{#vrez.58707}
Клетки на замену
Как известно, поджелудочная железа в течение дня регулирует уровень глюкозы в крови с помощью секреции бета-клетками, расположенными в так называемых островках Лангерганса, гормона инсулина. При сахарном диабете 1 типа клетки собственной иммунной системы организма, по невыясненным пока причинам, проникают в островки Лангерганса и уничтожают бета-клетки. Недостаток инсулина приводит к таким тяжелым последствиям, как нарушение сердечной функции, потеря зрения, инсульт, почечная недостаточность и другим. Больным приходится пожизненно несколько раз в день делать себе инъекции подобранных доз инсулина, однако абсолютно точного соответствия естественному процессу выброса гормона в кровь добиться все же невозможно.
Ученые всего мира уже в течение десятилетий ищут способы замены утраченных из-за аутоиммунного процесса бета-клеток. В частности, был разработан метод трансплантации инсулоцитов (клеток островков Лангерганса), выделенных из донорских поджелудочных желез. Однако этот метод остается экспериментальным, доступным из-за нехватки донорских органов лишь небольшому числу пациентов. Кроме того, трансплантация донорских клеток, для предотвращения их отторжения, требует постоянного приема мощных иммуноподавляющих препаратов со всеми сопутствующими негативными побочными эффектами.
После изоляции в 1998 году эмбриональных стволовых клеток, потенциально способных превращаться в любые клетки организма, целью многих научных групп стали поиски методов получения функционирующих бета-клеток именно из них. Нескольким командам удалось in vitro (вне живого организма) трансформировать эмбриональные клетки в клетки-предшественники (прекурсоры) инсулоцитов, которые затем дозревают, будучи помещенными в организмы специально выведенной линии лабораторных животных и начинают вырабатывать инсулин. Процесс созревания занимает около шести недель.
В частности, такого успеха добились специалисты из Калифорнийского университета (Сан-Диего). 9 сентября они, совместно с местной биотехнологической компанией ViaCyte, объявили о начале первых в своем роде клинических испытаний экспериментального препарата VC-01, представляющего собой выращенные из эмбриональных стволовых клеток прекурсоры бета-клеток, помещенные в полупроницаемую оболочку. Предполагается, что первая фаза испытаний, призванная оценить эффективность, переносимость и безопасность различных доз препарата, продлится два года, в ней примут участие примерно 40 пациентов. Исследователи ожидают, что многообещающие результаты, полученные в ходе экспериментов на животных, удастся повторить на людях и имплантированные под кожу прекурсоры бета-клеток созреют и начнут производить нужное организму количество инсулина, что позволит пациентам отказаться от инъекций.
Помимо эмбриональных стволовых клеток, источником для получения инсулоцитов могут быть и индуцированные плюрипотентные стволовые клетки (iPSC) – незрелые клетки, перепрограммированные из зрелых и потенциально способные специализироваться в клетки всех типов, присутствующих во взрослом организме. Однако эксперименты показали, что этот процесс очень сложен и долог, а получающиеся бета-клетки лишены многих характеристик «родных» клеток.
Поллитра бета-клеток
Тем временем группа Мелтона заявила, что разработала метод, позволяющий избежать всех недостатков – источником инсулоцитов могут быть как эмбриональные стволовые клетки, так и iPSC, весь процесс происходит in vitro, а на выходе уже через 35 дней получается полулитровый сосуд с 200 миллионами зрелых, нормально функционирующих бета-клеток, что, теоретически, достаточно для трансплантации одному пациенту. Сам Мелтон назвал получившийся протокол «воспроизводимым, но очень кропотливым». «Никакого волшебства, только десятилетия упорной работы», – цитирует его журнал Science. Протокол включает поэтапное введение в очень точно подобранной комбинации пяти различных факторов роста и 11 молекулярных факторов.
{#vrez.58708}
Пока метод Мелтона показал отличные результаты в экспериментах на мышиной модели диабета 1 типа. Через две недели после трансплантации в организм больных диабетом мышей, полученные из стволовых клеток человеческие бета-клетки поджелудочной железы начали вырабатывать достаточное количество инсулина для того, чтобы вылечить животных.
Однако, прежде, чем перейти к испытаниям на людях, Мелтону и его коллегам необходимо решить еще одну проблему – как защитить трансплантат от атаки иммунной системы. Тот же самый аутоиммунный процесс, ставший причиной болезни, может затронуть новые бета-клетки, полученные из собственных iPSC пациента, а инсулоциты, полученные из эмбриональных стволовых клеток, могут стать мишенью для нормального иммунного ответа, как чужеродные агенты. В настоящее время группа Мелтона в сотрудничестве с другими научными центрами работает над тем, как наиболее эффективно решить эту проблему. Среди вариантов – помещение новых бета-клеток в некую защитную оболочку либо их модификация с тем, чтобы они могли не поддаваться атаке иммунных клеток.
Мелтон не сомневается, что эта трудность будет преодолена. По его мнению, клинические испытания его метода начнутся в течение ближайших нескольких лет. «Нам сейчас остается всего один шаг до финиша», – считает он.
Сахарный диабет – заболевание, приводящее к пожизненным инъекциям инсулина, инвалидности и фатальным осложнениям. Ученые из Приволжского исследовательского медицинского университета (ПИМУ) приступили к разработке принципиально нового метода лечения этого недуга.
Чтобы понять механизм технологии, нужно сказать о том, как работает поджелудочная железа, отчего возникает диабет. В этом органе есть так называемые бета-клетки, объединенные в островки, которые автоматически продуцируют инсулин в ответ на повышение уровня глюкозы в крови. При ряде аутоиммунных или хронических болезней общая их масса снижается, появляются функциональные нарушения в виде недостаточной выработки инсулина. Результат – повышение уровня глюкозы в сыворотке крови.
– Это инсулинопотребный сахарный диабет. Он возникает, если число островков уменьшилось на 80 процентов, – рассказывает заведующий кафедрой факультетской хирургии и трансплантологии, главный внештатный трансплантолог минздрава Нижегородской области Владимир Загайнов.
Ученый подчеркивает, что метод лечения диабета только один – трансплантация поджелудочной железы. Потребность в этой операции в России удовлетворяется на тысячные доли процента, что связано с дефицитом донорских органов. Во всех остальных случаях речь идет о компенсации заболевания с помощью инсулина. Однако даже пересадка сопряжена с необходимостью иммуносупрессивной терапии, чтобы организм пациента не отторгал донорский орган. А у нее есть свои минусы, особенно в отдаленном периоде.
Главная идея проекта – пересадка не всей поджелудочной железы, а только островков, состоящих из тех самых бета-клеток.
– Островки будут выделяться из донорской железы специальным способом. Даже если целая железа не годится для трансплантации, из нее можно попытаться выделить островки и пересадить их, – поясняет Владимир Загайнов.
В мире эту идею пытаются реализовать разными способами и с разной степенью успешности. Введение островков от донора требует все той же небезопасной иммуносупрессивной терапии. В ПИМУ ученые разрабатывают вариант пересадки клеток, заключенных в специальные пористые капсулы. В теории клетки приживаются и начинают вырабатывать инсулин. Человек излечивается от диабета. А поры капсулы достаточно малы, чтобы предотвратить атаку иммунных клеток организма, поэтому никакой иммуносупрессивной терапии не требуется. Важно, что речь идет о малоинвазивных операциях, а не о сложной трансплантации. Возможных вариантов несколько: введение в брюшную полость путем пункции либо введение в печень по воротной вене.
Первые эксперименты ученых из НИИ экспериментальной онкологии и биомедицинских технологий ПИМУ вместе с Институтом металлоорганической химии РАН оказались успешными.
– В отдаленной перспективе планируем проработать выращивание бета-клеток из стволовых, – говорит Владимир Загайнов. – Параллельно вместе с коллегами из Национального медицинского исследовательского центра трансплантологии и искусственных органов имени Шумакова занимаемся легитимизацией технологии. Раньше в России за это никто не брался, поэтому трансплантация островков бета-клеток поджелудочной пока не вошла в список разрешенных, хотя в мире это уже существует. Надеемся, что в ближайшее время вопрос будет решен.
Планируем проработать выращивание бета-клеток из стволовых
В 2022 году проект, выполняемый по госзаданию Минздрава России, завершится. Можно будет испытывать метод на животных, а затем заниматься регистрацией. На мой вопрос, когда лечение будет доступно российским пациентам, профессор Загайнов ответил кратко:
– Деклараций в жизни хватает, давайте заниматься делом.
Комментарий
Ольга Занозина, доктор медицинских наук, заведующая отделением эндокринологии Нижегородской областной больницы имени Семашко:
– Наряду с совершенствованием самих инсулинов, способов их введения в организм пациента, улучшением терапевтического обучения больных сахарным диабетом развивается и другое направление – трансплантационные технологии, позволяющие вводить бета-клетки островков поджелудочной железы, которые вырабатывают инсулин, в организм больного человека.
Положительный эффект достигается при виртуозном заборе, хранении и введении островковых клеток больному человеку. При успешном результате – почти полный контроль за гликемией, отсутствие гипогликемий и потребности в экзогенном инсулине. Вся эта работа требует ювелирного мастерства.
