Диабет новости в излечении 1 типа
Сахарный диабет первого типа, который обычно развивается у детей и подростков, является хроническим заболеванием. Последние два года в Израиле и других странах ведутся интенсивные исследования этого заболевания, результаты которых заставляют ученых полностью пересмотреть традиционный подход к лечению сахарного диабета.
Считается, что сахарный диабет первого типа является аутоиммунным заболеванием, при котором происходит разрушение бета-клеток поджелудочной железы, ответственных за выработку инсулина – гормона, с помощью которого сахар (глюкоза) проникает в клетки организма. При разрушении бета-клеток количество выделяемого инсулина уменьшается и уровень сахара в крови повышается, что приводит к поражению кровеносных сосудов и другим пагубным последствиям для организма.
Несмотря на долгие годы исследований, ученые пока что не могут объяснить, почему организм разрушает собственные бета-клетки. Одна из теорий гласит, что причиной является вирусное заражение, при котором на молекулярном уровне вирусы похожи на бета-клетки, таким образом защитная реакция организма может быть ошибочно направлена на данный вид клеток. Согласно другой теории, причиной аутоиммунной атаки организма является излишняя стерильность, в которой растут дети, что приводит к повышенной чувствительности иммунной системы к собственным бета-клеткам поджелудочной железы.

Классическая модель развития сахарного диабета первого типа
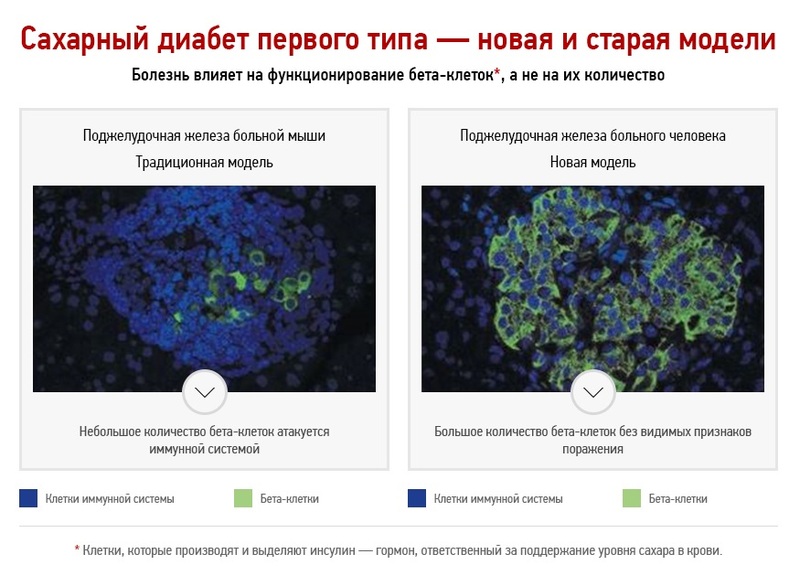
Принятая на сегодня теория развития сахарного диабета первого типа гласит, что первая стадия заболевания продолжается от нескольких месяцев до нескольких лет, в течение которых происходит постепенное разрушение бета-клеток поджелудочной железы. Заболевание не диагностируется на начальной стадии, потому что оставшиеся клетки начинают выделять больше инсулина, чтобы скомпенсировать его недостаток в крови. Сахарный диабет первого типа диагностируется, когда остается только 10 % бета-клеток, уже не способных выделять достаточно инсулина для поддержания требуемого уровня сахара в крови. На этом этапе пациент получает лечение – иньекции инсулина, параллельно с этим происходит полное уничтожение организмом оставшихся бета-клеток. Так как разрушение бета-клеток является необратимым процессом, пациент вынужден получать лечение на протяжении всей жизни.
Данная модель на протяжении многих лет оказывала огромное влияние на исследование сахарного диабета первого типа. Основным предположением было то, что на момент диагностики у пациента практически не остается бета-клеток поджелудочной железы. Старая модель основывалась на исследованиях, проведенных на одном виде мышей, развивающих болезнь, похожую на сахарный диабет первого типа у людей, а также на наблюдениях онкологических пациентов, у которых была удалена часть поджелудочной железы.
Новые исследования
В последние два года, благодаря значительным логическим усилиям, ученые получили возможность изучать десятки образцов тканей поджелудочной железы пациентов, страдающих сахарным диабетом первого типа, которые умерли незадолго после диагностики заболевания. Речь идет о редких и трагических случаях, когда пациенты (в основном дети) погибали при несчастных случаях, а семьи соглашались пожертвовать их органы для исследований.
Анализ образцов ткани этих пациентов показал неожиданные результаты. Оказалось, что в тканях поджелудочной железы имеется большое количество бета-клеток без видимых признаков поражения со стороны иммунной системы, а их количество значительно выше, чем 10 % здоровых клеток (согласно классической модели). Таким образом, ученые пришли к выводу, что на этапе диагностики сахарного диабета у человека имеется большое количество незатронутых иммунной системой бета-клеток.
Данное открытие проливает свет на известный в медицине эффект при начале лечения сахарного диабета первого типа с помощью инсулина, при котором в течение первых месяцев происходит временное «выздоровление», когда бета-клетки начинают вырабатывать инсулин в достаточном количестве. Классическая модель не может объяснить, каким образом такое небольшое количество бета-клеток выделяет достаточно инсулина. Новое исследование утверждает, что происходит функциональное поражение клеток, и при «разгрузке» с помощью инъекций инсулина их функции временно восстанавливаются, что было бы невозможно, если бы клетки были разрушены.
Важно отметить, что в организме происходит аутоиммунная реакция, направленная на разрушение бета-клеток поджелудочной железы. Однако, согласно новым исследованиям, происходит не уничтожение бета-клеток, а нарушение их функционирования, поэтому можно надеяться, что поражение такого рода может быть обратимым.
Какие последствия будет иметь данное открытие?
Теперь, когда известно, что на момент диагностики сахарного диабета первого типа имеется достаточно бета-клеток, пациент должен получать лекарства, нейтрализующие иммунную систему с целью предотвращения нарушения функционирования этих клеток. Разработка таких лекарств уже ведется. Другим направлением будут лекарства, которые смогут вернуть способность вырабатывать инсулин пораженным клеткам или обеспечить достаточную выработку инсулина оставшимися клетками. Ученые пока что далеки от создания подобных препаратов, но главное, что результаты последних исследований показали верный путь для лечения этого заболевания.
15190 просмотров
Источник
Сахарный диабет – заболевание, приводящее к пожизненным инъекциям инсулина, инвалидности и фатальным осложнениям. Ученые из Приволжского исследовательского медицинского университета (ПИМУ) приступили к разработке принципиально нового метода лечения этого недуга.
Чтобы понять механизм технологии, нужно сказать о том, как работает поджелудочная железа, отчего возникает диабет. В этом органе есть так называемые бета-клетки, объединенные в островки, которые автоматически продуцируют инсулин в ответ на повышение уровня глюкозы в крови. При ряде аутоиммунных или хронических болезней общая их масса снижается, появляются функциональные нарушения в виде недостаточной выработки инсулина. Результат – повышение уровня глюкозы в сыворотке крови.
– Это инсулинопотребный сахарный диабет. Он возникает, если число островков уменьшилось на 80 процентов, – рассказывает заведующий кафедрой факультетской хирургии и трансплантологии, главный внештатный трансплантолог минздрава Нижегородской области Владимир Загайнов.
Ученый подчеркивает, что метод лечения диабета только один – трансплантация поджелудочной железы. Потребность в этой операции в России удовлетворяется на тысячные доли процента, что связано с дефицитом донорских органов. Во всех остальных случаях речь идет о компенсации заболевания с помощью инсулина. Однако даже пересадка сопряжена с необходимостью иммуносупрессивной терапии, чтобы организм пациента не отторгал донорский орган. А у нее есть свои минусы, особенно в отдаленном периоде.
Главная идея проекта – пересадка не всей поджелудочной железы, а только островков, состоящих из тех самых бета-клеток.
– Островки будут выделяться из донорской железы специальным способом. Даже если целая железа не годится для трансплантации, из нее можно попытаться выделить островки и пересадить их, – поясняет Владимир Загайнов.
В мире эту идею пытаются реализовать разными способами и с разной степенью успешности. Введение островков от донора требует все той же небезопасной иммуносупрессивной терапии. В ПИМУ ученые разрабатывают вариант пересадки клеток, заключенных в специальные пористые капсулы. В теории клетки приживаются и начинают вырабатывать инсулин. Человек излечивается от диабета. А поры капсулы достаточно малы, чтобы предотвратить атаку иммунных клеток организма, поэтому никакой иммуносупрессивной терапии не требуется. Важно, что речь идет о малоинвазивных операциях, а не о сложной трансплантации. Возможных вариантов несколько: введение в брюшную полость путем пункции либо введение в печень по воротной вене.
Первые эксперименты ученых из НИИ экспериментальной онкологии и биомедицинских технологий ПИМУ вместе с Институтом металлоорганической химии РАН оказались успешными.
– В отдаленной перспективе планируем проработать выращивание бета-клеток из стволовых, – говорит Владимир Загайнов. – Параллельно вместе с коллегами из Национального медицинского исследовательского центра трансплантологии и искусственных органов имени Шумакова занимаемся легитимизацией технологии. Раньше в России за это никто не брался, поэтому трансплантация островков бета-клеток поджелудочной пока не вошла в список разрешенных, хотя в мире это уже существует. Надеемся, что в ближайшее время вопрос будет решен.
Планируем проработать выращивание бета-клеток из стволовых
В 2022 году проект, выполняемый по госзаданию Минздрава России, завершится. Можно будет испытывать метод на животных, а затем заниматься регистрацией. На мой вопрос, когда лечение будет доступно российским пациентам, профессор Загайнов ответил кратко:
– Деклараций в жизни хватает, давайте заниматься делом.
Комментарий
Ольга Занозина, доктор медицинских наук, заведующая отделением эндокринологии Нижегородской областной больницы имени Семашко:
– Наряду с совершенствованием самих инсулинов, способов их введения в организм пациента, улучшением терапевтического обучения больных сахарным диабетом развивается и другое направление – трансплантационные технологии, позволяющие вводить бета-клетки островков поджелудочной железы, которые вырабатывают инсулин, в организм больного человека.
Положительный эффект достигается при виртуозном заборе, хранении и введении островковых клеток больному человеку. При успешном результате – почти полный контроль за гликемией, отсутствие гипогликемий и потребности в экзогенном инсулине. Вся эта работа требует ювелирного мастерства.
Источник
Коротко
- «Витиви терапьютикс» (vTv Therapeutics) доложила об успешности клинической проверки экспериментального препарата TTP399 в ходе терапии сахарного диабета 1-го типа. На фоне известий биржевые котировки фармкомпании прибавили 50%.
- TTP399 – пероральный низкомолекулярный селективный активатор глюкокиназы в печени, разрабатываемый в качестве добавочной терапии инсулинозависимого сахарного диабета 1-го типа. Глюкокиназа – один из основных регуляторов гомеостаза глюкозы, выступающая ее физиологическим датчиком. Этот фермент меняет свои конформационную структуру, активность и/или внутриклеточное расположение сообразно колебаниям концентрации глюкозы. Глюкокиназа характеризуется двумя свойствами, востребованными в задаче таргетного контроля уровня сахара в крови. Во-первых, экспрессия глюкокиназы в основном ограничена чувствительными к глюкозе тканями (гепатоциты печени и бета-клетки поджелудочной железы). Во-вторых, глюкокиназа способна модулировать изменения в метаболизме глюкозы в печени, тем самым регулируя баланс между поглощением глюкозы и синтезом гликогена, а также модулировать изменения в секреции инсулина бета-клетками.
- Активация глюкокиназы – новый терапевтический подход к сахарному диабету 1-го типа, полностью отличающийся от существующих, которые представлены фактически только инъекциями инсулина. Его привлекательность заключена в отсутствии рисков диабетического кетоацидоза и тяжелой гипогликемии.
Подробности
Первая часть клинических исследований Simplici-T1 (NCT03335371) фазы I/II (рандомизированные, двойные слепые, плацебо-контролируемые, многоцентровые) охватила взрослых пациентов (n=19) с сахарным диабетом 1-го типа, диагноз которого был поставлен до 40-летнего возраста и который требует терапии при помощи либо инсулиновой помпы, либо ежедневных доз инсулина. На протяжении 12 недель участники каждый день получали 800 мг TTP399 или плацебо – на фоне оптимизированной инсулинотерапии. Первичная конечная точка была установлена изменением уровня гликированного гемоглобина (HbA1c).
Назначение TTP399 обеспечило статистически значимый (p=0,03) выход к заявленному показателю эффективности экспериментального лечения: усредненное снижение HbA1c составило 0,6% против усредненного роста на 0,1% в группе плацебо – итоговая разница 0,7%.
Среди получавших TTP399 отмечена тенденция к уменьшению общей дозы ежедневного болюсного инсулина – на 11% относительно исходной (p=0,02), тогда как в контрольной группе она снизилась на относительных 3%.
Согласно системе непрерывного мониторинга глюкозы (CGM), применение TTP399 на приблизительно два часа относительно плацебо (p=0,03) улучшило тот объем времени, в течение которого уровень сахара в крови находился в целевых терапевтических пределах. Другими словами, засвидетельствован более стабильный контроль над глюкозой.
Для исключения вероятности того, что в ходе клинических исследований падение HbA1c было вызвано введением избыточного инсулина, был проведен дополнительный оценочный анализ – среди пациентов без доказательств несоблюдения предписанного лечения, которые не вводили повышенную дозу болюсного инсулина (на три и более единиц в сутки). Установлено, что в этой подгруппе испытуемых TTP399 статистически значимо (p=0,001) снизил уровень HbA1c на усредненных 0,21% против его роста на 0,11% в контрольной группе – итоговая разница 0,32%.
Вскоре будут готовы результаты второй части клинических испытаний Simplici-T1, вовлекших 85 пациентов с сахарным диабетом 1-го типа.
На второе полугодие запланирован запуск двух опорных 24-недельных клинических испытаний. Поскольку свободных финансовых средств у «Витиви» не так много, для завершения клинической программы TTP399 придется либо подключать сторонних партнеров, либо выдавать лицензию.
Есть мнение, что TTP399 без проблем получит регуляторное одобрение. Во-первых, профиль безопасности приемлем. Во-вторых, согласно требованиям Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), улучшение HbA1c хотя бы на скромных 0,3% уже считается клинически значимым.
Ранее «Витиви» протестировала пригодность TTP399 в терапии сахарного диабета 2-го типа – молекула работает. В 24-недельных клинических испытаниях AGATA (NCT02405260) фазы IIb (рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых) препарат-кандидат, назначаемый в ежедневной дозе 800 мг на фоне стабильной дозы метформина, вывел разницу с плацебо по части снижения HbA1c к усредненным 0,9% (p<0,01). Впрочем, дальнейшая разработка была прекращена ввиду чрезвычайной насыщенности лекарственного рынка для сахарного диабета 2-го типа, не оставляющей мелким фармигрокам никаких шансов на игру с ценообразованием.
Тем временем китайская «Хуа медсин» (Hua Medicine) отчиталась по результатам удачной позднестадийной проверки дорзаглиатина (dorzagliatin) – глюкокиназного активатора, ориентирующегося на терапию сахарного диабета 2-го типа. Дорзаглиатин, в отличие от TTP399, является двойным активатором глюкокиназы, таргетирующим ее как в печени, так и в поджелудочной железе.
Необходимость в подобных на TTP399 или дорзаглиатину лекарственных противодиабетических препаратах чрезвычайно высока, ведь большинство пациентов с сахарным диабетом не могут выйти к оптимальному контролю уровня глюкозы в крови (HbA1c ниже 7,0%).
Научный эксперт R&A-офиса Mosmedpreparaty.ru.
Дополнительная информация о Романе и его контактные данные доступны в разделе «Научно-исследовательский офис».
Навигация по записям
Источник
В основе обеих патологий, и рассеянного склероза и диабета 1-го типа, лежат аутоиммунные реакции: клетки собственной иммунной системы ополчаются в первом случае против миелиновой оболочки нервных волокон, а во втором – против вырабатывающих инсулин клеток бета-островков поджелудочной железы. Один из способов лечения аутоиммунных заболеваний, пока экспериментальный, состоит в том, чтобы «перезагрузить» иммунную систему. У пациента сначала забирают гемопоэтические (кроветворные) стволовые клетки, затем дают им цитостатики, препараты, нарушающие клеточное деление, с целью убить «сошедшие с ума» иммунные клетки. Затем вводят обратно в организм забранные заранее гемопоэтические стволовые клетки, способные заново воссоздать систему кроветворения, включая клетки иммунной системы. Процедура рискованная: ведь в период, когда «старая» иммунная система уже уничтожена, а «новая» еще не восстановилась, человек полностью беззащитен перед инфекциями. При этом, по словам ученых, такая методика вполне успешно используется при лечении лейкозов – онкологических заболеваний кроветворной системы.
Недавно сообщалось о завершении второй фазы клинических испытаний, в которых тестировали методику лечения рассеянного склероза с помощью «перезагрузки» иммунной системы. Сейчас закончилась (начаты оба исследования были в 2006 г.) вторая фаза испытаний аналогичной методики лечения сахарного диабета 1-го типа.
При диабете 1-го типа происходит аутоиммунное поражение бета-клеток островков Лангерганса поджелудочной железы, вырабатывающих пептидный гормон инсулин, который регулирует уровень глюкозы в крови. Такой тип диабета приводит к пожизненной зависимости от инъекций инсулина, при этом в любом случае развиваются осложнения: дисфункция почек и сердечно-сосудистой системы, поражение глаз, некротическое поражение тканей. В результате – существенное снижение качества жизни, а зачастую инвалидность и ранняя смерть.
При диабете 2-го типа бета-клетки вырабатывают инсулин, но ткани организма теряют к нему чувствительность. Этот тип сахарного диабета называют еще инсулинонезависимым, он, в отличие от диабета 1-го типа, развивается преимущественно в пожилом возрасте и характеризуется относительно легким течением.
В испытаниях принимал участие двадцать один пациент с сахарным диабетом 1-го типа. После «перезагрузки» иммунной системы бета-клетки поджелудочной железы перестали разрушаться и со временем восстановили продукцию инсулина. У большинства пациентов ремиссия оказалась длительной – в среднем 3,5 года, а один из них не принимает инсулин уже более восьми лет.
Однако такой продолжительный эффект наблюдался не у всех. У некоторых участников испытаний ремиссия длилась всего 6-7 месяцев. Это печально, но зато удалось выяснить, при каких исходных иммунологических параметрах пациента методика будет успешной, а при каких работу иммунной системы сбалансировать «перезагрузкой» не удастся. Ученые говорят об этом знании как о первом шаге к персонализированному подходу к лечению инсулинозависимого сахарного диабета.
Поскольку пересадка стволовых клеток связана с тяжелой иммуносупрессией, вряд ли этот способ лечения диабета станет массовым, но, тем не менее, в каких-то случаях он может быть хорошим вариантом для больного. Полученные в результате исследований знания помогут ученым в разработке других способов терапии этого заболевания.
Фото: https://commons.wiki.org
Подготовила Мария Перепечаева
Источник
