Интерлейкин 2 при сахарном диабете
-2010/52/1.png)

Интерлейкин-2 (ИЛ-2) – первый молекулярно-клонированный цитокин, представлялся как важнейший фактор роста Т-клеток, необходимый для их пролиферации и дифференцировки. Последующие исследования показали, что ИЛ-2 способствует генерации, выживаемости и функциональной активности регуляторных Т-клеток Foxp3+ (Treg или Т-супрессоры; Foxp3 – транскрипционный фактор, регулирующий транскрипцию генов, ответственных за дифференцировку Т-клеток и экспрессию цитокинов), и в его отсутствие наблюдается глубокий дефицит Т-супрессоров, приводящий к развитию аутоиммунных заболеваний. Таким образом, ИЛ-2 имеет двойные и противоположные функции: поддержание регуляторных Т-клеток и индукция эффекторных клеток, одновременный контроль и стимуляция иммунных реакций.
Самым ранним терапевтическим применением ИЛ-2 была стимуляция иммунного ответа у онкобольных. Не так давно появились терапевтические стратегии использования ИЛ-2, моноклональных антител к нему, или применения химических модификаций ИЛ-2 для увеличения числа и функции клеток Treg с целью лечения аутоиммунных заболеваний. Однако остается актуальной проблема одновременной генерации эффекторных клеток и клеток памяти, естественных киллеров и других лимфоидных популяций при использовании в лечении ИЛ-2.
История
Интерлейкин-2 (ИЛ-2) был выявлен как аутокринный фактор роста для культивируемых Т-клеток и был первым цитокином, клонированным в 1983 году. Вскоре была установлена его роль в стимуляции пролиферации Т-клеток и дифференцировке эффекторных и клеток памяти. Это подтолкнуло к клиническим испытаниям для оценки способности высоких доз ИЛ-2 стимулировать противоопухолевый иммунный ответ у пациентов с меланомой, раком почек и другими опухолями. Фактически, ИЛ-2 был первым биологическим продуктом, полученным с использованием технологии рекомбинантной ДНК, который был введен онкобольным и ВИЧ-инфицированным пациентам для стимуляции Т-клеток и, таким образом, заложил основу одной из великих революций биотехнологии и клинической медицины. Успех ИЛ-2 в качестве иммунотерапии опухолей был ограничен токсичностью, вызванной необходимостью введения высоких доз, проявляющейся как “цитокиновая буря” и синдром капиллярной утечки. Еще одним доказательством роли ИЛ-2 как важного фактора роста Т-клеток in vivo является использование моноклональных антител для подавления отторжения трансплантатов (таких как базиликсимаб, действующее вещество которого блокирует α-субъединицу ИЛ-2 рецепторного комплекса (IL-2Rα, который также известен как CD25 антиген) на поверхности Т-лимфоцитов).
В 1980-х и 1990-х годах в ходе некоторых наблюдений догма об основной роли ИЛ-2 лишь в качестве индуктора активации эффекторных клеток начала подвергаться сомнению. В ходе исследований было установлено быстрое возникновение аутоиммунных реакций на фоне блокирования ИЛ-2 или его рецептора CD25. Эти данные свидетельствовали о том, что значимая функция ИЛ-2 заключается в контроле иммунных реакций и поддержании иммунологической толерантности, а его отсутствие приводит к дефектному контролю эффекторных клеток, что приводит к аутоиммунной агрессии.
Функции и механизмы регуляции интерлейкина-2
ИЛ-2 необходим для выживания и реализации супрессивных функций регуляторных Т-клеток (которые определяются как CD4+, Foxp3+, CD25+, CD127), а отсутствие ИЛ-2 или нарушение его связи с рецептором проявляется численным и/или функциональным дефицитом регуляторных Т-клеток, что является причиной аутоиммунных реакций. Многие экспериментальные подходы показали, что этот цитокин имеет решающее значение для поддержания функционирования клеток Treg: в отсутствие ИЛ-2 T-супрессоры исчезают из периферических лимфоидных органов, по-видимому, потому, что дефицит этого фактора роста приводит к апоптотической гибели клеток.
Так же важна, как роль ИЛ-2 в выживании регуляторных Т-клеток, его необходимость для реализации функциональной мощности клеток Treg. Он необходим для экспрессии Foxp3 и других медиаторов Treg, подавляющих клеточную активность. Стабильная экспрессия Foxp3 реализуется за счет связи с его промотором ИЛ-2-индуцированного транскрипционного фактора 5. Ограниченная доступность ИЛ-2 в тканях, подвергшихся локальному воспалению, может привести к нестабильности клеток Treg, потере экспрессии Foxp3 и последующему производству патогенных цитокинов эффекторными клетками, которые могут усугубить аутоиммунизацию.
Поскольку зрелые клетки Treg не производят ИЛ-2, а он, предположительно, функционирует аутокринно, неизвестен был источник цитокина, который поддерживает на периферии регуляторные Т-клетки. Предполагалось, что стандартные (Foxp3-) Т-клетки продуцируют ИЛ-2, который затем действует на Т-супрессоры. Эта теория была подтверждена исследованиями, проведенными в условиях внутривидовой визуализации и показавшими, что регуляторные и стандартные Т-клетки локализуются вместе с антигенпредставляющими дендритными клетками, и в этих трехклеточных кластерах стандартные клетки реагируют на антиген путем секреции ИЛ-2, тогда как клетки Treg этот цитокин принимают.
Таким образом было установлено, что ИЛ-2 служит, по-видимому, обеим задачам: как стимуляции иммунного ответа, так и его контролю и сдерживанию (рис.1). Интересен вопрос о том, при каких обстоятельствах какая функция доминирует. Одно из предположений заключается в том, что доминирующая функция определяется количеством и кинетикой продукции ИЛ-2: индукция эффекторных клеток в ответ на кратковременное воздействие высоких доз цитокина и регуляторных клеток в ответ на стойкое содержание низкого уровня цитокинов. На активацию различных популяций Т-клеток также влияет кинетика экспрессии интерлейкиновых рецепторов. Рецептор поглощается клеткой после связывания с цитокином, а небольшой пул внутриклеточного IL-2Rβ стандартных CD4+ Т-клеток не позволяет им поддерживать их длительную экспрессию. Регуляторные Т-клетки, напротив, имеют крупные внутриклеточные пулы рецепторных цепей, благодаря чему способны осуществлять их экспрессию и в течение длительного времени могут представлять более устойчивое выделение ИЛ-2, чем другие популяции Т-клеток.
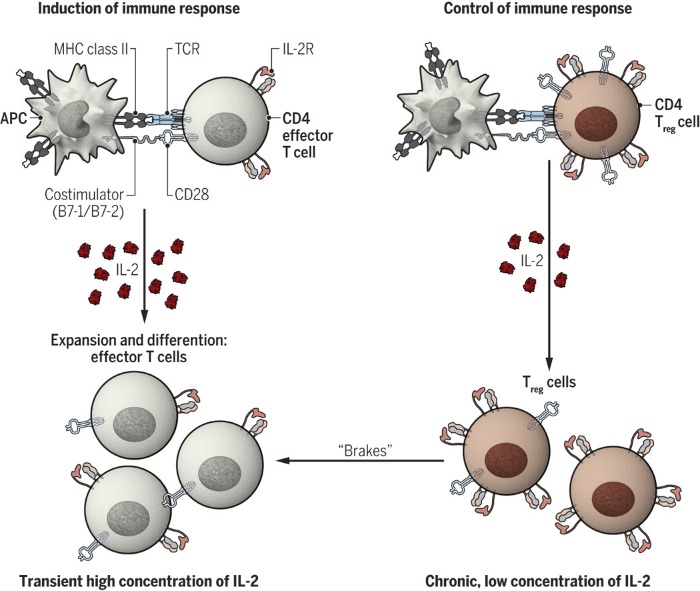
Рис. 1. Двойная роль ИЛ-2 в активации Т-клеток.
ИЛ-2 участвует в индукции иммунных реакций путем стимуляции пролиферации и дифференцировки «обычных» Т-клеток и контроля иммунных реакций за счет поддержания функции регуляторных Т-клеток. Эта двойственная активность, вероятно, различается по кинетике и количеству произведенного ИЛ-2.
MHC – основной комплекс гистосовместимости; TCR – рецептор Т-клеток; APC -антигенпредставляющая клетка.
Наконец, следует упомянуть, что ИЛ-2 осуществляет важные функции по отношению к другим клеткам лимфоидного ряда, включая NK-клетки и лимфоидные клетки врожденного иммунного ответа (рис.2). В одних случаях ИЛ-2 может увеличивать подмножество CD56+ NK-клеток, которые считаются популяцией подавляющей микроокружение опухолей, в других – способствует пролиферации лимфоидных клеток врожденного иммунного ответа (ILC2), способствующим продукции ИЛ-5, что, в свою очередь, приводит к эозинофилии и альтернативной активации макрофов. Кроме того, ИЛ-2 контролирует и другие содержащие CD25+ клетки, необходимые для поддержания тканевого гомеостаза.
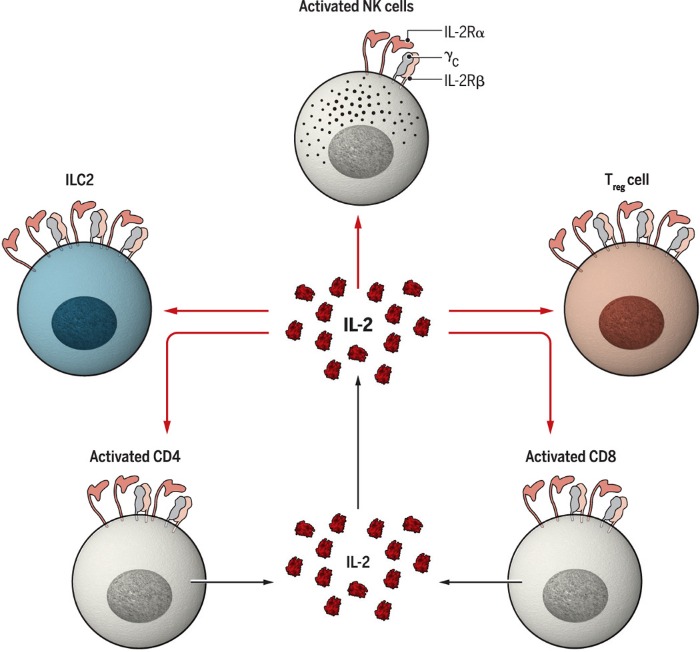
Рис. 2. Мишени действия ИЛ-2.
Помимо эффекторных и регуляторных Т-клеток, ИЛ-2 действует на NK-клетки и ILC. ILC2 – лимфоидные клетки врожденного иммунного ответа.
Генетические исследования ИЛ-2
Исследования в области генетики указывают на решающую роль нарушений регуляции ИЛ-2 как фактора риска аутоиммунных заболеваний. Редкие мутации, нарушающие аутокринный механизм регуляции ИЛ-2, могут вызывать тяжелые формы иммунной дисрегуляции. Дефицит IL2RA приводит к хроническому иммунодефициту и развитию IPEX-синдрома (иммуннодисрегуляция, полиэндокринопатия, энтеропатия и X-связанный синдром) – вариабельным аутоиммунным реакциям, развивающимся в первый год жизни и обусловленными мутацией транскрипционного активатора FOXP3. Мутации в транскрипционных факторах 5B, опосредующих сигналы ИЛ-2, также связаны с первичным иммунодефицитом и переменной аутоиммунизацией, что часто приводит к рецидивирующим инфекциям, экземе, хронической диарее и лимфоидной интерстициальной пневмонии. Варианты мутаций, также связанных с различными аутоиммунными заболеваниями, были обнаружены в генетических локусах, кодирующих ИЛ-2, его рецепторы, и связанные сигнальные факторы (включая 5A/5B и PTPN2).
В локусе гена IL2RA однонуклеотидные полиморфизмы (ОНП, SNP) влияют на уровни транскрипта IL2RA, растворимость рецептора IL-2RA, его экспрессию на специфические для него типы иммунных клеток и распространенность экспрессирующих IL-2RA Т-клеток в крови.
Недавно разработанное изящное картирование генов (fine mapping) указывает на потенциальные ОНП с улучшенным разрешением. В качестве значимого примера, в локусе IL-2RA был отображен один некодирующий вариант ОНП в первом интроне, ассоциированный с риском болезни Крона. Парадоксально, но тот же ОНП каким-то образом связан с защитой от сахарного диабета 1 типа, что согласуется с ситуационно ограниченными эффектами ИЛ-2, оказывающих диссонансное воздействие на два разных заболевания.
Регулярно сгруппированные короткие палиндромные повторы (CRISPR) продемонстрировали, что изящно картированный IL-2RA вариант с риском аутоиммунизации снижает время индукции IL-2RA в нативных Т-клетках при стимуляции. В будущем такие работы будут иметь потенциал в качестве открытия изменения в ответ на стимуляцию в индукции IL-2RA может изменять риск развития таких заболеваний, как болезнь Крона и сахарный диабет 1 типа. Селективная генная инженерия может быть использована для определения этих связанных с заболеванием вариантов, для оценки механистического воздействия на регуляцию IL-2RA и создания лекарственного средства будущего, работающего непосредственно в отношении затронутых клеточных реакций. Кроме того, CRISPR дает возможность «корректировать» серьезные мутации, которые нарушают сигнализацию IL-2 или переписывать последовательности кодирующих генов, контролирующих специфическую регуляцию сигнальных компонентов ИЛ-2 для генной инженерии в терапии будущего.
Структура ИЛ-2 и его рецептора
ИЛ-2 представляет собой типичный четырех-α-спиральный цитокин, который жестко регулируется на уровне мРНК с помощью сигналов от T-клеточного рецептора и CD28. ИЛ-2 связывается с клеткой через рецепторный комплекс, состоящий из трех субъединиц: IL-2Rα (CD25), IL-2Rβ (CD122) и общей γ-цепи (CD132). Высокое сродство тримерного комплекса IL-2/IL-2Rα/β указывает на его большую стабильность, чем ИЛ-2, связанный либо только с одной цепью α или β. Во время взаимодействия IL-2R тример IL-2/α/β принимает γ-цепь в четвертичный комплекс, что приводит к внутриклеточной передаче сигнала. Поскольку только часть остатка ИЛ-2 взаимодействуют как с цепями β, так и с γc, связывание ИЛ-2 может индуцировать конформационные изменения в β-цепи, что будет способствовать дальнейшему привлечению цепи γc. Для сигнализации необходимы цепочки β и γc, так как α-цепь не участвует в передаче сигналов. В отсутствие экспрессии IL-2Rα, IL-2Rβ и γc могут образовывать промежуточный аффинный рецептор, который полностью компетентен для сигнала. Структура ИЛ-2 и его рецептора является гибкой и может естественным образом существовать в разных конформациях, которые образуют либо высокоаффинный тримерный IL-2R, либо промежуточный аффинный димерный IL-2R, что приводит к активации иммунных клеток.
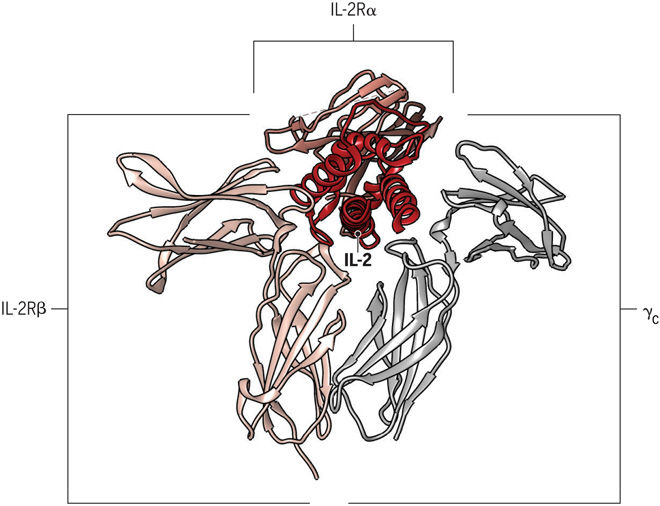
Рис. 3. Структура комплекса IL-2/IL-2R.
На диаграмме изображено, как цитокин взаимодействует с каждой из трех цепей рецептора.
Терапевтические возможности ИЛ-2
Выяснение роли ИЛ-2 для регуляторных Т-клеток предполагало возможность использования цитокина для борьбы с нежелательным иммунным ответом, а также в лечении аутоиммунных и воспалительных заболеваний. Задача использования ИЛ-2 для подавления патологических иммунных реакций заключается в том, что цитокин может активировать эффекторную ветвь клеток лимфоидного ряда, тем самым снижая риск обострения болезни. Разрабатывается несколько подходов для таргетирования ИЛ-2 на регуляторные клетки.
Низкодозированный ИЛ-2
Тримерный IL-2Rαβγc обычно экспрессируется в больших количествах клетками Treg, тогда как димерный IL-2Rβγc представляется в основном на активированных CD8+ Т-клетках и NK-клетках. В настоящее время установлено, что терапия низкими дозами ИЛ-2 предпочтительно активирует клетки Treg из-за свойственной им высокой экспрессии IL-2Rα. Первые клинические испытания показали, что низкодозированный ИЛ-2 эффективен при лечении васкулита, ассоциированного с вирусными гепатитами, и хронической реакции трансплантат против хозяина (GVHD). В дальнейшем испытания были проведены в терапии системной красной волчанки и сахарного диабета 1 типа. Результаты до сих пор являются многообещающими, а биологический агент уже одобрен для клинического применения. Однако терапевтическое окно для доз ИЛ-2 слишком мало, что накладывает сложности на применение такого лечения.
Конъюгаты антитело-цитокин
Другим подходом с изменением структуры ИЛ-2 является создание антител к нему, которые при образовании комплексов с цитокином могут стимулировать экспрессию регуляторных или эффекторных Т-клеток. Этот подход был предложен после обнаружения способности цитокина связываться с различными ИЛ-2-антителами, блокирующими на цитокине сайты для связи с β-цепью рецептора и индуцирующими аллостерический эффект, изменяющий связывание цепи IL-2Rα. Экспериментально разработаны ИЛ-2-антитела JES6-1, стерически блокирующие взаимодействие IL-2/IL-2Rβ и IL-2/IL-2Rγ, индуцируя предпочтительную активацию клеток IL-2Rα. Другие антитела к ИЛ-2, S4B6, напротив, изменяют его конформацию приводя к блокировке взаимодействия ИЛ-2/IL-2Rα и стабилизации взаимодействия IL-2/IL-2Rβ, приводящей к избирательному таргетированию эффекторных Т-клеток.
Эти результаты были воспроизведены путем разработки моноклональных антител к ИЛ-2, которые, связываясь цитокином, приводят к его конформационным изменениям, требующим как большей экспрессии CD25, так и меньшего порога для ускорения пролиферации, что реализует усиление активации и увеличение пула клеток Treg. Было показано, что эти антитела/комплексы ИЛ-2 эффективны в моделях таких аутоиммунных заболеваний, как сахарный диабет 1 типа и экспериментальный аутоиммунный энцефаломиелит, а также в модели РТПХ (реакция «трансплантат против хозяина»). Разработка таких препаратов для клинического применения может быть улучшена путем непосредственного связывания антитела с ИЛ-2, в результате чего образуется единый агент, который может увеличивать период полувыведения ИЛ-2 и в то же время ограничивать его нецелевую токсичность.
Химические модификации ИЛ-2
Некоторые усилия были приложены для модификации самого ИЛ-2 с целью улучшения его терапевтического потенциала. Shanafelt и др. генерировали мутеин ИЛ-2 с ~3000-кратной селективностью для Т-клеток, чем для NK-клеток in vitro в сравнении с натуральным цитокином и продемонстрировал его активность in vivo на животных моделях. В 2012 году лаборатория Garcia выпустила CD25-независимую версию ИЛ-2 с повышенной аффинностью связывания с IL-2Rβ, которая показала превосходное сродство с цитотоксическими клетками, что привело к улучшению противоопухолевого ответа. Несколько компаний, в том числе Celgene, Roche, Amgen и другие, разрабатывают новые ИЛ-2 мутеин, которые преимущественно вызывают прирост эффекторных или регуляторных Т-клеток. Эти аналоги ИЛ-2 действуют как частичные агонисты и по-разному влияют на те или иные популяции лимфоцитов.
Другие подходы к повышению эффективности ИЛ-2 состоят в соединении цитокина с крупными молекулами-переносчиками, такими как альбумин или полиэтиленгликоль (ПЭГ), или с генетическим слиянием ИЛ-2 с Fc (кристаллизующийся фрагмент) иммуноглобулина. В настоящее время ведется разработка ПЭГилированного ИЛ-2 от Nektar Therapeutics с пониженной аффинностью к тримерному IL-2R регуляторных Т-клеток, который в большей степени поддерживает цитотоксические CD8+ клетки, обеспечивая выраженную противоопухолевую активность.
Клеточная терапия ИЛ-2
Потенциал влияния ИЛ-2 на отдельные подтипы T-клеток или NK-клеток может быть использован для создания цитокиновой системы, в которой пара рецептор-лиганд ограничена исключительно совместным взаимодействием. Генно-инженерные Т-клетки могут экспрессировать мутантную версию IL-2Rβ, на которую будет избирательно влиять специфический мутантный ИЛ-2. Это повышает вероятность выборочного влияния на отдельные популяции Т-клеток и, следовательно, в перспективе может использоваться для лечения как аутоиммунных, так и онкозаболеваний.
Выводы
История ИЛ-2 дает замечательные уроки о том, как концепции полностью меняются в ходе тщательных научных изысканий. Долгие годы ИЛ-2 считался основным фактором роста Т-клеток и был вовлечен в инициирование иммунных реакций. Более свежие результаты от разнообразных экспериментальных подходов предполагают, что основная функция ИЛ-2 заключается в поддержании стабильной работы регуляторных T-клеток в лимфоидных органах и тканях. Эти новые разработки и пересмотр взгляда на биологию ИЛ-2 стали основой новых терапевтических стратегий, использующих этот цитокин для подавления, а не для стимуляции иммунных реакций. Конечно, многое еще предстоит изучить, чтобы реализовать весь его потенциал: следует учитывать способность ИЛ-2 воздействовать на различные популяции клеток, многие из которых могут способствовать воспалительным реакциям и, таким образом, служить риском развития аутоиммунных заболеваний. Достижение оптимального баланса между активацией эффекторных и регуляторных Т-клеток также остается постоянной проблемой в терапевтическом применении этого цитокина. Однако многие текущие клинические разработки должны решить эти проблемы в ближайшем будущем.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Введение
Актуальность профилактики хирургической инфекции определяется высокой частотой инфекционных осложнений послеоперационного периода. По данным Всемирной организации здравоохранения (ВОЗ), в 1995 г. у 30 % оперированных больных развивались осложнения, вызванные госпитальной инфекцией [1]. В настоящее время в хирургических стационарах г. Москвы гнойносептические осложнения составляют от 7,1 до 27,8 % (ГВМУ МО РФ, РАСХИ, 2004).
Традиционным и наиболее распространенным методом профилактики послеоперационной инфекции является предоперационное введение антибиотиков [2]. Эффективность антибиотикопрофилактики постепенно снижается изза увеличения антибиотикорезистентных штаммов патогенных микроорганизмов, увеличения доли больных преклонного возраста, пациентов с иммунодефицитом [3].
Среди причин развития инфекционных осложнений в послеоперационном периоде одно из главных мест занимает нарушение функционирования системы иммунитета [4]. Вторичный иммунодефицит также характерен для больных сахарным диабетом (СД). По этой причине сахарный диабет включен ВОЗ в классификацию болезней, приводящих к развитию вторичного иммунодефицита. Проблема актуальна тем, что количество больных СД в мире только на сегодняшний день составляет более 285 млн, а к 2025 г. их количество возрастет до 380 млн, что составит около 7,1 % от всего взрослого населения планеты. Увеличивающееся число больных, страдающих СД, и сопутствующая этому заболеванию иммуносупрессия обусловливают увеличение частоты послеоперационных инфекционных осложнений, несмотря на существующие меры антибиотикопрофилактики хирургических инфекций [5]. Несмотря на успехи современной эндокринологии и хирургии, число послеоперационных осложнений в этой группе достигает 30-37 %. Расшифровка процесса клеточного и гуморального иммунитета позволила выявить механизмы работы антимикробной защиты человека. Важным компонентом этих механизмов являются цитокины, которые оказались неотъемлемыми модуляторами иммунного ответа.
Одним из наиболее важных и изученных цитокинов, участвующих в процессе развития и усиления иммунного ответа, является интерлейкин2. Многогранность биологической активности интерлейкина2 позволяет при его применении в качестве иммуномодулятора рассчитывать не только на коррекцию проявлений иммунной недостаточности, но и на оптимизацию функционирования всей системы иммунитета и адекватное ее взаимодействие с другими системами организма. Широкий спектр биологических эффектов интерлейкина2 объясняет повышенное внимание специалистов к рекомбинантным препаратам этого цитокина как потенциальным средствам иммунотерапии различных вариантов вторичной иммунной недостаточности. Наше внимание привлек отечественный препарат рекомбинантного интерлейкина2 – ронколейкин, выделенного из клеток продуцента – рекомбинантного штамма непатогенных пекарских дрожжей вида Saccharomyces cerevisiae. Ронколейкин – полный структурный и функциональный аналог эндогенного интерлейкина2, обладающий тем же спектром функциональной активности. Препарат включен в Федеральное руководство по использованию лекарственных средств (формулярная система) МЗ РФ. Препарат успешно прошел клинические испытания и используется в комплексном лечении различных патологических процессов.
Однако информации о применении ронколейкина в качестве средства профилактики послеоперационной инфекции у больных СД при ампутации конечности на уровне бедра в доступной литературе найдено не было. Все это послужило основанием для настоящего исследования.
Цель исследования – улучшить результаты хирургического лечения при ампутации нижних конечностей на уровне бедра у больных сахарным диабетом, используя препарат рекомбинантного интерлейкина2 ронколейкин в целях иммунопрофилактики.
Материал и методы исследования
На первом этапе исследования для выявления факторов, способствующих развитию инфекционных осложнений в послеоперационном периоде у больных СД 2го типа, анализировались результаты лечения 67 больных. В группу включались все больные, которым выполнялась ампутация на уровне бедра по поводу гнойновоспалительных заболеваний нижних конечностей на фоне диабетической ангиопатии сосудов нижних конечностей (табл. 1).
-2010/52/1.png)
Всем больным проводилась традиционная предоперационная антибиотикопрофилактика цефазолином в дозе 2 г внутримышечно за 1 ч до операции. Выбор антибиотика и схема профилактики были регламентированы внутрибольничным формуляром антибиотикопрофилактики и рекомендациями межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии и научнометодического центра Минздрава России по мониторингу антибиотикорезистентности 2005 г. В процессе исследования любые другие антибактериальные средства или препараты иммуноориентированной терапии не использовались. У пациентов оценивались частота возникновения инфекционных послеоперационных осложнений в зависимости от тяжести состояния, массы тела больного, наличия сопутствующей патологии, а также от степени декомпенсации сахарного диабета, длительности предоперационного нахождения в стационаре, наличия и выраженности иммунодефицита.
Ампутация нижней конечности на уровне бедра проводилась с выкраиванием кожных, фасциальных лоскутов и пересечением мышц у основания этих лоскутов. Во всех случаях использовалась спинномозговая анестезия. Рана ушивалась наглухо с оставлением в подкожной клетчатке на 2 сут. дренажа по Редону для активной аспирации раневого отделяемого. Дренаж удаляли на 2е сутки после операции. При удалении из дренажа раневое отделяемое в количестве около 3 мл собирали в пробирку. В клинической лаборатории делали мазки, просматривали под микроскопом, подсчитывали клеточные элементы, микрофлору. Для бактериологического исследования использовали свободный участок дренажа, находившийся в полости раны. Швы снимались на 8-9е сутки.
При повышении температуры тела, появлении отека, гиперемии кожи культи, гнойного отделяемого из раны регистрировалась инфекция области оперативного вмешательства. Появление у больного кашля, развитие или нарастание одышки, повышение температуры тела, наличие свежих инфильтративных изменений при рентгенографии в легких были диагностическими критериями развития пневмонии в послеоперационном периоде.
После уточнения факторов, способствующих развитию послеоперационных инфекционных осложнений, оценивалась эффективность иммунопрофилактики послеоперационной хирургической инфекции препаратом рекомбинантного интерлейкина2 – ронколейкином с использованием метода подкожного введения. Проведено исследование, в которое были включены 60 больных (42 женщины и 18 мужчин) от 55 до 75 лет с СД 2го типа, которым предстояла ампутация на уровне бедра по поводу гнойносептических заболеваний дистальных отделов конечностей. Больные были распределены в две группы. Группы были сопоставимы по длительности заболевания СД, полу, возрасту, наличию сопутствующих заболеваний.
В контрольной группе (30 больных) предоперационная профилактика инфекции проводилась по традиционной схеме: за 1 ч до ампутации вводили цефазолин в дозе 2 г внутримышечно. Основной группе (30 больных) профилактика инфекции осуществлялась введением за 1 ч до ампутации цефазолина в дозе 2 г внутримышечно и, кроме того, ронколейкина в дозе 0,5 мг (500 000 ME – 250 000 МЕ в бедро и живот) подкожно в смеси с 2 мл изотонического раствора хлорида натрия в одном шприце. В послеоперационном периоде у больных основной группы продолжалось введение ронколейкина: вторая инъекция 0,5 млн ЕД ронколейкина – через 48 ч после завершения операции, третья инъекция 0,5 млн ЕД ронколейкина – на 5е сутки послеоперационного периода подкожно (по 250 000 МЕ в бедро и живот) в смеси с 2 мл изотонического раствора хлорида натрия в одном шприце.
Результаты, полученные при исследованиях, обработаны вариационностатистическим методом по tкритерию Стьюдента. Различие считали статистически достоверным, если уровень значимости был p < 0,05, что является мерой достаточной надежности результатов в медицине. Расчеты произведены на персональном компьютере с использованием статистической программы Exсel.
Результаты исследования и их обсуждение
При оценке результатов лечения 67 пациентов, страдающих СД 2го типа, после ампутации нижней конечности на уровне бедра по поводу гнойновоспалительных заболеваний конечностей отмечено развитие инфекционных послеоперационных осложнений у 14 (21 %) больных.
При сопоставлении особенностей течения послеоперационного периода и данных предоперационного обследования установлено, что фактором, способствующим развитию инфекций области оперативного вмешательства у больных СД 2го типа после ампутации нижних конечностей на уровне бедра, является наличие гипертонической болезни III стадии, ожирения II и более стадии. У 44 % больных с индексом массы тела (ИМТ) 40 кг/м2 и более развивалось нагноение культи в послеоперационном периоде. Вероятно, это связано с тем, что выполнение ампутации при морбидном ожирении сопровождается техническими сложностями, что способствует образованию и затрудняет своевременную диагностику подкожных гематом, сером области операционной раны.
Развитие пневмоний у трети больных с ИМТ 40 кг/м2 и более связано с ограничением подвижности пациентов в пределах постели, усугублением течения сопутствующей патологии. В развитии послеоперационной пневмонии играют роль сопутствующая гипертоническая болезнь III стадии, фактор курения, ограничение подвижности изза заболеваний нервной системы, суставов. Курение способствует увеличению частоты развития пневмоний в послеоперационном периоде (16,6 % у курящих против 7,2 % у некурящих).
В развитии местных и висцеральных инфекционных осложнений послеоперационного периода важными являются длительность предоперационного пребывания больных в стационаре (нахождение в стационаре до операции более 4 сут.), общее состояние больных средней и более степени тяжести. Инфекционные осложнения в послеоперационном периоде развились у 30,7 % (9) больных среди пациентов с тяжелым общим состоянием до операции. Из больных с состоянием средней степени тяжести осложненное инфекцией течение послеоперационного периода развилось у 4 (10,5 %) пациентов.
Одним из ведущих факторов в развитии послеоперационных инфекционных осложнений было наличие декомпенсированного СД. Инфекция послеоперационного периода развилась у 80 % больных с декомпенсированным СД. В том числе инфекция области оперативного вмешательства возникала у 40 % пациентов с декомпенсированным течением СД.
В то же время нагноение культи у больных с компенсированным СД отмечалось лишь в 7 % случаев. Это обстоятельство связано с выраженной иммуносупрессией у пациентов с декомпенсированным СД. При анализе показателей иммунограмм у таких больных в популяционном составе лимфоцитов отмечены изменения, характеризующие существенные нарушения в иммунной системе. Статистически достоверно сниженным (р < 0,05) было относительное и абсолютное содержание зрелых Тлимфоцитов, Тхелперов у пациентов с декомпенсированным СД, а также уменьшение показателя абсолютных значений Тцитотоксических лимфоцитов. Отмечается угнетение факторов неспецифического иммунитета. Достоверно (р < 0,05) снижено значение фагоцитарного показателя у больных с декомпенсированным СД.
Показатели иммуноглобулинов были в пределах нормы, что обусловлено преимущественным поражением Тклеточного иммунитета. При анализе иммунограмм важно отметить статистически достоверно сниженное (р < 0,05) абсолютное содержание зрелых Тлифоцитов у больных с развившимися в дальнейшем послеоперационными инфекционными осложнениями по сравнению с пациентами с неосложненным течением послеоперационного периода.
При анализе цитограмм раневого отделяемого на 2е сутки послеоперационного периода не удалось выявить какихлибо закономерностей между количеством и процентным соотношением клеточных элементов и частотой нагноения ран в послеоперационном периоде.
У 29 (43 %) из 67 пациентов микрофлоры в мазках обнаружено не было. У остальных 38 (57 %) в мазках выявлены микроорганизмы. Их них у 32 (48 %) больных в цитограммах отмечено от 0 до 10 микробных клеток в поле зрения и у 6 (9 %) пациентов количество микробов в мазках было от 10 до 100 микробных клеток в поле зрения.
Использование микроскопии осадка раневого отделяемого культи на 2е сутки после операции позволяет прогнозировать нагноение раны в послеоперационном периоде.
При бактериологическом исследовании кусочков дренажей, удаленных на 2е сутки послеоперационного периода, рост микрофлоры обнаруживался в 34 % случаев (23 больных от общего числа пациентов). Следует отметить, что положительные бактериологические посевы на 2е сутки после операции в 35 % случаев соответствовали нагноению раны культи на 5-8е сутки послеоперационного периода. Наличие развернутого микробиологического анализа возбудителей к 7м суткам послеоперационного периода помогает в подборе антибиотиков для лечения развившегося нагноения операционной раны.
Таким образом, анализируя полученные данные, можно сделать вывод, что перечисленные факторы риска, особенно декомпенсированное течение СД, ведут к увеличению числа послеоперационных инфекционных осложнений. Заметим, что ведущую роль здесь играет угнетение иммунитета. По этой причине введение в схему профилактики хирургической инфекции препарата интерлейкина2 наиболее оправданно. Ронколейкин достаточно быстро корректирует иммунологические изменения, поэтому он был дополнительно введен в традиционную схему антибиотикопрофилактики перед операцией. Препарат рекомбинантного интерлейкина2 (ронколейкин) во всех случаях вводился по единой методике подкожно. Частота послеоперационных инфекционных осложнений в группе больных, которые получали иммунопрофилактику препаратом ронколейкин, составила 3,3 % (нагноение послеоперационной раны у 1 больного) против 20 % осложненного инфекцией послеоперационного течения у пациентов контрольной группы.
Висцеральных послеоперационных инфекционных осложнений у больных основной группы не было.
Отмечалось уменьшение длительности нахождения в стационаре больных основной группы в среднем на 8,4 ± 0,9 сут., что связано с меньшим количеством инфекционных осложнений в группе. Обращает на себя тенденция к более быстрой нормализации общего самочувствия у больных, получавших иммунопрофилактику. На введение ронколейкина ожидалось появление изменений в показателях иммунитета.
Следует отметить статистически достоверное (р < 0,05) увеличение лимфоцитов в основной группе по сравнению с контрольной, что обусловлено иммуностимулирующим действием интерлейкина2. В результате применения ронколейкина увеличилось количество преимущественно популяции Тклеточного звена иммунитета.
Наблюдался прирост количества Влимфоцитов как результат активизации Тклеточного звена иммунитета. Достоверно (р < 0,05) увеличилось абсолютное количество Влимфоцитов в основной группе к 7м суткам послеоперационного периода по сравнению с контрольной группой. Отмечено статистически незначимое (р > 0,05) увеличение уровня иммуноглобулинов к 7м суткам послеоперационного периода у больных, получавших ронколейкин, по сравнению с больными контрольной группы.
У больных, получавших иммунопрофилактику, отмечается увеличение показателей факторов неспецифического иммунитета: статистически достоверно (р < 0,05) увеличились значения показателей фагоцитарного числа и фагоцитарного показателя к 7м суткам послеоперационного периода по сравнению с показателями дооперационного периода.
Статистически достоверно (р < 0,05) более высокие значения показателей относительного и абсолютного содержания зрелых Тлимфоцитов, Тхелперов в основной группе к 7м суткам послеоперационного периода по сравнению с контрольной группой.
В цитограммах раневого отделяемого у 13 (43 %) больных основной группы и у 16 (53 %) контрольной группы на 2е сутки после операции обнаруживалась смешанная микрофлора. Цитограммы с количеством микрофлоры от 0 до 10 микробных клеток в поле зрения были у 11 (36 %) больных основной группы и у 13 (43 %) пациентов контрольной.
Цитограммы с количеством микрофлоры от 10 до 100 микробных клеток в поле зрения были у 2 (7 %) больных основной группы и у 3 (10 %) пациентов контрольной группы. Заметим, что при таком количестве микрофлоры нагноение послеоперационной раны развилось у 1 больного основной группы и у 2 контрольной группы.
Бактериологическое исследование дренажей, удаленных на 2е сутки послеоперационного периода, выявило рост микрофлоры в основной группе у 8 (27 %) больных и у 9 (30 %) – в контрольной.
Необходимо подчеркнуть, что инфекция области оперативного вмешательства развилась только у 1 (12,5 %) больного основной группы из 8 положительных бактериологических посевов. В то же время нагноение культи в контрольной группе развилось у 3 (33 %) больных из 9 посевов с ростом микрофлоры. На основании полученных данных можно говорить об уменьшении числа нагноения ран у больных, получавших иммунопрофилактику ронколейкином.
Следует отметить, что тяжелых нежелательных реакций на введение ронколейкина зарегистрировано не было.
Таким образом, применение ронколейкина у больных сахарным диабетом при ампутации на уровне бедра по поводу гнойнонекротических заболеваний нижних конечностей приводит к коррекции нарушений иммунитета и, как следствие, к снижению числа осложнений инфекционного характера в послеоперационном периоде, сокращению сроков лечения больных. Ронколейкин является безопасным и удобным лекарственным средством.
Иммунопрофилактика с использованием метода подкожного введения ронколейкина у больных сахарным диабетом при ампутации ни?
