Новости в области сахарного диабета
Сахарный диабет – заболевание, приводящее к пожизненным инъекциям инсулина, инвалидности и фатальным осложнениям. Ученые из Приволжского исследовательского медицинского университета (ПИМУ) приступили к разработке принципиально нового метода лечения этого недуга.
Чтобы понять механизм технологии, нужно сказать о том, как работает поджелудочная железа, отчего возникает диабет. В этом органе есть так называемые бета-клетки, объединенные в островки, которые автоматически продуцируют инсулин в ответ на повышение уровня глюкозы в крови. При ряде аутоиммунных или хронических болезней общая их масса снижается, появляются функциональные нарушения в виде недостаточной выработки инсулина. Результат – повышение уровня глюкозы в сыворотке крови.
– Это инсулинопотребный сахарный диабет. Он возникает, если число островков уменьшилось на 80 процентов, – рассказывает заведующий кафедрой факультетской хирургии и трансплантологии, главный внештатный трансплантолог минздрава Нижегородской области Владимир Загайнов.
Ученый подчеркивает, что метод лечения диабета только один – трансплантация поджелудочной железы. Потребность в этой операции в России удовлетворяется на тысячные доли процента, что связано с дефицитом донорских органов. Во всех остальных случаях речь идет о компенсации заболевания с помощью инсулина. Однако даже пересадка сопряжена с необходимостью иммуносупрессивной терапии, чтобы организм пациента не отторгал донорский орган. А у нее есть свои минусы, особенно в отдаленном периоде.
Главная идея проекта – пересадка не всей поджелудочной железы, а только островков, состоящих из тех самых бета-клеток.
– Островки будут выделяться из донорской железы специальным способом. Даже если целая железа не годится для трансплантации, из нее можно попытаться выделить островки и пересадить их, – поясняет Владимир Загайнов.
В мире эту идею пытаются реализовать разными способами и с разной степенью успешности. Введение островков от донора требует все той же небезопасной иммуносупрессивной терапии. В ПИМУ ученые разрабатывают вариант пересадки клеток, заключенных в специальные пористые капсулы. В теории клетки приживаются и начинают вырабатывать инсулин. Человек излечивается от диабета. А поры капсулы достаточно малы, чтобы предотвратить атаку иммунных клеток организма, поэтому никакой иммуносупрессивной терапии не требуется. Важно, что речь идет о малоинвазивных операциях, а не о сложной трансплантации. Возможных вариантов несколько: введение в брюшную полость путем пункции либо введение в печень по воротной вене.
Первые эксперименты ученых из НИИ экспериментальной онкологии и биомедицинских технологий ПИМУ вместе с Институтом металлоорганической химии РАН оказались успешными.
– В отдаленной перспективе планируем проработать выращивание бета-клеток из стволовых, – говорит Владимир Загайнов. – Параллельно вместе с коллегами из Национального медицинского исследовательского центра трансплантологии и искусственных органов имени Шумакова занимаемся легитимизацией технологии. Раньше в России за это никто не брался, поэтому трансплантация островков бета-клеток поджелудочной пока не вошла в список разрешенных, хотя в мире это уже существует. Надеемся, что в ближайшее время вопрос будет решен.
Планируем проработать выращивание бета-клеток из стволовых
В 2022 году проект, выполняемый по госзаданию Минздрава России, завершится. Можно будет испытывать метод на животных, а затем заниматься регистрацией. На мой вопрос, когда лечение будет доступно российским пациентам, профессор Загайнов ответил кратко:
– Деклараций в жизни хватает, давайте заниматься делом.
Комментарий
Ольга Занозина, доктор медицинских наук, заведующая отделением эндокринологии Нижегородской областной больницы имени Семашко:
– Наряду с совершенствованием самих инсулинов, способов их введения в организм пациента, улучшением терапевтического обучения больных сахарным диабетом развивается и другое направление – трансплантационные технологии, позволяющие вводить бета-клетки островков поджелудочной железы, которые вырабатывают инсулин, в организм больного человека.
Положительный эффект достигается при виртуозном заборе, хранении и введении островковых клеток больному человеку. При успешном результате – почти полный контроль за гликемией, отсутствие гипогликемий и потребности в экзогенном инсулине. Вся эта работа требует ювелирного мастерства.

Компания Ново Нордиск объявила, что выводит на российский рынок новый сверхбыстродействующий прандиальный инсулин Фиасп®. Профиль эффективности и безопасности препарата был исследован в рамках программы клинических исследований IIIа фазы “onset”
Компания Ново Нордиск объявила, что выводит на российский рынок новый сверхбыстродействующий прандиальный инсулин Фиасп® – инсулин аспарт в инновационной лекарственной форме, которая более точно имитирует естественный физиологический ответ инсулина у человека без сахарного диабета после приема пищи по сравнению с препаратом НовоРапид® (обычный инсулин аспарт). Препарат Фиасп® также обладает возможностью гибкого режима дозирования (до 20 минут после начала приема пищи) без ущерба для общего контроля гликемии. Фиасп® – единственный сверхбыстродействующий инсулин аспарт с лучшим контролем гликемии без увеличения риска всех гипогликемий и возможностью гибкого введения.
«Многие пациенты с сахарным диабетом вынуждены бороться с чрезмерной гипергликемией после приема пищи, которая возникает из-за того, что доступные в настоящее время быстродействующие инсулины все же недостаточно быстры. Помимо того, что это создает ежедневные проблемы, отражаясь на качестве жизни, неоптимальный контроль постпрандиальной гликемии значительно увеличивает риск развития тяжелых осложнений сахарного диабета, – сказал доктор медицинских наук, главный научный сотрудник, заведующий отделением диабетической стопы, ФГБУ «Национальный медицинский исследовательский центр эндокринологии» МЗ РФ, профессор Гагик Радикович Галстян. – Появление ультракороткого инсулина Фиасп® открывает новую страницу в диабетологии, предоставляя возможность результативно и безопасно держать постпрандиальную гипергликемию под контролем».
Препарат Фиасп® всасывается быстрее, чем НовоРапид®, появляясь в кровотоке после введения в два раза быстрее, что приводит к улучшению контроля гликемии после приема пищи. В клинических исследованиях препарат Фиасп® продемонстрировал улучшение общего контроля гликемии при сахарном диабете 1 типа и сопоставимый общий контроль гликемии при сахарном диабете 2 типа по сравнению с препаратом НовоРапид®. Результаты также показали улучшение контроля прандиальной концентрации глюкозы при сахарном диабете 1 и 2 типа. Это было достигнуто без существенных различий в общей частоте развития тяжелой или подтвержденной гипогликемии по сравнению с препаратом НовоРапид®.
«Компания Ново Нордиск всегда стремится найти инновационные решения, направленные на повышение качества и увеличение продолжительности жизни людей с сахарным диабетом. Значимым преимуществом для здоровья людей с диабетом является наибольшее приближение к естественному физиологическому ответу инсулина у человека без сахарного диабета, и Фиасп® является примером этого, – отметил вице-президент и генеральный директор компании Ново Нордиск в России и Беларуси Ханс Дюиф. – В этой области в последние годы было мало инноваций, и мы действительно рады предложить новое решение, которое удовлетворяет критическую потребность людей с сахарным диабетом в достижении оптимального контроля глюкозы во время приема пищи».
Источник: пресс-релиз компании Ново Нордиск
Все новости и обзоры – в нашем канале на «Яндекс.Дзене».
Подписывайтесь
Сахарный диабет первого типа, который обычно развивается у детей и подростков, является хроническим заболеванием. Последние два года в Израиле и других странах ведутся интенсивные исследования этого заболевания, результаты которых заставляют ученых полностью пересмотреть традиционный подход к лечению сахарного диабета.
Считается, что сахарный диабет первого типа является аутоиммунным заболеванием, при котором происходит разрушение бета-клеток поджелудочной железы, ответственных за выработку инсулина — гормона, с помощью которого сахар (глюкоза) проникает в клетки организма. При разрушении бета-клеток количество выделяемого инсулина уменьшается и уровень сахара в крови повышается, что приводит к поражению кровеносных сосудов и другим пагубным последствиям для организма.
Несмотря на долгие годы исследований, ученые пока что не могут объяснить, почему организм разрушает собственные бета-клетки. Одна из теорий гласит, что причиной является вирусное заражение, при котором на молекулярном уровне вирусы похожи на бета-клетки, таким образом защитная реакция организма может быть ошибочно направлена на данный вид клеток. Согласно другой теории, причиной аутоиммунной атаки организма является излишняя стерильность, в которой растут дети, что приводит к повышенной чувствительности иммунной системы к собственным бета-клеткам поджелудочной железы.
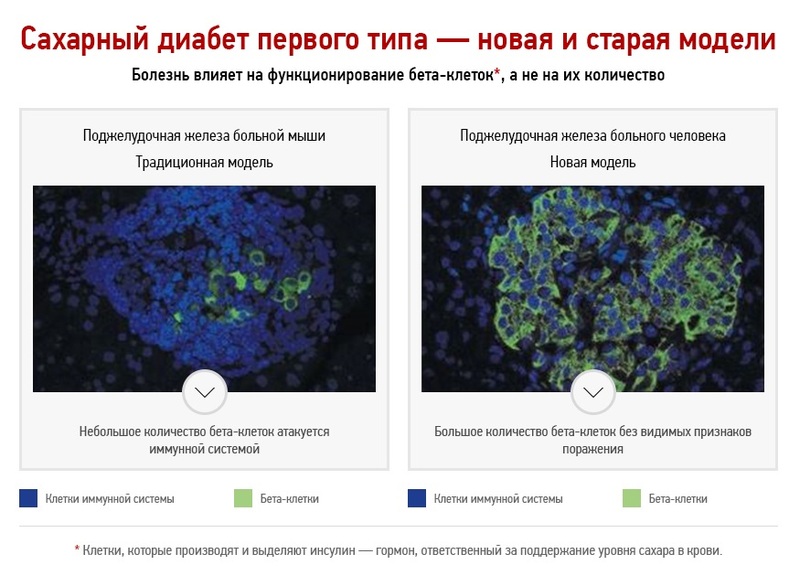
Классическая модель развития сахарного диабета первого типа
Принятая на сегодня теория развития сахарного диабета первого типа гласит, что первая стадия заболевания продолжается от нескольких месяцев до нескольких лет, в течение которых происходит постепенное разрушение бета-клеток поджелудочной железы. Заболевание не диагностируется на начальной стадии, потому что оставшиеся клетки начинают выделять больше инсулина, чтобы скомпенсировать его недостаток в крови. Сахарный диабет первого типа диагностируется, когда остается только 10 % бета-клеток, уже не способных выделять достаточно инсулина для поддержания требуемого уровня сахара в крови. На этом этапе пациент получает лечение — иньекции инсулина, параллельно с этим происходит полное уничтожение организмом оставшихся бета-клеток. Так как разрушение бета-клеток является необратимым процессом, пациент вынужден получать лечение на протяжении всей жизни.
Данная модель на протяжении многих лет оказывала огромное влияние на исследование сахарного диабета первого типа. Основным предположением было то, что на момент диагностики у пациента практически не остается бета-клеток поджелудочной железы. Старая модель основывалась на исследованиях, проведенных на одном виде мышей, развивающих болезнь, похожую на сахарный диабет первого типа у людей, а также на наблюдениях онкологических пациентов, у которых была удалена часть поджелудочной железы.
Новые исследования
В последние два года, благодаря значительным логическим усилиям, ученые получили возможность изучать десятки образцов тканей поджелудочной железы пациентов, страдающих сахарным диабетом первого типа, которые умерли незадолго после диагностики заболевания. Речь идет о редких и трагических случаях, когда пациенты (в основном дети) погибали при несчастных случаях, а семьи соглашались пожертвовать их органы для исследований.
Анализ образцов ткани этих пациентов показал неожиданные результаты. Оказалось, что в тканях поджелудочной железы имеется большое количество бета-клеток без видимых признаков поражения со стороны иммунной системы, а их количество значительно выше, чем 10 % здоровых клеток (согласно классической модели). Таким образом, ученые пришли к выводу, что на этапе диагностики сахарного диабета у человека имеется большое количество незатронутых иммунной системой бета-клеток.
Данное открытие проливает свет на известный в медицине эффект при начале лечения сахарного диабета первого типа с помощью инсулина, при котором в течение первых месяцев происходит временное «выздоровление», когда бета-клетки начинают вырабатывать инсулин в достаточном количестве. Классическая модель не может объяснить, каким образом такое небольшое количество бета-клеток выделяет достаточно инсулина. Новое исследование утверждает, что происходит функциональное поражение клеток, и при «разгрузке» с помощью инъекций инсулина их функции временно восстанавливаются, что было бы невозможно, если бы клетки были разрушены.
Важно отметить, что в организме происходит аутоиммунная реакция, направленная на разрушение бета-клеток поджелудочной железы. Однако, согласно новым исследованиям, происходит не уничтожение бета-клеток, а нарушение их функционирования, поэтому можно надеяться, что поражение такого рода может быть обратимым.
Какие последствия будет иметь данное открытие?
Теперь, когда известно, что на момент диагностики сахарного диабета первого типа имеется достаточно бета-клеток, пациент должен получать лекарства, нейтрализующие иммунную систему с целью предотвращения нарушения функционирования этих клеток. Разработка таких лекарств уже ведется. Другим направлением будут лекарства, которые смогут вернуть способность вырабатывать инсулин пораженным клеткам или обеспечить достаточную выработку инсулина оставшимися клетками. Ученые пока что далеки от создания подобных препаратов, но главное, что результаты последних исследований показали верный путь для лечения этого заболевания.
12447 просмотров
На 80-й сессии ежегодного конгресса Американской диабетической ассоциации (ADA 2020) представили результаты недавних исследований по диабетологии. В частности, были освещены такие темы, как распространенность диастолической дисфункции среди молодых людей с диабетом в США, сравнение эффективности ингибиторов SGLT2 и агонистов рецепторов ГПП-1 для пациентов с диабетом и потенциал высокочастотной стимуляции спинного мозга для облегчения боли при диабетической нейропатии.
В США среди молодых людей с диабетом распространена диастолическая дисфункция
Согласно мнению экспертов из Медицинского центра детской больницы Цинциннати (Cincinnati Children’s Hospital Medical Center), в США практически половина подростков и молодых людей с сахарным диабетом 1-го типа (СД1) или сахарным диабетом 2-го типа (СД2) имеют диастолическую дисфункцию, являющуюся прямым предшественником сердечной недостаточности (СН).
Для анализа были использованы данные из 4 центров США по пациентам с СД1 или СД2, включенным в исследование SEARCH for Diabetes in Youth, которые в течение 2016 – 2019 гг. прошли допплерографию тканей. Средняя продолжительность заболевания диабетом у участников составляла 10,9 года. Диастолическая дисфункция у пациентов определялась нарушением показателей объема диастолического наполнения левого желудочка (ЛЖ), давления наполнения ЛЖ и скорости митрального клапана. Из 458 участников исследования 255 имели СД1 (средний возраст 21,2 года; 60,8% – белые, неиспаноязычного происхождения; 54,1% – женщины; средний уровень А1с – 9±1,9%), а 203 страдали СД2 (средний возраст 24,3 года, 24,1% – белые, неиспаноязычного происхождения; 75,4% – женщины; средний А1с – 9,6±3%).
В результате у участников с СД2 обнаружили худший профиль сердечно-сосудистого риска (выраженный более высокими показателями индекса массы тела, систолического и диастолического артериального давления, уровня триглицеридов, ХС ЛПНП и A1c, а также более низким уровнем ЛПВП), по сравнению с пациентами с СД1. Кроме того, у испытуемых с СД2 также зафиксировали более низкие показатели объема наполнения ЛЖ, скорости митрального клапана и более высокое давление ЛЖ. Вместе с тем, нескорректированная частота диастолической дисфункции была высокой в обеих группах (57,7% при СД2 против 47,2% при СД1).
Результаты исследования указывают на необходимость наблюдения за молодыми людьми с диабетом на предмет развития у них сердечно-сосудистых осложнений.
Эксперты сравнили эффективность ингибиторов SGLT2 с агонистами рецепторов ГПП-1 для пациентов с диабетом
По данным наблюдательного исследования в реальных условиях, проведенного экспертами из компании Humana, у пациентов с сахарным диабетом 2-го типа (СД2), которым назначают ингибиторы натрий-глюкозного котранспортера 2-го типа (SGLT2), зарегистрированы лучшие показатели приверженности к лечению, меньшее число обращений за медицинской помощью и более низкие расходы на медицинскую помощь, по сравнению с теми, кто использует агонисты рецепторов глюкагоноподобного пептида-1 (ГПП-1).
В ходе исследования были проанализированы сведения из базы данных Humana Research для выявления пациентов с СД2, которым недавно назначили ингибиторы SGLT2 или агонисты рецепторов ГПП-1 в период с января 2015 по июнь 2017 года. Возраст участников исследования составил 19-89 лет. В каждой из групп, проходящих лечение (либо ингибиторами SGLT2, либо агонистами рецепторов ГПП-1), было по 5507 пациентов.
Установили, что участники, которым назначили терапию агонистами рецепторов ГПП-1, были более склонны прекратить свое лечение, были подвержены более высокому риску госпитализации и с большей вероятностью обращались в отделения неотложной помощи, чем пациенты, принимавшие ингибиторы SGLT2. Кроме того, прием агонистов рецепторов ГПП-1 ассоциировался с более высокими медицинскими и фармацевтическими затратами по сравнению с использованием ингибиторов SGLT2.
Однако совокупный риск первичного сердечно-сосудистого исхода (инфаркта миокарда, инсульта или летального исхода) и вторичного сердечно-сосудистого исхода (сердечной недостаточности или смерти) был схожим среди участников обеих групп.
Высокочастотная стимуляция спинного мозга может облегчить боль при диабетической нейропатии
По данным экспертов из компании Nevro, высокочастотная стимуляция спинного мозга оказывает эффективное воздействие на облегчение боли у пациентов с диабетической нейропатией.
В исследовании SENZA-PDN приняли участие люди с болезненной диабетической нейропатией. При этом, 103 пациентов рандомизировали для прохождения традиционного медицинского лечения, а 113 участникам наряду с такой терапией также провели имплантацию стимулятора спинного мозга. Средний возраст участников равнялся примерно 61 годам, и около двух третей пациентов составили мужчины. На момент включения в испытание все пациенты испытывали боль в нижних конечностях со средней интенсивностью не менее 5 из 10 см по визуальной аналоговой шкале (VAS).
Через 3 месяца после стимуляции спинного мозга у 79% участников, которым осуществили имплантацию устройства, зарегистрировали ответную реакцию, выраженную снижением боли на 50% или более, а также отсутствием ухудшения неврологических симптомов, связанных с болезненной диабетической нейропатией. Для сравнения: лишь 5% участников, которым назначили только традиционное медицинское лечение, добились такого же результата.
Средний показатель интенсивности боли по шкале VAS среди пациентов, которым осуществили имплантацию стимулятора спинного мозга, снизился с 7,6 в начале исследования до 2,4 спустя 1 месяц и 1,7 спустя 3 месяца. Что касается участников, следовавших обычной терапии, этот показатель равнялся 7 в начале испытания, затем сократился до 6,7 спустя 1 месяц и составил 6,5 через 3 месяца.
Улучшение качества жизни, связанное с качеством сна и активной жизнедеятельностью, также было более заметным через 3 месяца в группе участников, прошедших стимуляцию спинного мозга.
