При сахарном диабете 2 типа экг


Обзор

- Распространённость сахарного диабета (СД) неуклонно увеличивается.
- Типичными осложнениями СД являются макро- и микроангиопатии,
- приводящие к развитию сердечно-сосудистых заболеваний (ССЗ),
- сопряженных с рядом особенно неблагоприятных состояний, такими как:
- инфаркт миокарда,
- острое нарушение мозгового кровообращения,
- потери конечности в результате нетравматической ампутации,
- ретинопатии.
- СД является мощнейшим независимым фактором риска не только увеличения заболеваемости ССЗ,
- но и смертности от ССЗ, которая зачастую ассоциирована с нарушением ритма, в первую очередь с:
- фибрилляцией предсердий (ФП),
- желудочковой аритмией (ЖА).
- но и смертности от ССЗ, которая зачастую ассоциирована с нарушением ритма, в первую очередь с:
- Этот обзор – попытка обобщить имеющиеся данные о патофизиологии связи между СД и нарушением ритма (ФП и ЖА).
Введение
- Сахарный диабет (СД) давно признан значимым фактором риска ССЗ, причем он влияет как на показатели заболеваемости, так и смертности.
- Несмотря на то, что ишемическая болезнь сердца является наиболее часто регистрируемым осложнением СД, проводящая система сердца – так же является мишенью для пагубного воздействия гипергликемии.
- В Фрамингемском исследовании (период наблюдения – 38 лет) было показано, что СД является независимым фактором риска ФП.
- Недавно, Хаксли и соав. провели мета-анализ и выявили, что риск развития ФП у пациентов с СД на 40% выше, чем у пациентов без диабета.
- Кроме того, в последние годы появляется всё больше и больше данных, свидетельствующих о том, что гипогликемия провоцирует ЖА.
- И в то время как число больных диабетом растет день ото дня, патогенез развития аритмии при СД остается не до конца ясным.
- Вполне вероятно, что в ближайшее время связь между этими состояниями будет изучаться более пристально. А в этом обзоре изложено общее представление об имеющихся сейчас данных о связи между нарушениями ритма и СД.
Диабет и фибрилляция предсердий

- ФП – самый распространенный в клинической практике вид аритмии, приводящий к увеличению как заболеваемости другими ССЗ, так и смертности от них.
- Ранее в Фрамингемском исследовании уже было показано, что СД является мощным независимым фактором риска ФП. Наличие такой тесной связи между двумя состояниями закономерно рождает вопрос: а существует ли объяснение патогенеза этого явления? И хотя нет единого и однозначного ответа на этот вопрос, несомненно, важную роль в патогенезе играют:
- Процессы электрического и анатомического ремоделирования миокарда.
- Характерный для ФП анатомо-гистологическим признак – обширный фиброз в области предсердия, который запускает патогенетическую цепочку формирования патологического ритма;
- А, кроме того, расширение зоны фиброза предрасполагает к
- трансформации пароксизмальной формы ФП в постоянную
- и устойчивости ФП к лечению антиаритмическими препаратами.
- Kato и соав. в опытах на крысах показали, что определенную роль в инициации ФП может играть диабет-ассоциированный фиброз предсердий.
- Есть основания полагать, что ключевым фактором, запускающим процесс фиброза в условиях СД, служит повышение уровня системного и клеточного оксидативного стресса.
- В исследовании Dudley и соав. оценивали концентрацию супероксид-анион-радикала на модели ФП у свиней.
- Авторы сравнивали уровни супероксид-анион-радикала в левом предсердии в группах свиней
- с нормальным сердечным ритмом
- и со стимулированным ритмом предсердий.
- Исследование показало, что во второй группе концентрация супероксид-анион-радикала в левом предсердии была почти в три раза ваше, чем в контрольной.
- Авторы сравнивали уровни супероксид-анион-радикала в левом предсердии в группах свиней
- Anderson и соав. показали, что у людей, страдающих диабетом, в тканях предсердия усилены процессы окислительного стресса в митохондриях.
- Результаты этих работ говорят о том, что на фоне СД, несмотря на повышение уровня системного оксидативного стресса, конкретно в тканях предсердия из-за активности митохондрий могут образовываться активные формы кислорода.
- Взаимодействие гликозилированных белков (неферметативное гликозилирование) и конечных продуктов избыточного гликозилирования (AGE) с соответствующими рецепторами (RAGE) повышает экспрессию гена фактора роста соединительной ткани (CGTF), в том числе и в миокарде предсердий.
- В связи с этим система AGE-RAGE может стимулировать фиброзирующие процессы в предсердии.
- У пациентов с СД зачастую выявляются признаки автономной нейропатии:
- обусловленной, по-видимому, нарушением равновесия в вегетативной нервной системе и доминированием её симпатического отдела;
- которая также играет важную роль в развитии ФП.
- В опытах на мышах со стрептозоцин-индуцированным сахарным диабетом Otake и соав. наглядно показали, что чрезмерная активация симпатической нервной системы повышает частоту ФП по сравнению с контрольной группой.
- При более детальном изучении оказалось, что у крыс с СД отмечается:
- Укорочение эффективного рефрактерный период (ЭРП) предсердий и
- Увеличение дисперсии ЭРП.
- В другом исследовании было предположено, что у пациентов с СД с сохранной фракцией выброса имеется связь между снижением скорости восстановления пульса и бóльшей распространённостью ФП.
- Вышеупомянутые клинические и лабораторные находки указывают на то, что определенную роль в патогенезе ФП у пациентов с СД играет дисфункция вегетативной нервной системы (дистония).
- Проводящая система сердца – одна из мишеней СД.
- К основным компонентам ремоделирования проводящей системы сердца относятся:
- Укорочение ЭРП предсердий;
- Увеличение дисперсии ЭРП;
- Замедление внутрипредсердной проводимости.
- Chao и соав. проанализировали результаты детализированного трёхмерного электроанатомического картирования миокарда 228 пациентов с СД или нарушением углеводного обмена, которым впервые была проведена радиочастотная абляция по поводу СД:
- В основной группе вольтаж обоих предсердий был значительно снижен;
- Более того, в этой группе пациентов частота рецидивов ФП была выше.
- Acar и соав. опубликовали результаты исследования: оказалось, что у пациентов с СД по сравнению с контрольной группой меж- и внутрипредсердная задержка импульса значительно больше,
- Это приводит к нарушению диастолической функции предсердия.
- Было показано, что у пациентов с СД развиваются специфические изменения, затрагивающие процессы межклеточного взаимодействия:
- Так, у мышей со стрептозоцин-индуцированным СД экспрессия коннексина 43 в предсердиях была значительно выше, чем экспрессия коннексина 40;
- Что может указывать на активацию экспрессии коннексина 43, мембранного белка из семейства белков щелевых контактов, обеспечивающего диффузию низкомолекулярных соединений между клетками, у пациентов с СД.
- Так, у мышей со стрептозоцин-индуцированным СД экспрессия коннексина 43 в предсердиях была значительно выше, чем экспрессия коннексина 40;
- К основным компонентам ремоделирования проводящей системы сердца относятся:
- По другим данным, более высокая распространённость ФП среди пациентов с СД обусловлена не столько хронической гипергликемией, сколько резкими колебаниями уровня гликемии.
- Saito и соав. показали, что у мышей со стрептозоцин-индуцированным СД ФП развивается чаще при больших колебаниях уровня гликемии.
- У пациентов без диабета, Huxley и соав. не удалось обнаружить связи между дебютом ФП и показателями:
- Гликемии натощак,
- Концентрацией инсулина,
- Уровнем
- В другом клиническом исследовании Fatemi и соав. проспективно оценивали влияние интенсивного гликемического контроля на частоту возникновения ФП у пациентов с СД:
- Любопытно, что авторам так и не удалось установить взаимосвязь между частотой ФП и характером проводимой терапии (интенсивной или стандартной).
- Однако нужно учесть, что в исследовании регистрация ЭКГ проводилась периодически из-за чего эпизоды пароксизмальной ФП могли пройти незамеченными, что в свою очередь могло отразиться на результатах.
- Рандомизированных исследований, посвященных влиянию СД на риск развития других наджелудочковых аритмий, не проводилось;
- Однако имеются сообщения о клинических случаях, в которых резкие метаболические нарушения на фоне кетоацидоза могли спровоцировать наджелудочковые тахиаритмии.
↓
- СД играет определяющую роль в развитии и поддержании ФП:
- Специфические структурные, электрические и электромеханические нарушения при диабете могут приводить к образованию анатомического субстрата для возникновения ФП.
- С другой стороны, пусковым механизмом в формировании аритмии могут быть:
- Резкие перепады гликемии (остро развывшаяся гипо- или гипергликемия),
- Резкое нарушение электролитного баланса и кислотно-щелочного равновесия,
- Вегетососудистая дистония.
Схема 1.Теоретический патогенез развития фибрилляции предсердий при сахарном диабете.

Диабет и аритмии желудочкового генеза
- И хотя основным связующим звеном между ЖА, ВСС и СД является ИБС, в формирование этого явления принимают участие проявления атеросклероза другой локализации (вне венечных артерий):
- Вегетососудистая дистония,
- Микроваскулярное поражение сердца,
- Структурные и электрические изменения желудочков.
- В связи с распространённостью атеросклеротических поражений сердца, а также с их обширностью этих поражений у пациентов с СД, в этой группе неминуемо выше распространённость
- Желудочковых аритмий (ЖА)
- И внезапной сердечной смерти (ВСС).
- Сердечно-сосудистые заболевания – ведущая причина смерти пациентов с СД;
- С патогенетической точки зрения СД – синоним атеросклероза и ишемической болезни сердца (ИБС).
- Нарушение реполяризации желудочков
- Определяется по удлинению интервала QT
- В некоторых исследования подчеркивается, что у пациентов с СД отмечается тенденция к удлинению QT;
- И ассоциировано с более высоким риском ЖА.
- Поскольку СД предрасполагает миокард к возникновению аритмий, вероятно, он же и является пусковым механизмом их возникновения.
- Определяется по удлинению интервала QT
- Работа Chen-Scarabelli и соавт. была посвящена изучению взаимосвязи между уровнем HbA1c и риском ЖА у пациентов с имплантированным ранее электрокардиостимулятором.
- В исследование вошли 141 пациент с СД, 195 пациентов – без.
- Была показано, что частота спонтанных ЖА
- В значительной мере зависит от уровня HbA1c (8%-10), а значит хронической гипергликемии и неполноценного гликемического контроля,
- И не зависит от удлинения QT.
- В одном небольшом исследовании было показано, что другой предвестник ЖА (микроальтернация (МА) зубцов Т) встречается в группе пациентов с СД без ранее выявленных ССЗ значительно чаще, чем в контрольной.
- При этом оказалось, что у пациентов с нетипичной формой МА зубцов Т был значительно повышен уровень HbA1c:
- Увеличение HbA1c на 1% соответствует 13-кратному увеличению риска развития нетипичной формы МА зубцов Т,
- А неполноценный гликемический контроль связан с более высоким риском спонтанных ЖА, независящих от продолжительности интервала QT.
- Подобные результаты свидетельствуют о том, что у диабетиков миокард склонен к электрической нестабильности,
- Что создает потенциальный субстрат для ЖА (вне зависимости от наличия рубцовых изменений и ишемический повреждений миокарда).
- При этом оказалось, что у пациентов с нетипичной формой МА зубцов Т был значительно повышен уровень HbA1c:
- С другой стороны, вегетососудистая дистония, развивающаяся при СД, приводит к непропорциональному воздействию симпатики на миокард,
- Усугубляя электрическую нестабильность
- И предрасполагая к развитию летальных аритмий.
- Ещё одной серьезной проблемой является диабетическая сенсорная нейропатия, которая может приводить
- Как к развитию ЖА,
- Так и к внезапной сердечной смерти (при развитии безболевой/немой ишемии миокарда).
- В другом рандомизированном проспективном исследовании авторы рассматривали связь между эпизодами гипогликемии и ЖА у пациентов с СД 2 типа и верифицированным ССЗ:
- 30 пациентов, получали инсулин и/или препараты сульфонилмочевины;
- Для контрольной группы с учётом возраста были подобраны 12 пациентов, получавших терапию препаратами с низким риском развития гипогликемии.
- В основной группе были выше частота
- Гипогликемий
- «Молчащих» ЖА.
- Дальнейшее изучение гипогликемии на риск развития ЖА изучали Pistrosch и соавт. на более крупных когортах пациентов с СД:
- Было показано, что гипогликемия может провоцировать развитие ЖА и
- Что не менее интересно, низко-нормальный уровень тиреотропного гормона, свидетельствующий о субклиническом гипертиреозе, является независимым фактором развития ЖА.
- И, несмотря на то, что два вышеупомянутых исследования не дают представления о причинно-следственных связях между гипогликемией и ЖА у пациентов с СД,
- Можно уверенно утверждать, что гипогликемия может служить провоцирующим фактором для развития ЖА
- Как вызывая чрезмерную стимуляцию симпатического отдела ВНС,
- Так и за счёт удлинения интервала QT.
- Можно уверенно утверждать, что гипогликемия может служить провоцирующим фактором для развития ЖА
- Интересно, что в другом исследовании наличие связи между СД и ЖА в группе пациентов с тяжелой сердечной недостаточностью не подтвердилось;
- Кроме того, авторы заключили, что в группе пациентов с декомпенсированной сердечной недостаточностью СД обладает протективным в отношении ЖА действием.
↓
- Итак, помимо того, что СД, является фактором, повышающим заболеваемость ИБС и ухудшающим её течение
- Он также может играть определяющую роль в образовании субстрата для возникновения ЖА;
- И/или может непосредственно провоцировать развитие ЖА.
- В противовес этому, имеются клинические данные за то, что СД является протективным в отношении ЖА фактором (по крайней мере, в определённых группах пациентов).
- Увы, рандомизированных крупномасштабных исследований, которые могли бы предоставить однозначный взгляд на патогенетические взаимоотношения между СД и ЖА до сих пор не проводилось.
Заключение
- ФП и ЖА – наиболее распространённые формы аритмий,
- снижающие качество жизни,
- приводящие к ряду осложнений со стороны сердечно-сосудистой системы,
- повышающие смертность в группе пациентов с СД.
- Доказано, что СД ассоциирован со стояниями, являющимися по своей сути субстратом для возникновения аритмии:
- Структурные и электрические изменения сердца:
- гетерогенность реполяризации предсердий и желудочков,
- обширное поражение миокарда,
- образование рубцовых изменений,
- вегетососудистой дистонии,
- колебания уровня гликемии.
- Структурные и электрические изменения сердца:
- Однако однозначно установить причины, а также патогенетические и электрофизиологические механизмы возможно только при дальнейшем изучении проблемы.

Источник:
- Koektuerk B, Aksoy M, Horlitz M, Bozdag-Turan I, Turan RG. Role of diabetes in heart rhythm disorders. World Journal of Diabetes. 2016;7(3):45-49. doi:10.4239/wjd.v7.i3.45.
: в, диабета, нарушении, ритма, Роль, сахарного, сердечного
Навигация по записям
Источник
Диабетическая кардиомиопатия ‒ это совокупность патологических изменений в сердце, обусловленных метаболическими, сосудистыми и электролитными нарушениями при сахарном диабете. Клиника данного состояния разнообразна ‒ от бессимптомного течения до выраженной сердечной недостаточности с одышкой, отеками, кардиалгией, акроцианозом. Диагностика включает электрокардиографию, эхокардиографию, сцинтиграфию миокарда с таллием-201, функциональные пробы. Лечение комплексное, с обязательной коррекцией уровня глюкозы в крови и применением кардиопротективных средств, препаратов калия, тиазолидиндионов и статинов.
Общие сведения
Диабетическая кардиомиопатия (ДК) выделена как отдельное заболевание в 1973 году. Она может возникать при любом типе сахарного диабета (СД), а также диагностироваться у детей, если при беременности их матери страдали гипергликемией. Нередко это состояние регистрируется спустя 10-15 лет после выявления повышенного уровня сахара. Однако срок развития патологии очень вариабелен, так как зависит от ряда факторов ‒ типа диабета, схемы его лечения, диеты, наличия иных предрасполагающих факторов. По статистике, поражение сердца служит причиной летального исхода примерно у 20-25% больных со стойкой гипергликемией. Но данные цифры часто оспариваются, поскольку четко разграничить причины кардиомиопатии у пациентов с диабетом не всегда удается.
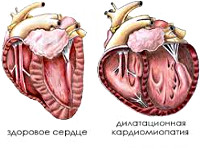
Диабетическая кардиомиопатия
Причины
Недостаточная выработка инсулина (1-й тип СД) или ослабление его воздействия на ткани (2-й тип СД) пагубно влияют на сердечно-сосудистую систему, что является важнейшей причиной развития кардиомиопатии. Существуют определенные предпосылки, увеличивающие вероятность поражения сердца при диабете, обусловленные как внешними, так и внутренними факторами. Это объясняет тот факт, что ДК развивается не у всех больных сахарным диабетом, а только у их части. Выделяют три основные группы причин возникновения данной патологии:
- Нарушение режима лечения и питания. Пренебрежение рекомендациями врача-эндокринолога является наиболее распространенным фактором развития ДК. В случае несоблюдения диеты концентрация глюкозы периодически повышается, что способствует повреждению кардиомиоцитов. Аналогично неправильное использование гипогликемических средств может нарушать микроциркуляцию в тканях сердца, приводя к их ишемии.
- Декомпенсация сахарного диабета. В тяжелых случаях при стойком повышении уровня глюкозы развивается поражение миокарда. Расстройство работы иных органов и систем (например, печени, почек, нейровегетативной системы) опосредованно также приводит к увеличению нагрузки на сердце. Поэтому при прогрессирующем диабете практически всегда возникает ДК, осложняя общую картину заболевания.
- Диабетическая эмбриофетопатия. При наличии у беременной женщины декомпенсированного диабета может поражаться сердце плода – возникает достаточно редкое детское заболевание, характеризующееся врожденной кардиомегалией и аритмией. Это происходит как из-за гипергликемии, так и из-за воздействия инсулина и гипогликемических препаратов на развитие ребенка
Кроме того, сахарный диабет является одним из факторов риска возникновения атеросклероза, поражающего коронарные сосуды. Однако многими авторами ишемическая болезнь сердца, развивающаяся из-за диабета и атеросклероза, не относится к истинной диабетической кардиомиопатии. Редкой причиной ДК выступают также повреждения сердца в результате использования некачественных гипогликемических средств (например, плохо очищенных препаратов инсулина).
Патогенез
В развитии диабетической кардиомиопатии принимают участие три патогенетических механизма – метаболический, ангиопатический и нейровегетативный. Наиболее значим первый вариант ‒ инсулиновая недостаточность приводит к энергетическому дефициту внутри кардиомиоцитов, которые компенсируют его процессами протеолиза и липолиза.
В результате внутри сердечной мышцы происходит накопление продуктов распада липидов и аминокислот, что влечет за собой увеличение выработки NO и других медиаторов воспаления. Кислотно-основное равновесие в тканях смещается к ацидозу, изменяя трансмембранный потенциал и концентрацию неорганических ионов. Это снижает автоматизм и приводит к нарушению проводимости в сердце. Одновременно в тканях увеличивается количество гликозилированных белков и протеогликанов, затрудняющих доставку кислорода к клеткам и усугубляющих недостаток энергии.
Ангиопатический механизм повреждения миокарда при диабете может развиваться как изолированно, так и в сочетании с метаболическими расстройствами. Резкие колебания уровня инсулина стимулируют рецепторы, активизирующие пролиферацию гладкомышечного слоя коронарных сосудов. Это приводит к их сужению и дополнительному снижению перфузии миокарда. Итогом данного процесса является микроангиопатия, осложняющаяся повреждением эндотелия и усугубляющая ишемические явления. Также происходит разрастание аномального коллагена в тканях сердечной мышцы, что изменяет ее плотность и эластичность.
Дистрофия нейровегетативной системы, затрагивающая сердце, возникает на конечных этапах развития ДК. Как правило, прямое поражение кардиомиоцитов и сосудов развивается раньше. В результате гипергликемии, а также диабетического гепатоза (при глубокой декомпенсации сахарного диабета) происходит повреждение вегетативной нервной системы. Ее волокна демиелинизируются, а центры могут повреждаться в результате недостатка глюкозы и кетоацидоза. На этом фоне возникает вагусная денервация сердца, проявляющаяся нарушением ритма его сокращений. Совокупность этих процессов приводит к ишемической болезни, увеличению объема миокарда и в конечном итоге ‒ к сердечной недостаточности.
Классификация
В практической кардиологии выделяют несколько разновидностей диабетической кардиомиопатии, классификация основана на этиологических и патогенетических особенностях заболевания. Несмотря на то, что в развитии патологии задействованы сразу несколько механизмов, обычно один из них выражен сильнее остальных. Знание ведущего сценария патогенеза позволяет специалисту скорректировать лечение для большей его эффективности у конкретного больного. В настоящее время известно три формы ДК:
- Первичная форма. При этом варианте основную роль в поражении миокарда играют метаболические расстройства, связанные с накоплением в тканях продуктов метаболизма жиров и гликозилированных протеинов. Является распространенным видом болезни, но зачастую характеризуется бессимптомным течением и случайно выявляется при обследовании пациента, страдающего сахарным диабетом.
- Вторичная форма. Может возникать изначально или в результате прогрессирования метаболических нарушений. При этом типе поражаются коронарные артериолы, ухудшается микроциркуляция, снижается перфузия, и появляется ишемия миокарда. Некоторые кардиологи относят к этому варианту и коронарный атеросклероз диабетической этиологии.
- Эмбриофетопатический тип. Редкая форма, диагностирующаяся у детей, матери которых страдали от сахарного диабета. Многими специалистами оспаривается отношение данной патологии к диабетической кардиомиопатии.
Симптомы диабетической кардиомиопатии
С момента начала поражения сердца до первых симптомов заболевания может пройти длительное время ‒ от нескольких месяцев до 4-6 лет. Чаще всего больные жалуются на боли в области сердца, напоминающие ишемические ‒ давящее ощущение в левой половине грудной клетки. Однако их выраженность намного слабее, нежели при стенокардии, также не характерна иррадиация в шею, зону лопатки, левую руку. Первоначально кардиалгия появляется после физической нагрузки или пропуска приема инсулина, но в дальнейшем может возникать и в спокойном состоянии. Важным диагностическим признаком является отсутствие реакции на прием нитратов ‒ нитроглицерин не устраняет болевые ощущения.
У части пациентов болевой синдром не развивается, но имеет место одышка, акроцианоз, головокружение ‒ они также возникают как на фоне нагрузок, так и без таковых. Длительность приступа составляет от нескольких минут до 1-3 часов, после чего (на начальных этапах заболевания) кардиальные симптомы ослабевают. При запущенных формах ДК больные указывают на практически постоянную боль в груди, слабость, головокружение и головные боли. Даже самые слабые нагрузки (подъем по лестнице, ускоренный шаг) вызывают сильную одышку, кашель и усиление неприятных ощущений.
Осложнения
При отсутствии лечения, продолжении нарушения пищевого режима, некорригируемой гипергликемии диабетическая кардиомиопатия приводит к нарастающей сердечной недостаточности застойного характера. В результате этого может развиваться кардиогенный отек легких и дистрофия печени. Данные явления значительно усугубляют течение сахарного диабета и угрожают жизни больного. Слабость миокарда также способствует нарушению микроциркуляции, особенно на дистальных участках конечностей, что в комплексе с микроангиопатией ведет к образованию трофических язв и гангрены. Хроническая ишемия миокарда значительно облегчает развитие инфаркта, мелко- и крупноочагового кардиосклероза.
Диагностика
Для успешного лечения диабетической кардиомиопатии важна ранняя диагностика, поскольку это значительно снижает риск осложнений и замедляет прогрессирование патологии. С этой целью больным сахарным диабетом следует регулярно проходить обследование у кардиолога даже при отсутствии субъективных симптомов. В клинической практике используют множество методик, позволяющих дифференцировать ДК от иных сердечно-сосудистых заболеваний и определить тип и стадию болезни для разработки эффективной схемы лечения. Наиболее часто при кардиомиопатии применяют следующие диагностические техники:
- Электрокардиография. Простой и эффективный метод мониторинга сердечной активности и выявления ранних изменений в сердечной мышце. У больных с ДК картина ЭКГ схожа с ишемической болезнью ‒ смещение сегмента ST, сглаживание комплекса QRS, деформация зубца Т. По мере прогрессирования патологии также возможно снижение вольтажа, изменение электрической оси сердца, аритмия.
- Эхокардиография. При ЭхоКГ выявляется утолщение стенок желудочков, увеличение общей массы сердца и изменение плотности миокарда. Одновременно обнаруживается снижение сократительной способности сердечной мышцы и объема выброса крови. При длительном течении патологии возможно увидеть признаки дилатационной кардиомиопатии или очагового кардиосклероза.
- Радиосцинтиграфия. Радионуклидное изучение поступления крови к тканям сердца производится при помощи РФП, содержащих таллий-201. Перфузионная сцинтиграфия миокарда позволяет выявить наиболее ранние признаки коронарной микроангиопатии (вторичной ДК) на основании снижения поступления препарата в миокард. Однако на ранних этапах первичной диабетической кардиомиопатии результаты теста могут быть неоднозначными.
При легких формах заболевания нередко назначают велоэргометрию для обнаружения изменений на ЭКГ в период физических нагрузок, что позволяет уточнить диагноз. Также больным проводится биохимический анализ крови, в рамках которого определяется уровень глюкозы, липопротеидов, сердечных и печеночных ферментов. Коронарография необходима при подозрении на атеросклероз сосудов сердца. Все эти методики позволяют отличить ДК от ишемической болезни и других состояний, прямо не связанных с сахарным диабетом.
Лечение диабетической кардиомиопатии
Терапия этого состояния многокомпонентная и неразрывно связана с лечением основного заболевания ‒ сахарного диабета. Адекватная диета, постоянный контроль уровня сахара в крови, устранение резких скачков уровня инсулина даже без приема сердечных препаратов способны значительно улучшить состояние больного. Но в ряде случаев ДК обнаруживается уже в довольно запущенном состоянии, требующем вмешательства врача-кардиолога. Для замедления прогрессирования и лечения кардиомиопатии при диабете используют следующие группы препаратов:
- Тиазолидиндионы. Эти гипогликемические препараты избирательно замедляют деление гладкомышечных клеток коронарных артериол, препятствуя уменьшению их просвета и ухудшению перфузии миокарда. Однако их допустимо использовать лишь при доказанном поражении микроциркуляторной сети сердца – в редких случаях они могут вызывать кардиопатическое воздействие, причины которого неясны.
- Препараты калия. При ДК следствием метаболических расстройств является нехватка ионов калия в кардиомиоцитах. Его дефицит также может быть обусловлен повышенным диурезом, что нередко наблюдается при диабете, нарушением диеты, приемом некоторых лекарств. Препараты калия пополняют количество микроэлемента в организме, нормализуя электролитный состав и мембранный потенциал клеток миокарда.
- Статины. У ряда больных наблюдается гиперлипидемия, которая повышает риск развития атеросклероза, осложняющего течение кардиомиопатии. Данные средства, например, аторвастатин, снижают уровень опасных ЛПНП, а также способствуют элиминации из тканей сердца продуктов расщепления жиров. В долгосрочной перспективе использование статинов увеличивает продолжительность жизни больных диабетом и резко уменьшает риск инфарктов и инсультов.
- Бета-адреноблокаторы. Их назначают при выраженных ишемических изменениях в миокарде или развитии тахиаритмии. Они снижают частоту сердечных сокращений и уменьшают потребность миокарда в кислороде, улучшая его метаболизм. Особенно актуально использование бета-блокаторов при дистрофии вегетативных нервов, которые в норме способствуют снижению частоты сердечных сокращений.
По показаниям могут применяться различные гипогликемические средства (особенно при диабете 2-го типа), ингибиторы АПФ, блокаторы кальциевых каналов, антиоксиданты. При наличии застойной сердечной недостаточности и развитии отеков назначают диуретические препараты с постоянным контролем ионного состава плазмы крови. В качестве поддерживающего лечения при сложных формах кардиомиопатии используют сердечные гликозиды.
Прогноз и профилактика
Прогностические перспективы диабетической кардиомиопатии тесно связаны с течением основного заболевания. При адекватной гипогликемической терапии, включающей как прием препаратов, так и образ жизни больного, скорость прогрессирования патологии существенно замедляется, а использование кардиопротективных средств помогает устранить кардиальные симптомы. В то же время, игнорирование болезни и пренебрежение к пищевому режиму на фоне сахарного диабета может привести к тяжелой сердечной недостаточности.
Профилактика ДК сводится к недопущению повышения уровня глюкозы и предотвращению развития декомпенсации диабета, регулярному наблюдению у эндокринолога. Особенно важно соблюдать эти правила беременным женщинам ‒ их дети могут получить внутриутробное поражение сердца.
Источник
