Что такое манифестация сахарного диабета
Сахарный диабет 1 типа – это эндокринное заболевание, характеризующееся недостаточным производством инсулина и повышением уровня глюкозы в крови. Из-за продолжительной гипергликемии пациенты страдают от жажды, теряют вес, быстро утомляются. Характерны мышечные и головные боли, судороги, кожный зуд, усиление аппетита, частые мочеиспускания, бессонница, приливы жара. Диагностика включает клинический опрос, лабораторные исследования крови и мочи, выявляющие гипергликемию, недостаток инсулина, метаболические нарушения. Лечение проводится методом инсулинотерапии, назначается диета, занятия физической культурой.
Общие сведения
Термин «диабет» происходит из греческого языка и означает «течет, вытекает», таким образом, название болезни описывает один из ее ключевых симптомов – полиурию, выделение большого количества мочи. Сахарный диабет 1 типа называют также аутоиммунным, инсулинозависимым и ювенильным. Заболевание может проявиться в любом возрасте, но чаще манифестирует у детей и подростков. В последние десятилетия отмечается рост эпидемиологических показателей. Распространенность всех форм сахарного диабета составляет 1-9%, на долю инсулинозависимого варианта патологии приходится 5-10% случаев. Заболеваемость зависит от этнической принадлежности пациентов, наиболее высока среди скандинавских народов.

Сахарный диабет 1 типа
Причины СД 1 типа
Факторы, способствующие развитию болезни, продолжают исследоваться. К настоящему времени установлено, что сахарный диабет первого типа возникает на основе сочетания биологической предрасположенности и внешних неблагоприятных воздействий. К наиболее вероятным причинам поражения поджелудочной железы, снижения выработки инсулина относят:
- Наследственность. Склонность к инсулинозависимому диабету передается по прямой линии – от родителей к детям. Выявлено несколько комбинаций генов, предрасполагающих к болезни. Они наиболее распространены среди жителей Европы и Северной Америки. При наличии больного родителя риск для ребенка увеличивается на 4-10% по сравнению с общей популяцией.
- Неизвестные внешние факторы. Существуют некие воздействия среды, провоцирующие СД 1 типа. Этот факт подтверждается тем, что однояйцевые близнецы, имеющие абсолютно одинаковый набор генов, заболевают вместе лишь в 30-50% случаев. Также установлено, что люди, мигрировавшие с территории с низкой заболеваемостью на территорию с более высокой эпидемиологией, чаще болеют диабетом, чем те, кто отказался от миграции.
- Вирусная инфекция. Аутоиммунный ответ на клетки поджелудочной может быть запущен вирусной инфекцией. Наиболее вероятно влияние вирусов Коксаки и краснухи.
- Химикаты, лекарства. Бета-клетки железы, производящей инсулин, могут быть поражены некоторыми химическими средствами. Примерами таких соединений являются крысиный яд и стрептозоцин – препарат для онкологических больных.
Патогенез
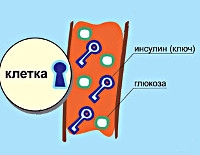
В основе патологии лежит недостаточность производства гормона инсулина в бета-клетках островков Лангерганса поджелудочной железы. К инсулинозависимым тканям относятся печеночная, жировая и мышечная. При сокращении секреции инсулина они перестают принимать глюкозу из крови. Возникает состояние гипергликемии – ключевой признак сахарного диабета. Кровь сгущается, нарушается кровоток в сосудах, что проявляется ухудшением зрения, трофическими поражениями конечностей.
Недостаточность инсулина стимулирует распад жиров и белков. Они поступают в кровь, а затем метаболизируются печенью в кетоны, которые становятся источниками энергии для инсулиннезависимых тканей, включая ткани головного мозга. Когда концентрация сахара крови превышает 7-10 ммоль/л, активизируется запасной путь выведения глюкозы – через почки. Развивается глюкозурия и полиурия, вследствие чего возрастает риск дегидратации организма и дефицита электролитов. Для компенсации потери воды усиливается чувство жажды (полидипсия).
Классификация
Согласно рекомендациям Всемирной организации здравоохранения, сахарный диабет I типа подразделяют на аутоиммунный (спровоцированный выработкой антител к клеткам железы) и идиопатический (органические изменения в железе отсутствуют, причины патологии остаются неизвестными). Развитие болезни происходит в несколько стадий:
- Выявление предрасположенности. Проводятся профилактические обследования, определяется генетическая отягощенность. С учетом средних статистических показателей по стране рассчитывается уровень риска развития заболевания в будущем.
- Начальный пусковой момент. Включаются аутоиммунные процессы, повреждаются β-клетки. Антитела уже вырабатываются, но производство инсулина остается нормальным.
- Активный хронический аутоиммунный инсулит. Титр антител становится высоким, количество клеток, производящих инсулин, сокращается. Определяется высокий риск манифестации СД в ближайшие 5 лет.
- Гипергликемия после углеводной нагрузки. Деструкции подвергается значительная часть вырабатывающих инсулин клеток. Производство гормона уменьшается. Сохраняется нормальный уровень глюкозы натощак, но после приема пищи в течение 2 часов определяется гипергликемия.
- Клиническая манифестация болезни. Проявляются симптомы, характерные для сахарного диабета. Секреция гормона резко снижена, деструкции подвержено 80-90% клеток железы.
- Абсолютная инсулиновая недостаточность. Все клетки, ответственные за синтез инсулина, погибают. Гормон поступает в организм только в форме препарата.
Симптомы СД 1 типа
Основные клинические признаки манифестации заболевания – полиурия, полидипсия и потеря веса. Учащаются позывы к мочеиспусканию, объем суточной мочи достигает 3-4 литров, иногда появляется ночное недержание. Пациенты испытывают жажду, ощущают сухость во рту, выпивают до 8-10 литров воды за сутки. Аппетит усиливается, но масса тела уменьшается на 5-12 кг за 2-3 месяца. Дополнительно может отмечаться бессонница ночью и сонливость днем, головокружения, раздражительность, быстрая утомляемость. Больные чувствуют постоянную усталость, с трудом выполняют привычную работу.
Возникает зуд кожи и слизистых оболочек, высыпания, изъязвления. Ухудшается состояние волос и ногтей, долго не заживают раны и иные кожные поражения. Нарушение кровотока в капиллярах и сосудах называется диабетической ангиопатией. Поражение капилляров проявляется снижением зрения (диабетическая ретинопатия), угнетением функций почек с отеками, артериальной гипертензией (диабетическая нефропатия), неравномерным румянцем на щеках и подбородке. При макроангиопатии, когда в патологический процесс вовлекаются вены и артерии, начинает прогрессировать атеросклероз сосудов сердца и нижних конечностей, развивается гангрена.
У половины больных определяются симптомы диабетической нейропатии, которая является результатом электролитного дисбаланса, недостаточного кровоснабжения и отека нервной ткани. Ухудшается проводимость нервных волокон, провоцируются судороги. При периферической нейропатии пациенты жалуются на жжение и болезненные явления в ногах, особенно по ночам, на ощущение «мурашек», онемение, повышенную чувствительность к прикосновениям. Для автономной нейропатии характерны сбои со стороны функций внутренних органов – возникают симптомы расстройств пищеварения, пареза мочевого пузыря, мочеполовых инфекций, эректильной дисфункции, стенокардии. При очаговой нейропатии формируются боли различной локализации и интенсивности.
Осложнения
Продолжительное нарушение углеводного обмена может привести к диабетическому кетоацидозу – состоянию, характеризующемуся накоплением в плазме кетонов и глюкозы, повышением кислотности крови. Протекает остро: исчезает аппетит, появляется тошнота и рвота, боль в животе, запах ацетона в выдыхаемом воздухе. При отсутствии медицинской помощи наступает помрачение сознания, кома и смерть. Больные с признаками кетоацидоза нуждаются в неотложном лечении. Среди других опасных осложнений диабета – гиперосмолярная кома, гипогликемическая кома (при неправильном применении инсулина), «диабетическая стопа» с риском ампутации конечности, тяжелая ретинопатия с полной потерей зрения.
Диагностика
Обследование пациентов осуществляет врач-эндокринолог. Достаточными клиническими критериями болезни являются полидипсия, полиурия, изменения веса и аппетита – признаки гипергликемии. В ходе опроса врач также уточняет наличие наследственной отягощенности. Предполагаемый диагноз подтверждается результатами лабораторных исследований крови, мочи. Обнаружение гипергликемии позволяет различить сахарный диабет с психогенной полидипсией, гиперпаратиреозом, хронической почечной недостаточностью, несахарным диабетом. На втором этапе диагностики проводится дифференциация различных форм СД. Комплексное лабораторное обследование включает следующие анализы:
- Глюкоза (кровь). Определение сахара выполняется трехкратно: с утра натощак, через 2 часа после нагрузки углеводами и перед сном. О гипергликемии свидетельствуют показатели от 7 ммоль/л натощак и от 11,1 ммоль/л после употребления углеводной пищи.
- Глюкоза (моча). Глюкозурия указывает на стойкую и выраженную гипергликемию. Нормальные значения для данного теста (в ммоль/л) – до 1,7, пограничные – 1,8-2,7, патологические – более 2,8.
- Гликированный гемоглобин. В отличие от свободной, несвязанной с белком глюкозы, количество гликозилированного гемоглобина крови остается относительно постоянным на протяжении суток. Диагноз диабета подтверждается при показателях 6,5% и выше.
- Гормональные тесты. Проводятся тесты на инсулин и С-пептид. Нормальная концентрация иммунореактивного инсулина крови натощак составляет от 6 до 12,5 мкЕД/мл. Показатель С-пептида позволяет оценить активность бета-клеток, объем производства инсулина. Нормальный результат – 0,78-1,89 мкг/л, при сахарном диабете концентрация маркера снижена.
- Белковый метаболизм. Выполняются анализы на креатинин и мочевину. Итоговые данные дают возможность уточнить функциональные возможности почек, степень изменения белкового обмена. При поражении почек показатели выше нормы.
- Липидный метаболизм. Для раннего выявления кетоацидоза исследуется содержание кетоновых тел в кровотоке, моче. С целью оценки риска атеросклероза определяется уровень холестеринов крови (общий холестерин, ЛПНП, ЛПВП).
Лечение СД 1 типа
Усилия врачей нацелены на устранение клинических проявлений диабета, а также на предупреждение осложнений, обучение пациентов самостоятельному поддержанию нормогликемии. Больных сопровождает полипрофессиональная бригада специалистов, в которую входят эндокринологи, диетологи, инструктора ЛФК. Лечение включает консультации, применение лекарственных средств, обучающие занятия. К основным методам относятся:
- Инсулинотерапия. Использование препаратов инсулина необходимо для максимально достижимой компенсации метаболических нарушений, предотвращения состояния гипергликемии. Инъекции являются жизненно необходимыми. Схема введения составляется индивидуально.
- Диета. Пациентам показана низкоуглеводная, в том числе кетогенная диета (кетоны служат источником энергии вместо глюкозы). Основу рациона составляют овощи, мясо, рыба, молочные продукты. В умеренных количествах допускаются источники сложных углеводов – цельнозерновой хлеб, крупы.
- Дозированные индивидуальные физические нагрузки. Физическая активность полезна большинству больных, не имеющих тяжелых осложнений. Занятия подбираются инструктором по ЛФК индивидуально, проводятся систематически. Специалист определяет продолжительность и интенсивность тренировок с учетом общего состояния здоровья пациента, уровня компенсации СД. Назначается регулярная ходьба, легкая атлетика, спортивные игры. Противопоказан силовой спорт, марафонский бег.
- Обучение самоконтролю. Успешность поддерживающего лечения при диабете во многом зависит от уровня мотивации больных. На специальных занятиях им рассказывают о механизмах болезни, о возможных способах компенсации, осложнениях, подчеркивают важность регулярного контроля количества сахара и применения инсулина. Больные осваивают навык самостоятельного выполнения инъекции, выбора продуктов питания, составления меню.
- Профилактика осложнений. Применяются лекарства, улучшающие ферментную функцию железистых клеток. К ним относятся средства, способствующие оксигенации тканей, иммуномодулирующие препараты. Проводится своевременное лечение инфекций, гемодиализ, антидот-терапия для выведения соединений, ускоряющих развитие патологии (тиазидов, кортикостероидов).
Среди экспериментальных методов лечения стоит отметить разработку ДНК-вакцины BHT-3021. У пациентов, получавших внутримышечные инъекции в течение 12 недель, повышался уровень C-пептида – маркера активности островковых клеток поджелудочной железы. Другое направление исследований – превращение стволовых клеток в железистые клетки, производящие инсулин. Проведенные опыты на крысах дали положительный результат, но для использования метода в клинической практике необходимы доказательства безопасности процедуры.
Прогноз и профилактика
Инсулинозависимая форма сахарного диабета является хроническим заболеванием, но правильная поддерживающая терапия позволяет сохранить высокое качество жизни больных. Профилактические меры до сих пор не разработаны, так как не выяснены точные причины болезни. В настоящее время всем людям из групп риска рекомендовано проходить ежегодные обследования для выявления заболевания на ранней стадии и своевременного начала лечения. Такая мера позволяет замедлить процесс формирования стойкой гипергликемии, минимизирует вероятность осложнений.
Описаны два клинических случая спровоцированного вирусной инфекцией тяжелого манифеста сахарного диабета 1 типа с развитием кетоацидотической комы, поражением центральной нервной системы, потерей зрения, геморрагическим инсультом, острой почечной недостаточностью. Своевременно назначенная комплексная терапия позволила добиться улучшения состояния обоих детей дошкольного возраста и избежать летального исхода.

Таблица. Триггеры сахарного диабета 1 типа
Сахарный диабет (СД) – заболевание обмена веществ различной этиологии, которое характеризуется хронической гипергликемией, возникающей в результате нарушения секреции или действия инсулина либо обоих факторов одновременно (определение ISPAD, 2000) [1, 2]. Это наиболее распространенное из всех эндокринных заболеваний, число больных которым с каждым годом увеличивается. В 1994 г. на планете было зарегистрировано 110,4 млн больных СД, к 2006 г. их количество увеличилось более чем вдвое и составило 230 млн, а по прогнозам на 2025 г. достигнет 350 млн. Ежегодный прирост вновь выявленных случаев заболевания составляет 6-10%, это число удваивается каждые 10-15 лет [3].
В Москве распространенность СД 1 типа составляет 5,6 на 1000 населения, что более чем в 6 раз ниже, чем в Финляндии (35,5 на 1000). По данным регистра Московской области, распространенность СД 1 типа составляет 50,8 на 100 тыс. детского населения, при этом возрастные пики приходятся на 3-6 и 10-14 лет. СД представляет собой неоднородную группу заболеваний, различных по этиологии, патогенезу, клиническому течению и подходам к терапии. В соответствии с классификацией Всемирной организации здравоохранения (ВОЗ, 1995) выделяют две основные формы СД:
- инсулинзависимый сахарный диабет – СД 1 типа;
- инсулиннезависимый сахарный диабет – СД 2 типа.
В происхождении СД 1 типа, удельный вес которого в общей структуре заболеваемости СД не превышает 10-15%, ведущую роль играют аутоиммунные механизмы повреждения эндокринной ткани поджелудочной железы, индуцированные вирусной инфекцией на фоне нарушений иммунитета, которые приводят к гибели бета-клеток, абсолютному дефициту инсулина и нарушению утилизации глюкозы. Представление о СД 1 типа как об аутоиммунном заболевании сформировалось в 1970-е гг., когда были обнаружены антитела к антигенам бета-клеток и открыто явление аутоиммунной агрессии против клеток поджелудочной железы, в котором участвуют как клеточные, так и гуморальные звенья иммунитета. Несколько позже были получены данные об ассоциации СД 1 типа с антигенами системы HLA (human leukocyte antigens – лейкоцитарные антигены человека), которые участвуют в регуляции иммунного ответа. Трансплантация поджелудочной железы больному СД от здорового монозиготного близнеца привела к 6-7-месячной полной ремиссии заболевания, которая затем вновь сменилась рецидивом диабета. При биопсии трансплантата была обнаружена селективная деструкция островковых клеток. Все это позволило сделать вывод об аутоиммунной природе СД 1 типа [1].
Несмотря на большое число исследований, патогенез СД 1 типа во многом неясен. В настоящее время преобладает концепция об участии триггеров, которые индуцируют аутоиммунные процессы (табл.).
Клинические проявления заболевания зависят от возраста ребенка и длительности течения СД 1 типа. Для детей младшего возраста характерно острое начало, с быстрым нарастанием симптоматики до развития кетоацидоза и, в отсутствие своевременной диагностики, кетоацидотической комы. У детей среднего и старшего возраста заподозрить СД 1 типа можно по основным симптомам: полиурии, полидипсии, полифагии, снижению массы тела, запаху ацетона в выдыхаемом воздухе. При развитии симптоматики СД 1 типа отмечаются повышение уровня гликемии крови выше 11,1 ммоль/л, глюкозурия, кетонурия. Определение уровня С-пептида в сыворотке крови позволяет оценить функциональное состояние бета-клеток. Базальный уровень С-пептида у здоровых детей составляет 0,28-1,32 пг/мл. При СД 1 типа его уровень значительно снижен. Определение гликированного гемоглобина является одним из основных методов диагностики степени компенсации углеводного обмена.
Сахарный диабет 1 типа – заболевание, в основе которого лежит абсолютная инсулиновая недостаточность, обусловленная аутоиммунным разрушением клеток поджелудочной железы, продуцирующих инсулин. В настоящее время введение инсулина является единственным патогенетическим методом его лечения. Отсутствие собственного инсулина у больных СД 1 типа обусловливает назначение инсулиновых препаратов для замещения физиологической секреции гормона. Для этого используются человеческие генноинженерные препараты инсулина: комбинация пролонгированного инсулина в двух инъекциях и короткого инсулина не менее трех инъекций.
Препараты инсулина по длительности действия можно разделить на три группы – инсулины короткого действия, пролонгированные препараты инсулина и комбинированные препараты, состоящие из инсулина короткого и пролонгированного действия. Инсулины короткого действия имитируют эндогенную быструю секрецию инсулина в ответ на прием пищи. Пролонгированные инсулины замещают базальную секрецию инсулина и обеспечивают поддержание стабильной гликемии ночью и в периоды между приемами пищи. Комбинированные препараты, соответственно, обладают свойствами обоих типов.
В современной диабетологии, за более чем 90-летний период применения, достигнут большой прогресс в понимании особенностей и механизмов действия инсулина. Однако отличный от физиологического путь введения экзогенного инсулина порождает целый ряд проблем. Это несвоевременное поступление в организм и дефицит инсулина в печени, периферическая гиперинсулинемия, дефицит гликогена в печени, активация липолиза, глюконеогенеза, жировой гепатоз и высокий риск развития гипогликемий. Препараты инсулина отличаются по своим характеристикам – времени начала, пика и окончания действия, не соответствующим физиологическому ритму секреции этого гормона. Короткие инсулины действуют дольше необходимого времени и требуют «перекуса» между основными приемами пищи [4].
Решить этот вопрос позволило создание и внедрение в практику инсулинов ультракороткого действия, наиболее приближенного к нормальной физиологической секреции инсулина. С 1995 г. используется аналог инсулина лизпро, несколько позже появились еще два препарата с ультракороткой активностью – инсулин аспарт и инсулин глулизин. Длительность действия ультракоротких инсулинов обусловлена скоростью их всасывания из места инъекции. Короткие инсулины состоят из шести молекул – гексамеров. Вследствие этого введенный инсулин медленно всасывается. Бóльшая часть молекул ультракороткого инсулина находится в виде мономеров, чем и объясняется их быстрое всасывание. При их использовании облегчается возможность синхронизации пика действия парентерально введенного инсулина с пиком постпрандиальной гликемии. Однако назначение даже самых современных препаратов инсулина не решает проблему достижения компенсации СД. Лечение должно быть комплексным и включать следующие компоненты:
- инсулинотерапию;
- диету;
- физические нагрузки;
- самоконтроль;
- психологическую помощь (для достижения комплаентности пациента) [5].
Каждый из этих факторов является важной составляющей реабилитационных мероприятий. При нестабильном течении СД могут развиваться осложнения: диабетический кетоацидоз и кетоацидотическая кома, диабетическая полинейропатия, прогрессирующие ангиопатии (ретино-, нефропатия). В дебюте СД 1 типа на фоне гипергликемии и инсулиновой недостаточности прогрессируют явления кетоацидоза, сопровождающиеся дегидратацией, гиповолемией и электролитными нарушениями. Это приводит к снижению системного артериального давления и уменьшению перфузии в жизненно важных органах (головной мозг, сердце, почки). Критическое снижение почечного кровотока вызывает развитие острой почечной недостаточности. В патогенезе поражения центральной нервной системы при диабетическом кетоацидозе ведущую роль играет дегидратация нейронов головного мозга на фоне гиперосмолярности плазмы. Клинически это проявляется разнообразными неврологическими нарушениями, как общемозговыми (сопор, кома), так и очаговыми.
Ниже представлены два клинических случая развития ранних и поздних осложнений сахарного диабета 1 типа в дебюте заболевания. Ранний возраст детей, тяжесть течения, наличие множественных осложнений обусловливали необходимость назначения индивидуальных схем инсулинотерапии на всех этапах наблюдения за детьми (реанимационное отделение, педиатрическое отделение, поликлиника).
Больная П., 2007 г.р., поступила по экстренным показаниям в детское реанимационное отделение Московского областного научно-исследовательского клинического института им. М.Ф. Владимирского (МОНИКИ) 3 октября 2012 г. в крайне тяжелом состоянии с манифестом СД 1 типа. Больна с сентября 2012 г., когда на фоне острой вирусной инфекции появились жажда, полиурия, потеря массы тела, боли в животе. Была осмотрена участковым педиатром, назначено симптоматическое лечение. Состояние ребенка ухудшалось, и 24 сентября 2012 г. ребенок госпитализирован в детское соматическое отделение по месту жительства с диагнозом «острый фаринготрахеит, гастрит». Однако 26 сентября 2012 г. при обследовании выявлена гипергликемия до 12,3 ммоль/л. Состояние ребенка на фоне лечения (антибактериальная терапия, симптоматическая терапия, инфузионная терапия) – с отрицательной динамикой. С 30 сентября 2012 г. отмечено резкое ухудшение состояния: бледность, вялость, заторможенность, сопор. В этот же день девочка в тяжелом состоянии (уровень гликемии 16-19 ммоль/л) переводится в реанимационное отделение по месту жительства, где установлен диагноз сахарного диабета 1 типа, начата инсулинотерапия. На фоне проводимой терапии 2 октября 2012 г. отмечалась остановка сердечной деятельности и дыхания, судорожный синдром. Уровень гликемии колебался в пределах 3,7-36 ммоль/л, а 3 октября 2012 г. в крайне тяжелом состоянии с диагнозом «сахарный диабет, 1 тип, впервые выявленный, стадия декомпенсации, тяжелое течение; кетоацидотическая кома» девочка переведена в детское реанимационное отделение МОНИКИ для дальнейшего лечения.
При поступлении – без сознания, на искусственной вентиляции легких. Гипергликемическая кома I. Отек головного мозга. Лихорадка. Кожные покровы субиктеричные. Отмечается пастозность лица, передней брюшной стенки, нижних конечностей. В легких ослабление дыхания слева. Пульс 98 уд/мин. Артериальное давление 90/60 мм рт. ст. Тоны сердца приглушены, ритмичные. Живот мягкий, вздут. Печень + 2,0 см из-под края реберной дуги, селезенка + 1,0 см. В анализе крови лейкоцитоз до 24,8 × 109/л, общий белок 57 г/л, креатинин 252 мкмоль/л, креатинкиназа 869 Ед/л, альфа-амилаза 362 Ед/л, С-реактивный белок (СРБ) 41,6 мг/л. Уровень гликемии при поступлении – 47,7 ммоль/л. На рентгенограмме органов грудной клетки – признаки левосторонней пневмонии. По данным электрокардиограммы (ЭКГ) выявлена субэндокардиальная ишемия миокарда левого желудочка, при ультразвуковом исследовании (УЗИ) органов брюшной полости обнаружены камни в желчном пузыре, вторичные изменения поджелудочной железы.
На 7-е сутки пребывания в отделении на фоне стабилизации состояния у девочки отмечалась полная потеря зрения. В экстренном порядке проведено обследование: транскраниальное дуплексное сканирование сосудов головного мозга – без патологии. По данным рентгеновской компьютерной томографии (РКТ) и магнитно-резонансной томографии (МРТ) головного мозга отек и абсцесс головного мозга не выявлены, но в левой лобной доле обнаружен небольшой участок накопления контрастного вещества (очаг ишемии). Консультирована неврологом, диагностирована дисциркуляторно-дисметаболическая полинейропатия с хиазмальным синдромом, окулистом – амавроз на фоне гипоксического поражения центральной нервной системы, кардиологом – миокардиодистрофия, детским хирургом – желчнокаменная болезнь.
Клинический диагноз – «Сахарный диабет, 1 тип, впервые выявленный, стадия декомпенсации, тяжелое течение. Кетоацидотическая кома. Энцефалопатия смешанного генеза (дисметаболическая, дисциркуляторная). Задняя ишемическая нейропатия обоих глаз. Хиазмальный синдром. Отек головного мозга. Миокардиодистрофия. Септицемия. Левосторонняя пневмония, дыхательная недостаточность II ст. Токсико-метаболическая нефропатия. Инфекция мочевыводящих путей. Желчнокаменная болезнь (конкременты желчного пузыря). Вторичные реактивные изменения поджелудочной железы». Проводимая терапия:
- Инсулинотерапия: внутривенное капельное, далее подкожное введение инсулина ультракороткого действия НовоРапид (0,65 Ед/кг) и пролонгированного действия Левемир (0,3 Ед/кг).
- Массивная антибактериальная терапия (Зивокс, Цефтриаксон, Амикацин).
- Противовирусная и противогрибковая терапия.
- Симптоматическая терапия: внутривенные инфузии, Урсосан, ферменты, биопрепараты, Панангин, иммуномодуляторы, антидепрессанты, физиолечение, гипербарическая оксигенация.
Состояние девочки значительно улучшилось: стабилизировался уровень гликемии, нормализовались лабораторные показатели, восстановилось зрение. С рекомендациями по дальнейшему лечению пациентка была выписана домой под наблюдение детского эндокринолога по месту жительства.
Клинический случай 2
Больная М., 2007 г.р., поступила по экстренным показаниям в детское реанимационное отделение МОНИКИ 7 ноября 2012 г. в крайне тяжелом состоянии с диагнозом «сахарный диабет 1 типа, впервые выявленный; кетоацидотическая кома; отек головного мозга; острая почечная недостаточность». Больна с октября 2012 г., когда появились жажда, полиурия, потеря массы тела, боли в животе, одышка. Участковым педиатром госпитализирована в соматическое отделение по месту жительства с манифестом СД 1 типа. В связи с прогрессирующим ухудшением состояния переведена сначала в реанимационное отделение по месту жительства, а затем в детское реанимационное отделение МОНИКИ.
Состояние при поступлении в МОНИКИ крайне тяжелое. Без сознания. На искусственной вентиляции легких. Гипергликемическая кома III. Отек головного мозга. Лихорадка. Отмечается выраженная отечность лица, век, рук, передней брюшной стенки, нижних конечностей. Кожные покровы субиктеричные. В легких ослабление дыхания с обеих сторон. Пульс 102 уд/мин. Артериальное давление 115/60 мм рт. ст. Тоны сердца приглушены, ритмичные. Живот мягкий, вздут. Печень + 5,0 см из-под края реберной дуги, селезенка + 2,0 см. Анурия. В анализе крови лейкоцитоз до 13,7 × 109/л, общий белок 51 г/л, креатинин 279 мкмоль/л, мочевина 24,1 ммоль/л, мочевая кислота 855 мкмоль/л, СРБ 27,36 мг/л. Уровень гликемии при поступлении – 27 ммоль/л.
На рентгенограмме органов грудной клетки – признаки двустороннего пневмоторакса, двусторонней пневмонии. При МРТ головного мозга в задних отделах мозга определяются множественные очаги и участки геморрагии, больше справа, асимметрия диаметров и интенсивности МР-сигнала от сегментов передних мозговых артерий. При УЗИ органов брюшной полости выявлены камни желчного пузыря, гепатомегалия, вторичные изменения поджелудочной железы. На 21-е сутки пребывания в отделении на фоне стабилизации состояния у пациентки отмечалась полная потеря зрения. Ребенок наблюдался неврологом, офтальмологом, детским хирургом.
Клинический диагноз – «Сахарный диабет, 1 тип, впервые выявленный, стадия декомпенсации, тяжелое течение. Кетоацидотическая кома. Энцефалопатия смешанного генеза (дисметаболическая, дисциркуляторная). Геморрагический инсульт в бассейне задних мозговых артерий. Правосторонний гемипарез. Отек головного мозга. Задняя ишемическая нейропатия обоих глаз. Острая почечная недостаточность. Двусторонняя пневмония. Двусторонний пневмоторакс, дыхательная недостаточность III ст. Желчнокаменная болезнь (конкременты желчного пузыря). Вторичные реактивные изменения поджелудочной железы. Трофические нарушения мягких тканей головы и нижних конечностей. Множественный кариес. Герпетическая инфекция».
Ребенку на фоне инсулинотерапии проводилось внутривенное капельное введение инсулина, а далее подкожное введение инсулина ультракороткого действия НовоРапид (0,7 Ед/кг) и пролонгированного действия Левемир (0,5 Ед/кг), проводилась массивная антибактериальная терапия, включающая такие препараты, как Зивокс, Цефтриаксон, Амикацин, Меронем, Метрогил; противовирусная, противогрибковая, инфузионная терапия, симптоматическая терапия Урсосаном, препаратами ферментов, биопрепаратами, Панангином, иммуномодуляторами, физиолечение. Проведено 5 сеансов заместительной почечной терапии (ультрафильтрация). Состояние девочки улучшилось, восстановилось зрение, стабилизировался уровень гликемии, разрешилась пневмония, на контрольном МРТ-исследовании головного мозга отмечалась положительная динамика.
Приведенные клинические примеры демонстрируют тяжелый манифест СД 1 типа с развитием кетоацидотической комы, поражением центральной нервной системы, потерей зрения, геморрагическим инсультом, развитием острой почечной недостаточности. В обоих случаях дебют сахарного диабета был спровоцирован вирусной инфекцией. Индивидуальная комплексная терапия, вовремя назначенная, позволила добиться улучшения состояния этих детей и избежать летального исхода.
