Касаткина сахарный диабет 1 типа
В последние годы во всем мире, в том числе и в нашей стране, отмечается выраженная тенденция к росту заболеваемости сахарным диабетом 1 типа именно в данной возрастной группе. Все чаще заболевают дети на первом и втором году жизни. Эти дети проживут практически всю свою жизнь с сахарным диабетом. Следовательно, мы (врачи и родители) с первых дней заболевания должны быть озабочены тем, чтобы эти дети могли прожить, без специфических осложнений сахарного диабета, долгую и активную жизнь.
Первая задача, которую мы должны решить, – понять причину нестабильного течения заболевания у таких малышей и научиться, несмотря на возрастные особенности, добиваться стабильного течения заболевания. Задача очень сложная, но ее вполне можно решить совместными усилиями врачей и семьи.
Основная причина нестабильного течения заболевания в этом возрастном периоде – склонность к развитию гипогликемических состояний. Более того, гипогликемии у детей младшего возраста, как правило, не распознаются («нераспознанные» гипогликемии).
Последствием «нераспознанной» гипогликемии являются постгипогликемическая гипергликемия и, в связи с этим, – значительная вариабельность суточной гликемии и нестабильное течение заболевания. В этом возрасте основной причиной частых гипогликемий является высокая чувствительность к инсулину Основная же причина того обстоятельства, что гипогликемии у детей данного возраста в подавляющем большинстве случаев не распознаются, – незрелость мозга.
С целью понимания механизма формирования «нераспознанной» гипогликемии и тяжелых последствий подобных гипогликемий необходимо владеть информацией о характере реакции зрелого мозга и особенностях реакции мозга ребенка младшего возраста (незрелый мозг) на снижение уровня гликемии.
Реакция зрелого мозга на гипогликемию В ответ на снижение уровня гликемии и, как следствие, – голодание мозга, включается механизм контррегуляции, т.е.
- повышается уровень контринсулиновых гормонов (глюкагон, адреналин и др.), способствующих выходу глюкозы из печени с целью нормализации уровня сахара крови. В ответ на голодание мозга и повышение уровня адреналина в крови формируются клинические (узнаваемые) симптомы гипогликемии: неадекватное поведение, сонливость, страх, потливость, бледность кожных покровов, учащение пульса, повышение артериального давления, тремор пальцев рук и туловища.
Появление клинических симптомов гипогликемии заставляет больного (окружающих) принять соответствующие меры: исследовать уровень гликемии, принять дополнительную порцию углеводов. Таким образом, опасность дальнейшего снижения уровня гликемии ликвидируется.
У маленьких детей мозг, в силу его незрелости, не в состоянии распознать гипогликемию и, как следствие,
- не запускается механизм контррегуляции;
- не формируются клинические симптомы гипогликемии.
Отсутствие характерных симптомов гипогликемии является причиной бездействия окружающих: не исследуется уровень гликемии, не принимаются меры по повышению уровня гликемии.
Только в тех случаях, когда гипогликемия достигает опасного для жизни уровня, у большинства детей срабатывает механизм контррегуляции и повышается уровень гликемии. Однако, как правило, уровень подобной гликемии значительно превышает нормальные показатели постгипогликемическая гипергликемия. Нередко цифры гликемии достигают очень высоких значений (25-30 ммоль/л). При этом обращает на себя внимание, что общее состояние ребенка, как правило, не соответствует инсулинодефицитному характеру гипергликемии: больной не предъявляет жалобы и не имеет симптомов, характерных для подобной гипергликемии.
Постгипогликемическая гипергликемия, даже после единственной «нераспознанной» гипогликемии, может держаться в течение нескольких часов, а иногда и нескольких дней. Это позволяет окружающим считать гипергликемию инсулинодефицитной и наращивать дозу инсулина.
Подобная терапевтическая тактика не улучшает показатели гликемии и, напротив, – значительно ухудшает течение заболевания. Длительно завышенная доза инсулина приводит к серийному характеру «нерас- познанных» гипогликемий и, как следствие, – к длительному характеру постгипогликемической гипергликемии. Ежедневные исследования гликемии (несколько раз в день), как правило, не позволяют выявить гипогликемию.
Лишь суточное мониторирование глюкозы крови каждые 5 минут довольно часто выявляет гипогликемический уровень гликемии или выраженное падение уровня гликемии и, как следствие, – длительное значительное повышение уровня глюкозы крови.
Длительный характер лечения избыточными дозами инсулина может сопровождаться клиническими симптомами хронической передозировки инсулина: течение сахарного диабета становится крайне нестабильным, резко повышается аппетит, имеет место прибавка в весе, непереносимость физических нагрузок, повышенная раздражительность, склонность к депрессивным состояниям.
Итак, причины нестабильного течения заболевания в данной возрастной группе понятны: склонность к развитию «нераспознанных» гипогликемий.
Длительный характер постгипогликемической гипергликемии не позволяет увязать нестабильное течение сахарного диабета с избыточной дозой инсулина. Как правило, это приводит к дальнейшему увеличению дозы инсулина. Из этого можно сделать очень важный вывод: при лечении детей младшего возраста следует всегда помнить о высокой чувствительности к инсулину в этом возрасте. Длительная передозировка инсулина с частыми гипогликемиями у маленького ребенка с незрелым мозгом очень опасна по двум причинам. С одной стороны, гипогликемия и патологическая постгипогликемическая гипергликемия являются причиной нестабильного течения заболевания, с другой, – частые гипогликемии и длительная гипергликемия отрицательно влияют на развитие мозга, особенно у ребенка в возрасте до 6 лет, и, следовательно, снижают интеллектуальные возможности ребенка.
Какова же наша цель и каковы наши возможности при лечении детей младшего возраста? Основная цель при лечении больного сахарным диабетом в любом возрасте – достижение стабильной компенсации заболевания. Это гарантирует больному существенное снижение риска развития осложнений сахарного диабета и, следовательно, – высокое качество жизни. Учитывая, что основной причиной нестабильного течения заболевания у детей младшего возраста являются частые гипогликемии, следует признать основной задачей при лечении детей этого возраста – предупреждение гипогликемических состояний со всеми вытекающими из этого последствиями.
Единственная возможность предупредить развитие гипогликемии – адекватная инсулинотерапия, максимально имитирующая эндогенную секрецию инсулина. При подборе и контроле суточной дозы инсулина следует помнить, что потребность в инсулине в этой возрастной группе невелика, а гипогликемии, как правило, протекают бессимптомно и потому не распознаются. С учетом этих особенностей, суточная доза инсулина (у детей без кетоацидоза) на первом году заболевания не должна превышать 0,5 ЕД/кг массы тела, в дальнейшем – не более 0,7 ЕД/кг/сут., а контроль гликемии должен проводиться значительно чаще, чем в других возрастных группах, особенно на фоне активной двигательной нагрузки (прогулки).
Адекватность инсулинотерапии зависит не только от дозы инсулина, но и от фармакокинетических и фармакодинамических свойств используемого препарата.
В качестве болюсных препаратов в данной ситуации показаны уль- тракороткие препараты аналогов инсулина. Именно эти препараты способны максимально синхронизировать прием пищи и активность инсулина и, тем самым, усвоить принятую пищу и предупредить возможность развития гипогликемии в перерывах между приемами пищи. Эти качества ультракоротких аналогов инсулина важны для больных на любом этапе заболевания, но у детей младшего возраста эти качества препарата особенно ценны, т.к. предупреждают склонность к развитию гипогликемий в дневные часы.
В качестве базальной терапии у детей младшего возраста также предпочтительны аналоги инсулина пролонгированного действия. Эти препараты не имеют выраженных пиков активного действия и, тем самым, снижают риск развития гипогликемических состояний, особенно в ночные часы. Итак, аналоги инсулинов в адекватных дозах реально снижают риск развития опасных гипогликемии у детей младшего возраста.
В настоящее время активно обсуждается очень важный, на наш взгляд, вопрос – повышение уровня целевых значений гликемии и гликированного гемоглобина у детей младшего возраста. Это обусловлено тем, что, во-первых, у больных в данной возрастной группе имеет место высочайший риск развития гипогликемических состояний, во- вторых, незрелый мозг ребенка более уязвим к эффектам гипогликемии. В связи с чем возникает естественное желание «держать» ребенка на более высоких цифрах гликемии. Так, Американская диабетологическая ассоциация (АДА-2007 г.) предлагает повысить уровень целевых значений гликемии до 10 ммоль/л перед едой, до 11 ммоль/л перед сном и гликированного гемоглобина до 8,5% для детей младшего возраста.
Основанием для подобных рекомендаций послужили хорошо известные факты:
- трудность в достижении целевых значений уровня гликемии и гликированного гемоглобина без риска развития гипогликемии;
- отсутствие специфических осложнений сахарного диабета у большинства детей в допубертатном периоде.
С последним аргументом трудно согласиться. Действительно, в до- пубертатном периоде осложнения регистрируются достаточно редко даже в тех случаях, когда ребенок длительно находится в состоянии декомпенсации заболевания.
Однако это не значит, что в пубертате именно у этих детей в первую очередь и проявятся специфические осложнения сахарного диабета.
Дело в том, что значительную роль в развитии сосудистых осложнений играет временной фактор. У детей младшего возраста, с хорошими по возрасту сосудами, требуется больше времени для формирования характерных сосудистых осложнений сахарного диабета.
На наш взгляд, снижение требований к целевым (более правильно- допустимым) значениям возможно лишь как временная мера и лишь в тех случаях, когда уже запущен механизм патологической контррегуляции. При достижении более стабильного течения заболевания необходимо постепенно повышать требования к уровню гликемии и гликированного гемоглобина с тем, чтобы достичь целевых значений этих показателей.
Врачи, дети более старшего возраста, подростки и члены семьи должны четко знать: только уровень гликемии и гликированного гемоглобина, максимально соответствующие нормальному, в отсутствие патологической вариабельности суточной гликемии, реально гарантируют значительное снижение риска сосудистых осложнений в дальнейшем.
Итак, достижение целевых значений уровня гликемии, суточной вариабельности гликемии, гликированного гемоглобина и, следовательно, стабильной компенсации заболевания у детей младшего возраста очень сложная, но, при соблюдении определенных условий, вполне решаемая задача. Каковы же эти условия? Самое главное условие – глубокое понимание всеми участниками лечебного процесса причины нестабильного течения заболевания в данном возрасте. Это позволит грамотно решать вопросы профилактики гипогликемических состояний.
С этой целью необходимо:
- поддерживать суточную дозу инсулина в пределах (не более!) 0,5 ЕД/кг в течение года после выявления заболевания и не более 0,7 ЕД/кг в ближайшие годы после заболевания;
- уметь синхронизировать дозу инсулина с приемом пищи и физическими нагрузками;
- отдавать предпочтение в этом возрасте аналогам инсулина (!);
- чаще исследовать уровень гликемии, особенно на фоне физических нагрузок.
Но, пожалуй, самое главное условие достижения стабильной компенсации заболевания – совместные усилия врача и семьи при полнейшем взаимопонимании сторон.
Роль врача, в первую очередь, сводится к обучению семьи вопросам, объясняющим:
- причины нестабильного течения заболевания в этом возрасте;
- возможность выхода из данной ситуации.
Помимо обучения, врач должен систематически контролировать качество самоконтроля заболевания, который проводится в семье с целью достижения целевых значений гликемии, ее вариабельности и гликированного гемоглобина.
Роль семьи сводится к четкому выполнению рекомендаций врача по самоконтролю заболевания (контроль синхронизации инсулинотерапии с питанием и физическими нагрузками) и неформальному ведению дневника для того, чтобы эти записи смогли в дальнейшем ответить на многие вопросы, возникающие в процессе лечения. Таким образом, у Вас сформируется индивидуальный учебник по особенностям сахарного диабета у Вашего ребенка.
Статья из монографии “Сахарный диабет: от ребёнка до взрослого”.
Сахарный диабет 1-го типа (СД 1) – заболевание, развивающееся преимущественно у детей и лиц молодого возраста, связанное с дефектом секреции инсулина и склонностью к кетоацидозу, требующее обязательной инсулинзаместительной терапии для достижения компенсации состояния углеводного обмена. Последнее положение явилось основой для возникновения термина инсулинзависимый сахарный диабет.
Поскольку при других клинических типах сахарного диабета также могут использоваться препараты инсулина при соответствующих показаниях, данный термин является некорректным.
Больные сахарным диабетом 1-го типа составляют 5-10% всех больных диабетом. Согласно международным данным, при сахарном диабете 1-го типа деструкция инсулинпродуцирующих β-клеток обычно является аутоиммунным процессом у лиц с соответствующей генетической предрасположенностью. Около 5% лиц, страдающих СД 1, имеют неаутоиммунную (идиопатическую) форму заболевания. Преимущественно это лица азиатского и африканского происхождения. Они склонны к развитию кетоацидоза, но, ни один из обычных маркеров аутоиммунного процесса у них не выявляется.
С точки зрения патологической физиологии формирования сахарного диабета 1-го типа, в 80-х годах ХХ века Дж. Эйзенбартом была сформулирована концепция его стадийности:
- Стадия генетической предрасположенности.
- Провоцирующее событие.
- Стадия явных иммунологических аномалий (развитие смешанной аутоиммунной реакции против панкреатических островков, опосредованной как аутореактивными CD8-лимфоцитами, так и циркулирующими антителами, с формированием прогрессирующего инсулита).
- Стадия латентного диабета (с нормальным уровнем глюкозы натощак и выявляемого нагрузочными пробами).
- Явный диабет (характерные клинические признаки заболевания).
- Терминальный диабет (с высокой потребностью в препаратах инсулина, признаками микроангиопатий, отрицательными или слабоположительными аутоиммунными тестами вследствие полной гибели β-клеток).
На рис. 2.1 представлена смена фаз заболевания в зависимости от состояния пула β-клеток по данным IDF (2007), основанным на вышеизложенной концепции Дж. Эйзенбарта.
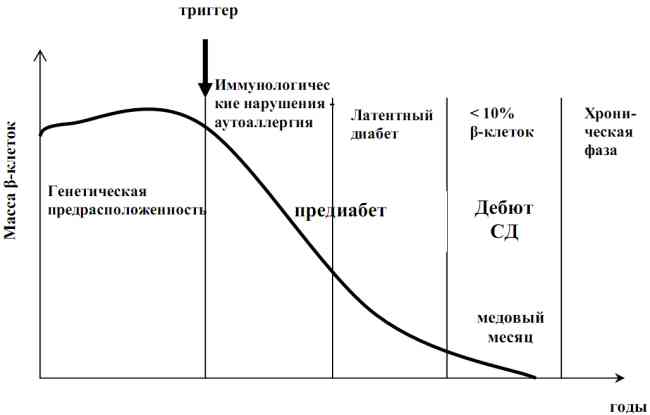
Рис. 2.1. Зависимость фаз СД 1 от состояния пула β-клеток (IDF, 2007, согласно концепции Дж. Эйзенбарта)
В качестве триггерных факторов наиболее часто выступают различные инфекционные агенты, такие как вирусы Коксаки, ECHO, краснухи, простого герпеса, цитомегаловируса. Общепризнанным является факт дебютирования сахарного диабета при поражении около 90% клеток поджелудочной железы.
Таким образом, в клиническом течении сахарного диабета 1-го типа на современном этапе (IDF, ISPAD, 2007-2008) выделяют такие фазы:
- доклинический диабет;
- дебют СД;
- частичная ремиссия («медовый месяц»);
- хроническая фаза пожизненной зависимости от применения препаратов инсулина.
Очевидно, что доклинический диабет соответствует стадиям генетической предрасположенности, влияния провоцирующего события, стадии явных иммунологических аномалий и латентного СД на ранних фазах. Дебют сахарного диабета, частичная ремиссия и хроническая фаза соответствуют стадии явного диабета (в том числе и латентного на поздних стадиях). Длительное хроническое прогрессирующее течение заболевания соответствует стадии терминального диабета.
Доклинический сахарный диабет 1-го типа
Фаза доклинического СД может длиться месяцы или даже годы, предшествуя клиническому дебюту заболевания. В качестве маркеров аутоиммунного поражения β-клеток могут быть определены следующие показатели:
- Антитела к островковым клеткам.
- Антитела к глутаматдекарбоксилазе.
- Антитела к тирозинфосфатазе.
- Аутоантитела к инсулину.
- Генетические маркеры HLA-генотипа, INS-генотипа.
- Снижение скорости высвобождения инсулина в ответ на внутривенный (в/в) тест толерантности к глюкозе.
Риск прогрессирования сахарного диабета 1-го типа определяется наличием следующих HLA-генотипов:
- HLA DR3-DQA1*0501-DQB1* 0201 (поддерживающий генотип);
- HLA DR4-DQA1*0301-DQB1* 0302 (поддерживающий генотип);
- HLA DR2-DQA1*0102-DQB1* 0602 (протективный генотип).
Лица с позитивным результатом скрининга на СД должны регистрироваться в интернациональной сети исследования сахарного диабета и быть предупреждены о высоком риске дебютирования заболевания (ADA, 2006).
Дебют сахарного диабета 1-го типа
В результате формирования тотального инсулинодефицита наступает фаза дебюта сахарного диабета 1-го типа. Учитывая наличие доклинической фазы, корректнее говорить о клиническом дебюте заболевания.
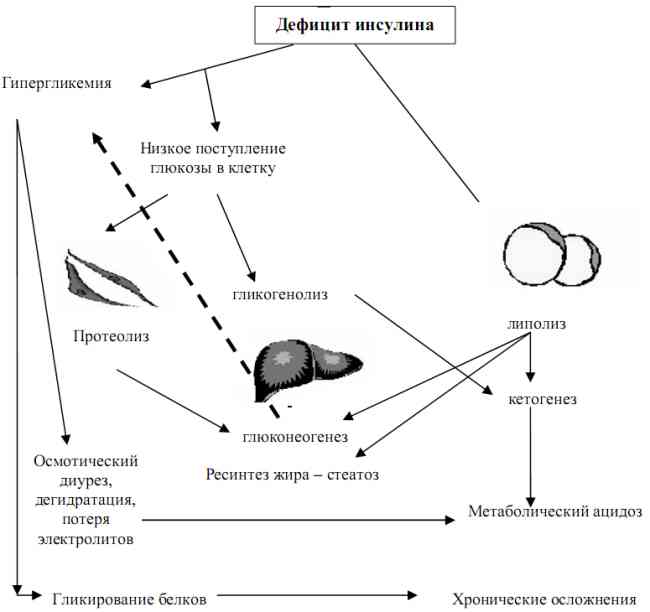
Основы формирования нарушений представлены на рис. 2.2 и тезисно сводятся к следующему:
- дефицит инсулина;
- гипергликемия / низкое поступление глюкозы в клетку;
- снижение потребления глюкозы мышечными клетками с последующим протеолизом и захватом аминокислот печенью с целью превращения в глюкозу (глюконеогенез);
- липолиз с нарушением превращения триглицеридов, ведущий к повышению выброса свободных жирных кислот (СЖК) с ресинтезом липидов в печени и кетогенезом (через ацетил-КоА);
- редуцирование захвата глюкозы печенью, гликогенолиз, продукция кетоновых тел (через пировиноградную кислоту (ПВК)).

Рис. 2.2. Эффекты инсулинодефицита при СД 1
Таким образом, клиническая картина нарушений при явном (клинически значимом) сахарном диабете 1-го типа является следствием приведенных нарушений. Несмотря на классическое острое начало заболевания, сахарный диабет 1-го типа имеет длительный скрытый период, который может продолжаться в течение многих лет.
Согласно данным G. S. Eisenbarth (1989), выделяют шесть стадий этого процесса.
I стадия – генетическая предрасположенность, которая реализуется менее чем у половины однояйцевых близнецов и у 2-5% сибсов. Большое значение придается наличию антигенов HLA, особонно II класса (DR 3, DR 4, DQ). При этом риск развития сахарного диабета 1-го типа возрастает многократно.
II стадия – гипотетический триггерный фактор (вирусная инфекция, стресс, характер питания, химические факторы).
III стадия – иммунные нарушения при сохранении нормальной секреции инсулина. Определяют иммунологические маркеры СД 1: аутоантитела к антигенам β-клеток (ICA), инсулину (IAA), глутаматдекарбоксилазе (GAD), тирозинфосфатазе островковых клеток (IA2α, IA2β).
IV стадия – выраженные иммунные нарушения, прогрессирующее снижение секреции инсулина вследствие развивающегося инсулина при нормальном уровне глюкозы в крови.
V стадия – клиническая манифестация, которая развивается после гибели 80- 90% массы β-клеток. При этом сохраняется остаточная секреция С-пептида.
VI стадия – полная деструкция β-клеток.
Дебют сахарного диабета 1-го типа варьирует от неинтенсивных форм до тяжелой дегидратации и диабетического кетоацидоза. Достаточно часто первые симптомы заболевания ошибочно принимают за иную патологию, что ведет к диагностированию СД, когда пациент находится уже в крайне тяжелом состоянии.
Неинтенсивный дебют сахарного диабета 1-го типа характеризуется:
- дебютом энуреза, который может ошибочно расцениваться как проявление инфекции мочевыводящих путей;
- вагинальным кандидозом, особенно в пубертатном и препубертатном возрасте;
- рвотой, которая может быть ошибочно принята как симптом гастроэнтерит;
- хронической потерей массы тела или плохим ее набором;
- раздражительностью и снижением школьной успеваемости;
- рецидивирующими инфекциями кожи.
Интенсивный дебют заболевания характеризуется наличием тяжелых форм классических клинических проявлений СД:
- тяжелой дегидратации;
- частой рвоты;
- пролонгированной полиурии, усугубляющейся проявлениями дегидратации;
- потери массы тела вследствие потери жидкости, мышечной и жировой массы;
- наличием ацетона в выдыхаемом воздухе;
- диабетического рубеоза щек на фоне кетоацидоза;
- гипервентиляции на фоне диабетического кетоацидоза в виде высокой частоты и большой амплитуды дыханий (дыхание типа Куссмауля);
- нарушения сознания;
- шока (частый пульс, обедненная периферическая циркуляция с периферическим цианозом);
- артериальной гипотензии (поздний и редко встречающийся у детей признак).
Степень выраженности клинических проявлений заболевания зависит от возраста, дебюта и стадии в период выявления.
В семьях детей, больных сахарным диабетом 1-го типа, имеет место эффект накопления генов и отмечается «синдром упрежения»: сахарный диабет развивается в более молодом возрасте, чем у родителей, и протекает тяжелее. В последнее время число больных сахарным диабетом 1-го типа растет преимущественно за счет детей до 5 лет.
Так называемое омоложение СД 1, то есть тенденция к более высокой частоте заболевания детей в раннем возрасте, прослеживается и по данным эндокринологического отделения Областной детской клинической больницы г. Харькова. Так, за последние 7 лет заболеваемость СД возросла в 4 раза преимущественно за счет дебюта в раннем возрасте.
Особенностью дебюта заболевания у грудных детей и детей раннего возраста является интенсивное начало заболевания с формированием диабетического кетоацидоза и сопутствующего синдрома мальабсорбции.
У грудных детей имеет место краткосрочный продромальный период в виде прогрессирующей дистрофии на фоне сохраненного аппетита с последующим присоединением инфекции, формированием токсико-септического и коматозного состояния.
В дебюте заболевания у взрослых, когда диабет уже диагностирован, но сахарный диабет 2-го типа не исключен, в пользу подтверждения сахарного диабета 1-го типа служит выявление следующих симптомов:
- наличие кетонурии, или
- потеря массы тела, или
- отсутствие у пациента признаков метаболического синдрома или других родственных заболеваний.
Частичная ремиссия («медовый месяц»)
«Медовый месяц» – кратковременный период течения сахарного диабета 1-го типа в начале заболевания, когда снижается потребность в инсулине. Данная фаза СД 1 обусловлена тем, что повышенный уровень глюкозы в крови индуцирует последние резервы β-клеток с выделением субадекватного количества инсулина. На этом этапе течения заболевания около 80% детей и подростков, больных СД 1, нуждаются в существенном снижении дозы вводимых препаратов инсулина. Известны случаи, когда потребность в инсулине в этой фазе составляла 0,5-0,25 ЕД инсулина в сутки.
Критерии фазы частичной ремиссии неконкретны. Наиболее часто она диагностируется при снижении потребности в препаратах инсулина менее 0,5 ЕД/кг/сут при уровне HbA1c < 7 %.
Фаза частичной ремиссии длится от нескольких дней до нескольких месяцев, что зависит от состояния поджелудочной железы конкретного индивидуума. В течение этой фазы уровень глюкозы крови часто стабилизируется на нормальных значениях, несмотря на нарушения диеты и режима физических нагрузок.
Указанная особенность этой фазы ведет к тому, что многие взрослые пациенты и родители заболевших детей отказываются от инъекций препарата по причине «удовлетворительного состояния и хорошего самочувствия», что ведет к возникновению нового эпизода декомпенсации заболевания. Такая ситуация требует проведения обязательной разъяснительной работы. Пациентам и их родителям необходимо объяснить, что фаза ремиссии со снижением дозы инсулина является временной, а введение препарата не только не оказывает повреждающего действия на инсулярный аппарат, но является крайне необходимым для предотвращения тяжелой декомпенсации. Имеются данные, что кетоацидоз в дебюте заболевания существенно снижает вероятность возникновения фазы частичной ремиссии и сокращает ее длительность.
Хроническая фаза пожизненной зависимости от применения препаратов инсулина
Прогрессирование заболевания от фазы частичной ремиссии до хронической пожизненной зависимости от препаратов инсулина обусловлено постепенным снижением функции остаточных β-клеток, особенно на фоне интеркуррентных заболеваний, требующих для компенсации состояния повышенного инсулинообеспечения.
Данная фаза характеризуется отрицательными или слабоположительными аутоиммунными тестами на аутоиммунитет вследствие полной гибели β-клеток, неспособных генерировать С-пептид. При этом иммунореактивный инсулин внепанкреатического и экзогенного происхождения может обнаруживаться в крови. В среднем обычно полное исчезновение β-клеток происходит в течение 3,5-5 лет. Хроническая гипергликемия в сочетании с гликированием белков ведут к формированию микро- и макрососудистых осложнений заболевания.
В целом, хроническая фаза сахарного диабета у детей и подростков протекает аналогично таковой у взрослых, хотя имеют место некоторые особенности. Следует остановиться на таком феномене, хорошо известном детским эндокринологам, как лабильность течения заболевания. Основа этого феномена заключается в особенностях иммунной системы ребенка. Аутоантитела, стимулирующие инсулиновый рецептор, способны вызывать гипогликемический эффект вследствие инсулиномиметического действия на клетки-мишени.
Подростковый период является переходным периодом от ребенка до взрослого и характеризуется существенными биологическими и психосоциальными изменениями в организме, что ведет к лабильному течению заболевания с эпизодами гипо- и гипергликемий.
Психологический профиль подростков с сахарным диабетом 1-го типа характеризуется в большинстве случаев плохим метаболическим контролем вследствие нарушения режимов инсулинотерапии, несоблюдением принципов самоконтроля, склонностью к девиантному поведению с употреблением спиртных напитков, табакокурением, использованием наркотических веществ. Даже при адекватном соблюдении рекомендаций стиль жизни подростка изменяется вследствие активных физических и психоэмоциональных нагрузок, связанных с обучением и адаптацией к коллективу, началом активной половой жизни.
Гормональным обеспечением такого стиля жизни являются стрессовые реакции, реализующиеся посредством дополнительного выброса катехоламинов, адренокортикотропного гормона (АКТГ), кортизола, соматотропина (СТГ), пролактина, андрогенов, а также появления в организме хорионического гонадотропина и повышения концентрации прогестерона. Последние обладают прямым контринсулярным эффектом и снижают действие инсулина на периферии.
Так, «феномен утренней зари», проявляющийся повышением уровня глюкозы и потребности в инсулине в ранние утренние часы без эпизодов ночной гипогликемии, обусловлен ночным выбросом соматотропина.
Из монографии «Сахарный диабет: от ребенка до взрослого»
Сенаторова А.С., Караченцев Ю.И., Кравчун Н.А., Казаков А.В., Рига Е.А., Макеева Н.И., Чайченко Т.В.
ГУ «Институт проблем эндокринной патологии им. В.Я. Данилевского АМН Украины»
Харьковский национальный медицинский университет
Харьковская медицинская академия последипломного образования МЗ Украины
Источник
