Сахарный диабет 2 типа демидова
В помощь практическому врачу освещены вопросы лечения больных сахарным диабетом 2 типа и коморбидными заболеваниями
Актуальность
Первые сообщения о диабете появились еще в Древнем Египте, при этом его описывали как заболевание, основными симптомами которого являлись потеря веса и полиурия. Сам термин «диабет» был предложен древнегреческим врачом Aertaeus. Название болезни происходит от греческого слова «диавэно», означающего «прохожу сквозь», «протекаю». Для обозначения сахарного диабета к слову «диабет» добавили mellitus (от латинского mel — мёд) [1].
В наше время проблема СД по-прежнему остается крайне актуальной в связи с тем, что наблюдается неуклонный рост числа пациентов с СД, а также диабету сопутствуют осложнения со стороны различных органов и систем. Согласно данным официальной статистики в России в настоящее время сохраняется высокая распространенность СД2 — им страдают 4,15 млн населения (мужчины — 28,9%, женщины — 71,1%). Средний возраст дебюта СД2 в 2017 г., по данным официальной статистики, составляет 57,8 года, при этом средняя продолжительность жизни данных больных — около 8,5 года [2].
Сахароснижающая терапия с учетом коморбидности СД2
Вместе с тем становится очевидным, что для практикующего врача при таком среднем возрасте дебюта СД2 на первый план выходит проблема коморбидности СД2 с поражением других органов и систем, что особенно важно для подбора сахароснижающей терапии, адекватной клинической ситуации.
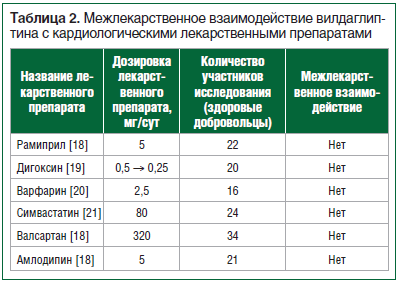
Достижение целевых значений НbА1с у больных СД2 является наглядным отражением эффективности сахароснижающей терапии. Выбор целевого значения НbА1с на современном этапе должен осуществляться с учетом индивидуальных особенностей каждого пациента с СД2, включая возраст, клинические характеристики, а также функциональное состояние (табл. 1) [3].
Современное представление о пациенте с СД2 включает понятие «кардио-рено-метаболического пациента». Другими словами, у пациента с СД2 особенно уязвимы сердечно-сосудистая система, почки и метаболизм. Поэтому с самого начала болезни необходимо отслеживать и уделять должное внимание коррекции нарушений со стороны этих систем с целью комплексной профилактики осложнений и прогрессирования патологии. При СД2 все взаимосвязано, по-видимому, патогенетически, это изначальная коморбидность, а не сочетание заболеваний или последствия гипергликемии, как думали раньше. Понимание этого крайне важно с учетом концепции патогенетического лечения СД2 и попытки коррекции этиологических факторов и всех звеньев патогенеза.
Какие же заболевания наиболее часто сопутствуют СД2? В 2015 г. были опубликованы результаты исследования А. Calderon-Larranaga et al., в котором авторы изучили частоту сопутствующих диабету заболеваний в Испании. Ретроспективно была проанализирована выборка из 10 398 больных СД2 в возрасте старше 14 лет на момент визита. Установлено, что наиболее частыми факторами риска сердечно-сосудистых осложнений (ССО) у больных СД2 являются артериальная гипертония (АГ) (59,32%), нарушения липидного обмена (41,4%) и ожирение (18,48%). Распространенность хронической сердечной недостаточности при этом составляет 4,65% [4]. Эти данные подтверждаются результатами другого исследования, проведенного в Великобритании в 2019 г., в котором были проанализированы медицинские карты 102 394 больных СД2 в возрасте старше 35 лет, которых наблюдали в первичном звене здравоохранения. Авторы установили, что наиболее частым фактором риска ССО у больных СД2 также является АГ (42,8% у мужчин и 45,8% у женщин). Обращает на себя внимание тот факт, что на втором месте у женщин с СД2 была депрессия (20,2%), а у мужчин — ИБС (13,6%) [5].
Метаболический контроль и, в частности, достижение целевого гликемического уровня у больных СД2 по-прежнему остаются актуальной проблемой современной эндокринологии, а многофакторный контроль, включающий достижение целевых уровней АД, холестерина липопротеидов низкой плотности (ХС ЛПНП) (концепция АВС), является фундаментальной основой лечения СД2. В опубликованных недавно европейских клинических рекомендациях по лечению больных СД2 под эгидой Европейского общества кардиологов и Европейской ассоциации по изучению сахарного диабета приведены целевые уровни АД и липидного профиля для больных СД2. Целевой уровень систолического АД (САД) составляет 130 мм рт. ст., но не менее 120 мм рт. ст., при этом у пациентов в возрасте старше 65 лет целевым уровнем САД является диапазон 130–139 мм рт. ст. (класс / уровень доказательности IA). Для пациентов с СД2 с умеренным риском развития ССО целевой уровень ХС ЛПНП составляет < 2,5 ммоль/л, с высоким уровнем ССО — <1,8 ммоль/л, а с очень высоким риском ССО — <1,4 ммоль/л (класс / уровень доказательности I A/B). Также необходимо отметить, что самый высокий класс / уровень доказательности для достижения всех указанных целевых показателей — I А/B, что подразумевает достижение указанных целевых значений абсолютно у всех больных СД2. Таким образом, европейские эксперты заключили, что без проведения адекватной антигипертензивной и гиполипидемической терапии у больных СД2 невозможно добиться существенного успеха в предотвращении сердечно-сосудистых катастроф [6]. Учитывая вышесказанное, очевидно, что лечение больных СД2 на современном этапе должно осуществляться совместно и эндокринологами, и кардиологами.
Профиль межлекарственного взаимодействия вилдаглиптина
Эффективность и безопасность вилдаглиптина у больных СД2 были доказаны результатами большого количества крупных рандомизированных исследований (РКИ), что послужило основанием для включения его в отечественные и международные алгоритмы по диагностике и лечению больных СД2 [3, 4, 7].
Известно, что при адекватной терапии на ранней стадии СД2 уменьшаются осложнения указанного заболевания, инвалидизация и смертность [8–10].В октябре 2019 г. на конгрессе Европейской ассоциации по изучению сахарного диабета, проходившем в Барселоне (Испания), были озвучены результаты РКИ VERIFY, впервые продемонстрировавшего преимущества ранней комбинированной терапии вилдаглиптин + метформин у больных с впервые выявленным СД2. Исследование продолжалось 5 лет и включило 2001 больного СД2 в возрасте 18–70 лет (55% женщин), с показателями HbA1c в диапазоне 6,5–7,5% и индексом массы тела 22–40 кг/м2. Было установлено, что назначение ранней комбинированной терапии вилдаглиптин + метформин позволяет на 49% снизить относительный риск неудачи проводимой терапии (уровень HbA1c ≥ 7,0%) по сравнению с монотерапией метформином исходно. В группе пациентов, исходно получавших монотерапию метформином, уже через 3 года наблюдалось ускользание лечебного эффекта, тогда как в группе ранней комбинированной терапии недостаточный гликемический контроль наблюдался через 5 лет и более. При сравнении этих двух стратегий также выявлено, что в группе ранней комбинированной терапии было на 26% меньше пациентов, которым потребовалась интенсификация лечения с помощью инсулинотерапии [11].
Для пациентов с длительным стажем СД2 и сопутствующей патологией вопросы межлекарственных взаимодействий в настоящее время так же актуальны, как и подбор оптимальной сахароснижающей терапии. Данные 8 ретроспективных и 4 проспективных исследований показали, что самыми частыми классами лекарственных препаратов, вызывающих межлекарственное взаимодействие, являются нестероидные противовоспалительные средства (23,2%), противосудорожные препараты (17,1%), антибиотики (12,6%), препараты для лечения ХОБЛ и бронхиальной астмы (8,9%), анальгетики (8,9%) [12].
Общеизвестно, чтопри увеличении числа препаратов увеличивается риск развития межлекарственных взаимодействий [13]. Актуальность данной проблемы подчеркивается тем, что потенциально опасные межлекарственные взаимодействия являются главной причиной отзыва лекарственного средства с фармацевтического рынка, а серьезные межлекарственные взаимодействия привели к 6,7% от всех госпитализаций в США [14]. В 2019 г. проблема полипрагмазии у больных СД2 была актуализирована результатами метаанализа, проведенного Al-Musawe L. et al., в котором установлена статистически значимая взаимосвязь между полипрагмазией, смертностью от всех причин (ОШ 1,622; 95% ДИ 1,606–1,637, p<0,001) и инфарктом миокарда (ОШ 1,962; 95% ДИ 1,942–1,982, p<0,001) [15].
С учетом того, что АГ и нарушения липидного обмена являются наиболее распространенными коморбидными заболеваниями у больных СД2, безопасный профиль межлекарственного взаимодействия вилдаглиптина представляется крайне важным для практикующего врача. Более того, в 2018 г. Национальный институт здоровья и клинического совершенствования Великобритании (NICE) с целью уменьшения неблагоприятных сердечно-сосудистых событий у больных СД2 добавил новые индикаторы для оценки качества процесса лечения, в т. ч. для оценки доли больных СД2, принимающих статины [16].
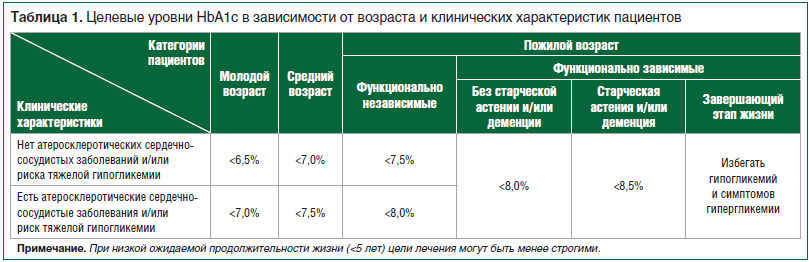
В исследованиях у здоровых добровольцев не было выявлено межлекарственных взаимодействий вилдаглиптина в дозе 100 мг/сут с часто применяемыми в клинической практике группами препаратов для лечения сердечно-сосудистой системы (ингибиторы АПФ, блокаторы рецепторов ангиотензина II типа 1, антагонисты кальциевых каналов дигидропиридинового ряда, статины, пероральные антикоагулянты, сердечные гликозиды) (табл. 2). Это может объясняться тем, что вилдаглиптин не метаболизируется в печени, не является субстратом изоферментов Р450 (CYP), не ингибирует и не индуцирует изоферменты цитохрома Р450 [17].

В настоящее время у больных СД2 сохраняется высокая распространенность поражения почек: почти у трети диагностирована хроническая болезнь почек (ХБП)
2–5 стадии, характеризующаяся микроальбуминурией/протеинурией и/или сниженной скоростью клубочковой фильтрации (СКФ) [22]. При этом известно, что нарушение функции почек значительно повышает сердечно-сосудистый риск и затрудняет достижение компенсации из-за высокого риска гипогликемий [23]. Вероятной причиной такой высокой распространенности ХБП у больных СД2 может быть связь механизмов развития ХБП с ожирением, АГ, СД и гиперактивностью ренин-ангиотензин-альдостероновой системы [24].
Определение клинических характеристик пациентов с СД2 в сочетании с ХБП существенно ограничило потенциальные варианты сахароснижающей терапии, поскольку данной категории пациентов противопоказана терапия метформином, ингибиторами α-глюкозидазы и большинством препаратов из группы сульфонилмочевины (ПСМ). Набор веса и задержка жидкости при лечении пиоглитазоном, разрешенным к применению в этой популяции, объясняют его низкую привлекательность для пациентов с нарушениями функции почек, а применение инсулинов короткого действия и ПСМ у пациентов со значительно сниженной СКФ повышает риск развития гипогликемии в связи с их непредсказуемым накоплением. Лечение СД2 у пациентов с нарушениями функции почек также осложнено повышенным или непредсказуемым уровнем системного воздействия не только противодиабетических средств, но и других лекарственных препаратов [22].
На фоне этого ингибиторы дипептидилпептидазы-4, проявляющие физиологическую активность, оказались подходящим альтернативным вариантом лечения пациентов с нарушениями функции почек. Данная концепция была подтверждена результатами крупного РКИ (n=525), проводившегося в течение одного года, в котором эффективность и безопасность вилдаглиптина изучали у пациентов с СД2 и умеренными или тяжелыми нарушениями функции почек. Установлено, что профиль безопасности вилдаглиптина в режиме 50 мг 1 р./сут у таких пациентов не отличался от профиля безопасности плацебо. В другом исследовании были определены аналогичные профили безопасности вилдаглиптина и ситаглиптина (n=148) у пациентов с СД2 и тяжелыми нарушениями функции почек. Было выявлено, что лечение вилдаглиптином хорошо переносилось пациентами с СД2 и тяжелыми нарушениями функции почек и недостаточным гликемическим контролем на фоне инсулинотерапии, пожилыми пациентами (≥75 лет) с умеренными или тяжелыми нарушениями функции почек, пациентами с впервые выявленным СД2 после трансплантации и пациентами на гемодиализе, а профиль нежелательных явлений и серьезных нежелательных явлений в группах сравнения существенно не отличался [22].
В 2017 г. D.W. Strain et al. провели всестороннюю оценку соотношения пользы и риска лечения вилдаглиптином пациентов с нарушениями функции почек, в т. ч. в фармакокинетических исследованиях и исследованиях клинической безопасности у пациентов на гемодиализе. Установлено, что фармакокинетический профиль вилдаглиптина у пациентов с умеренными и тяжелыми нарушениями функции почек в сравнении с фармакокинетическим профилем в популяции с сохранной функцией почек показал сопоставимую с максимальной концентрацией инсулина в плазме крови и в 2 раза увеличенную экспозицию вилдаглиптина. Эти наблюдения позволили снизить частоту приема препарата до 1 р./сут и при этом сохранить эквивалентный гликемический эффект, что привело к снижению стоимости терапии вилдаглиптином в 2 раза [25].
Для некомпенсированного СД характерны положительная корреляция с пиелонефритом, циститом и т. д. и склонность к частым обострениям, о которых надо помнить при интенсификации сахароснижающей терапии (в свете рекомендаций о широком назначении ингибиторов натрий-глюкозного котранспортера 2 типа). Все это необходимо учитывать при выборе сахароснижающего препарата, минимизируя риски развития урогенитальной инфекции.
В последние годы появился новый взгляд на формирование доброкачественной гиперплазии предстательной железы (ДГПЖ) как гормонально-метаболического заболевания. Патогенез ДГПЖ долгое время оставался неясным, в последние годы появилась информация о влиянии ожирения, инсулинорезистентности, метаболического синдрома на развитие ДГПЖ [26]. Данная гипотеза была подтверждена результатами сравнительного проспективного исследования у мужичин в возрасте ≥55 лет, в котором была установлена положительная взаимосвязь между наличием СД2 и объемом предстательной железы [27]. В другом исследовании у 117 мужчин пожилого возраста с СД2 и ДГПЖ также была выявлена позитивная взаимосвязь между степенью тяжести СД и объемом предстательной железы [28].
Заключение
Резюмируя, можно заключить, что диагностика и ведение пациентов с СД2 и наличием коморбидных заболеваний в настоящее время остается одной из наиболее сложных задач в клинической практике, а при выборе сахароснижающего препарата должен осуществляться персонифицированный подход с учетом благоприятного профиля межлекарственного взаимодействия назначаемых препаратов. С появлением в клинической практике вилдаглиптина появилась возможность патогенетической терапии, и лечение больных СД2 стало более безопасным и эффективным.
Сахарный диабет представляет собой серьезную медико–социальную проблему, что обусловлено его высокой распространенностью, сохраняющейся тенденцией к росту числа больных, хроническим течением, определяющим кумулятивный характер заболевания, высокой инвалидизацией больных и необходимостью создания системы специализированной помощи. Сахарный диабет (СД) занимает третье место среди непосредственных причин смерти после сердечно–сосудистых и онкологических заболеваний, поэтому решение вопросов, связанных с проблемой сахарного диабета, поставлено во многих странах на государственный уровень. По определению экспертов Всемирной Организации Здравоохранения, «сахарный диабет является проблемой всех возрастов и всех стран».
Важнейшей проблемой современной диабетологии является разработка новых, более эффективных способов профилактики и терапии СД 2 типа, призванных сократить темпы роста численности больных в популяции, а также значительно уменьшить риск развития микро– и макрососудистых осложнений, полиневропатии, увеличить продолжительность жизни больных и минимизировать социально–экономические потери. Опираясь на данные ретроспективного анализа множества крупномасштабных, международных исследований в области диабета, констатируется необходимость эффективного многофакторного управления многочисленными нарушениями, развивающимися при СД 2 типа, что связано с большими объективными и субъективными сложностями. Отмечаются новые акценты и цели коррекции метаболических и сосудистых отклонений, пересматривается понимание роли патогенетических факторов болезни, подчеркивается приоритетность многопланового интервенционного подхода. Современная тактика ведения больных СД 2 типа должна базироваться на глубоком понимании механизмов его развития с целью коррекции ключевых патогенетических дефектов, на достижении раннего, жесткого и, одновременно, безопасного гликемического контроля, а также длительной коррекции метаболических и сосудистых отклонений.
Основным клиническим нарушением, свойственным СД, является гипергликемия, которая приобретает хронический характер и оказывает токсическое, повреждающее воздействие на многочисленные ткани–мишени. Исследования последних лет показали важнейшую и, возможно, решающую роль вариабельности суточной гипергликемии в развитии патологических изменений не только в микроциркуляторном русле, на уровне капилляров, но и в формировании патологических процессов в магистральных сосудах и миокарде. Необходимо подчеркнуть, что СД 2 типа характеризуется двумя фундаментальными дефектами: инсулинорезистентностью (ИР) на уровне печени, жировой и мышечной тканей и дисфункцией β–клеток поджелудочной железы. Длительно существующая и прогрессирующая ИР составляет патофизиологический фундамент для гиперинсулинемии и последующей декомпенсации секреторной активности β–клеток поджелудочной железы, появления гипергликемии как натощак, так и постпрандиально. Следует отметить, что большое значение имеет скорость и выраженность снижения массы функционирующих β–клеток, это определяет тяжесть заболевания, характер гипергликемии, выбор медикаментозной коррекции. В целом диапазон колебания уровней глюкозы крови зависит от количества и вида пищи, адекватного инсулинсекреторного ответа поджелудочной железы и лишь вторично – от тканевой чувствительности к инсулину. Так, мониторирование суточной гликемии у больных СД 2 типа показало увеличение на 38% постпрандиальных уровней глюкозы в кровотоке после завтрака, обеда и ужина по сравнению с аналогичными показателями в группе здоровых лиц. Причем длительность каждого колебания постпрандиального уровня гликемии составляла более 240 минут, а общая продолжительность около 13 часов за день. Значит, показатели постпрандиальной гипергликемии являются важнейшим компонентом общего метаболизма и оказывают очень существенное влияние на состояние организма.
Значимость уровней глюкозы крови в первую очередь определяется феноменом «глюкозотоксичности», который на сегодняшний день подразделяется на острый и хронический, а его влияние рассматривается шире, чем просто деструктивное воздействие на b–клетки поджелудочной железы. «Глюкозотоксичность» ответственна за прогрессирование СД 2 типа, она замыкает порочный круг нарушений, свойственных этому заболеванию. В последнее время очень часто обсуждается роль вариабельности гипергликемического профиля в патогенезе поздних осложнений и повышении сердечно–сосудистой и цереброваскулярной заболеваемости, развитии ишемической болезни сердца. Большинство так называемых сердечно–сосудистых факторов риска у больных СД 2 типа напрямую связаны с повышением гликемии натощак и после приема пищи. Гипергликемия вносит существенный вклад в образование атеросклеротических бляшек на всех этапах. Атерогенные изменения липидного профиля напрямую коррелируют с повышением уровней глюкозы крови, они умножаются в постпрандиальном состоянии. Уровни триглицеридов, процессы окисления липопротеидов низкой плотности (ЛПНП) также тесно связаны с гипергликемией и, в свою очередь, снижаются при ее нормализации. В равной степени отмечается прямая зависимость между выраженностью гипергликемии и повышением факторов свертываемости крови и активности тромбина при СД 2 типа. И, наконец, существуют убедительные доказательства того, что гипергликемия может самостоятельно вызывать эндотелиальную дисфункцию, а также повышать показатели артериального давления как у лиц с нарушенной толерантностью к глюкозе (НТГ), так и у больных СД 2 типа. В последние годы оксидативный стресс и эндотелиальная дисфункция были признаны наиболее значительным патофизиологическим звеном между сердечно–сосудистыми заболеваниями и СД 2 типа. Специфические изменения сосудистой стенки, безусловно, напрямую зависят от длительности и выраженности хронической гипергликемии и ее пиковых значений, а ее адекватный контроль путем коррекции инсулиновой секреции и ИР является необходимым условием для предотвращения развития сердечно–сосудистых заболеваний, улучшения прогноза и качества жизни больных.
Итак, современные проблемы управления СД 2 типа приобретают новый характер, ставятся задачи достижения более раннего и жесткого гликемического контроля, снижения постпрандиальных пиков и гипогликемических эпизодов, нормализации вариабельности гликемического профиля, уменьшения ИР. Современное медикаментозное противодиабетическое лечение должно быть не только безопасным и эффективным – оно призвано замедлять темпы прогрессирования заболевания и даже восстанавливать массу функционирующих b–клеток и т.д. Для выполнения поставленных задач предлагаются определенные тактические подходы. Первое – это частый контроль уровня НВА1с (1 раз в 3 месяца) и незамедлительная интенсификация лечения в зависимости от полученного результата. Согласно рекомендациям Американской диабетической ассоциации и Российского Федерального руководства целевым значением HbA1c для больных СД 2 типа является уровень менее 7%. Однако подчеркивается необходимость индивидуализации целевого значения НВА1с и важность максимального, но безопасного (без эпизодов гипогликемии) приближения его к диапазону нормы (4–6%). Более низкие целевые параметры гликемического контроля могут предназначаться лишь для части пациентов, с небольшой длительностью СД 2 типа, большим ожиданием продолжительности жизни, при отсутствии значимых сердечно–сосудистых заболеваний (ССЗ). Эта категория больных СД 2 типа может получить дополнительные микроваскулярные преимущества от достижения более низкого целевого уровня HbA1c <7%. Другая часть пациентов, в анамнезе которых отмечаются тяжелые или частые гипогликемические реакции, с ограниченными ожиданиями продолжительности жизни, большой длительностью СД, с микро– и макрососудистыми осложнениями, напротив, могут получить пользу от менее жесткого целевого уровня HbA1c – (м.б.>7%). Баланс между потенциальными преимуществами и возможными рисками жесткого гликемического контроля, а также интенсификации лечения должен определяться в каждом конкретном случае. Кроме того, подчеркивается роль самоконтроля показателей глюкозы плазмы натощак (не выше 5,5 ммоль/л) и постпрандиально (ниже 7,5 ммоль/л).
Второе – это ранний переход на комбинированную терапию. Хорошо известно, что первым шагом в лечении СД 2 типа являются мероприятия по изменению образа жизни, направленные на изменение пищевого поведения, повышение уровня физической активности, снижение массы тела. Наряду с этим признана необходимость одновременного присоединения метформина при отсутствии противопоказаний или значимых побочных эффектов. Ставится задача одновременной, ранней коррекции всех патогенетически значимых дефектов СД 2 типа, наравне с метаболическим контролем, с целью снижения темпов прогресса основного заболевания. Вид выбранной противодиабетической монотерапии во многом определяет динамику этих важных аспектов. Так, крупное 5–летнее исследование ADOPT четко изучило все преимущества и недостатки длительной монотерапии различными пероральными, сахароснижающими препаратами (ПСП) – росиглитазоном (Авандия), метформином и глибенкламидом. Оказалось, что в среднем росиглитазон (Авандия) обеспечивал успешный целевой контроль СД 2 типа, согласно уровню НВА1с на 2 года дольше, по сравнению с глибенкламидом и на 1 год по сравнению с метформином. В дополнение к этому были выявлены различия по влиянию указанных препаратов на секреторную активность b–клеток и их чувствительность к глюкозному стимулу. Следует подчеркнуть, что именно этот дефект рассматривается в качестве ключевой причины прогрессирования СД 2 типа и усиления гипергликемии. Темпы снижения функциональных способностей b–клеток на фоне росиглитазона (Авандии) составлял 2% в год, в то время как на фоне терапии метформином этот показатель был 3%, а глибенкламидом – 6% в год. Несомненно, способность сохранять секреторную функцию b–клеток, является очень существенным преимуществом. К сожалению, любые ПСП не обладают способностью воздействовать на все ключевые звенья патогенеза СД 2 типа. Возможности обеспечивать долгосрочный контроль уровня глюкозы в крови на должном уровне ограничены, и возникает потребность в комбинированной терапии.
Третье – это четкое выполнение пациентом рекомендаций врача, систематический прием препаратов без пропусков и перерывов, то, что называют комплаентностью. Результаты исследований свидетельствуют о том, что значительная часть больных СД допускает нарушения в приеме ПСП, демонстрируя неудовлетворительный уровень приверженности лечению – от 31 до 60%. По обобщенным данным Cramer J.A. и соавторов, лишь 58% больных СД принимают ПСП регулярно (более 80% дней в году). Кроме этого, достаточно распространенным является полное прекращение медикаментозной терапии по собственной инициативе больного (8–16% случаев). Изучение основных причин невыполнения врачебных рекомендаций показало, что лишь часть из них имеют отношение к пациенту: социальное и финансовое положение, недостаточное понимание важности для здоровья, предубеждения в отношении лечения, и т.д. Другие факторы заключаются в длительном, хроническом течении заболевания, и необходимости пожизненного лечения, характеристиках используемого лекарственного средства, пути введения, сложности режима дозирования, реальных или предполагаемых побочных эффектах и т.д. Следовательно, нужны фиксированные комбинации.
Предлагаемые на сегодняшний день современные алгоритмы ведения больных СД 2 типа учитывают все указанные потребности. Выбор конкретной комбинации медикаментозных средств базируется на оценке выраженности и длительности гипергликемии, уровня НВА1с, наличия диабетических осложнений в органах–мишенях. Кроме того, важно учитывать наличие висцерального ожирения, сопутствующие заболевания, возраст, предпочтения и мотивацию больного. На выбор способа лечения влияет переносимость лекарственной терапии, выраженность побочных эффектов, риск развития гипогликемий и соблюдение пищевых рекомендаций. Необходимо помнить и о важности соблюдения сроков (3 месяца) безопасного достижения всех целей терапии СД 2 типа. Все больше это обусловливает раннее применение современных комбинированных препаратов и многофакторное воздействие на сосудистые и метаболические нарушения.
Одним из таких средств, зарегистрированных в России, является Авандамет, представляющий собой фиксированную комбинацию росиглитазона (Авандии) с метформином. Авандамет высоко эффективен и безопасен, может применяться независимо от приема пищи и не вызывает гипогликемических реакций. Авандамет доступен в нескольких дозировках: 1 мг Авандии + 500 мг метформина (1/500 мг), 2 мг Авандии + 500 мг метформина (2/500 мг), 2 мг Авандии + 1000 мг метформина (2/1000 мг) и 4 мг Авандии + 1000 мг метформина (4/1000 мг), что позволит легко подобрать необходимую суточную дозу с учетом индивидуальных особенностей каждого больного. Особенно важно, что по сахароснижающей эффективности, которая в первую очередь оценивалась по уровню НВА1с, Авандамет был абсолютно сопоставим с раздельной комбинацией препаратов сульфонилмочевины и метформина. Однако снижение НВА1с у больных, получавших Авандамет, сопровождалось статистически значимым улучшением функции b–клеток поджелудочной железы, о чем свидетельствовали биохимические маркеры и расчетные индексы, через 52 недели терапии. Было установлено, что применение Авандамета может позволить добиться целевых уровней НВА1с менее 7% почти у 77% больных, что крайне заманчиво. При этом эпизоды гипогликемии отмечались в пять раз реже при терапии Авандаметом по сравненнию с комбинацией сульфонилмочевины и метформина. Все основные параметры липидного обмена (уровней триглицеридов, липопротеидов низкой плотности, общего холестерина) могут оставаться без изменения или характеризоваться незначительной динамикой на фоне лечения Авандаметом, однако уровень свободных жирных кислот статистически значимо снижается, что уменьшает выраженность липотоксичного действия. Параметры амбулаторного уровня диастолического артериального давления и важнейших кардиоваскулярных маркеров, таких как высокочувствительный СРБ и РАI–1, статистически достоверно снижались в группе Авандамета, что также благоприятно для сосудистого русла. Особенно следует подчеркнуть необходимость контроля периферических отеков, которые являются достаточно редким побочным эффектом, но показанием для отмены препарата. Перед назначением Авандамета необходимо тщательно обследовать пациента в отношении сердечной недостаточности и учесть все противопоказания.
Следуя современным международным рекомендациям и выполняя требования по подбору адекватной и эффективной гипогликемизирующей терапии, мы сможем улучшить результаты лечения и добиться лучших отдаленных исходов.
Данная статья опубликована
при финансовой поддержке компании GlaxoSmithKline
