Сахарный диабет у детей новые разработки в лечении
Санофи представила результаты международного клинического исследования EDITION JUNIOR на Российской научно-практической конференции детских эндокринологов, которая прошла с 12 по 13 сентября в Санкт-Петербурге. Цель исследования: оценить применение базального инсулина последнего поколения Туджео СолоСтар® (инсулин гларгин 300 ЕД/мл) у детей с 6 лет и старше, которые имеют сахарный диабет и требуют лечения инсулином.1 В исследовании приняли участие 463 пациента в возрасте от 6 до 17 лет, среди которых были пациенты и из России.
В России отмечаются высокие темпы роста заболеваемости и распространённости сахарного диабета. По данным федерального регистра сахарного диабета, в РФ на 01.01.2019 г. на диспансерном учете состояло 4,58 млн человек с этим заболеванием. Среди них более 38 000 составляют пациенты с сахарным диабетом в возрасте до 18 лет.2
Особенностью сахарного диабета 1 типа у детей и подростков является большая вариабельность глюкозы в крови, чем у взрослых. Детский организм более чувствителен к инсулину, потребность в котором может быстро меняться. Важно постоянно поддерживать динамическое равновесие между гипогликемией и гипергликемией. Именно поэтому по мнению специалистов для данной возрастной группы особенно необходима современная инсулинотерапия, обеспечивающая имитацию физиологической секреции инсулина.
«В течение последних лет мы достигли значительного прогресса в лечении сахарного диабета у детей и подростков: появляются новые технологии управления заболеванием, совершенствуются подходы к самоконтролю, все шире применяются системы мониторирования показателей здоровья. Однако основой терапии сахарного диабета остается инсулинотерапия. Одной из целей лечения юных пациентов с сахарным диабетом является достижение максимально близкого к норме уровня углеводного обмена.
Достичь его непросто из-за необходимости соблюдения хрупкого баланса между оптимальным уровнем гликемии и риском гипогликемии. Появление нового поколения базальных аналогов инсулина, в том числе инсулина Туджео СолоСтар®, позволяет расширить наши возможности управления сахарным диабетом у детей и подростков», – отметила Петеркова В.А., академик РАН, профессор, д.м.н., научный руководитель Института Детской эндокринологии, заведующая кафедрой детской эндокринологии-диабетологии ФГБУ «НМИЦ эндокринологии» Минздрава России, Главный внештатный детский специалист эндокринолог Минздрава России.
Туджео СолоСтар® был одобрен к применению у пациентов 6 лет и старше в России в декабре 2019 года3 на основании данных открытого рандомизированного, контролируемого клинического исследования по сравнению инсулинов гларгин 300 ЕД/мл и гларгин 100 ЕД/мл у детей и подростков с сахарным диабетом 1 типа EDITION JUNIOR.4 Исследование проходило в течение 26 недель, и в нем приняли участие 463 пациента, в том числе пациенты из России. В группу пациентов, получавших инсулин гларгин 300 ЕД/мл, входили 73 пациента в возрасте
- В группе препарата инсулина гларгин 300 ЕД/мл с режимом дозирования один раз в сутки к 26-й неделе было продемонстрировано сходное снижение уровня гликированного гемоглобина и глюкозы плазмы натощак от исходного уровня по сравнению с инсулином гларгин 100 ЕД/мл.
- Частота возникновения гипогликемии (за сутки и в ночное время) у пациентов была сходна в группе инсулина гларгин 300 ЕД/мл и инсулина гларгин 100 ЕД/мл.
Процент пациентов, сообщивших о тяжелой гипогликемии, был численно ниже в группе терапии препаратом инсулин гларгин 300 ЕД/мл по сравнению с группой терапии инсулином гларгин 100 ЕД/мл (6% и 8,8% соответственно).
- Доля пациентов с эпизодами гипергликемии, сопровождавшейся кетозом, была численно ниже в группе препарата инсулин гларгин 300 ЕД/мл по сравнению с группой инсулина гларгин 100 ЕД/мл (6,4% и 11,8% соответственно).
- Для препарата инсулин гларгин 300 ЕД/мл не было выявлено каких-либо проблем безопасности в отношении нежелательных явлений и стандартных параметров безопасности. Выработка антител отмечалась в редких случаях и не оказывала клинически выраженного влияния.
Туджео СолоСтар® – базальный инсулин последнего поколения. Препарат был зарегистрирован в США и ЕС в 2015 году. На данный момент препарат зарегистрирован в 60 странах. В России Туджео СолоСтар® был зарегистрирован в мае 2016 года. В ноябре 2019 применение препарата для детей 6 лет и старше рекомендовал Комитет по лекарственным препаратам для медицинского применения (CHMP) Европейского агентства по лекарственным средствам (ЕМА). В декабре 2019 года Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило применение препарата Туджео СолоСтар® (инсулин гларгин 300 ЕД/мл) для лечения сахарного диабета первого и второго типа у детей с 6 лет.
«Инсулин Туджео СолоСтар® (инсулин гларгин 300 ЕД/мл) – представитель второго поколения базальных аналогов инсулина, который уже в течение нескольких лет применяется для лечения сахарного диабета у взрослых в России и многих других странах. Накоплено большое количество научных данных по применению препарата как в клинических исследованиях, так и в реальной практике. Изучение использования новых инсулинов в детской популяции особенно важно для оценки их безопасности и возможностей применения с учетом клинических особенностей течения сахарного диабета у детей и подростков. Результаты исследования EDITION Junior, первого сравнительного исследования инсулина гларгин 300 ЕД/мл с инсулином гларгин 100 ЕД/мл в детской популяции, позволяют расширить арсенал средств по лечению сахарного диабета у детей и возможности врача по индивидуальному подбору терапии», – отметила Елена Лунина, медицинский руководитель бизнес-подразделения «Общая Медицина» Санофи в Евразии.
Все стадии производства (за исключением производства фармацевтической субстанции) препарата Туджео СолоСтар® осуществляются в Российской Федерации на заводе ЗАО «Санофи-Авентис Восток» в Орловской области. Фармацевтическая субстанция производится на заводе Санофи во Франкфурте, Германия.
Источники:
1 Сайт Государственного реестра лекарственных средств. [Электронный ресурс] 07 февраля 2020 г. URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=424c4ad4-27fe-44e0-ad39-6b840d1de94c&t=
2 Викулова О.К., Дедов И.И., Шестакова М.В., Железнякова А.В., Исаков М.А. Атлас регистра сахарного диабета РФ. Том 22, спецвыпуск 2. 2019. https://dia-endojournals.ru/dia/article/view/12208/9338
3 Инструкция по медицинскому применению препарата Туджео СолоСтар®. РУ ЛП-003 653 от 30.05.2016
4 Danne T et al.., Diabetes Care 2020;43:1512–1519 | https://doi.org/10.2337/dc19-1926.
Сахарный диабет – заболевание, приводящее к пожизненным инъекциям инсулина, инвалидности и фатальным осложнениям. Ученые из Приволжского исследовательского медицинского университета (ПИМУ) приступили к разработке принципиально нового метода лечения этого недуга.
Чтобы понять механизм технологии, нужно сказать о том, как работает поджелудочная железа, отчего возникает диабет. В этом органе есть так называемые бета-клетки, объединенные в островки, которые автоматически продуцируют инсулин в ответ на повышение уровня глюкозы в крови. При ряде аутоиммунных или хронических болезней общая их масса снижается, появляются функциональные нарушения в виде недостаточной выработки инсулина. Результат – повышение уровня глюкозы в сыворотке крови.
– Это инсулинопотребный сахарный диабет. Он возникает, если число островков уменьшилось на 80 процентов, – рассказывает заведующий кафедрой факультетской хирургии и трансплантологии, главный внештатный трансплантолог минздрава Нижегородской области Владимир Загайнов.
Ученый подчеркивает, что метод лечения диабета только один – трансплантация поджелудочной железы. Потребность в этой операции в России удовлетворяется на тысячные доли процента, что связано с дефицитом донорских органов. Во всех остальных случаях речь идет о компенсации заболевания с помощью инсулина. Однако даже пересадка сопряжена с необходимостью иммуносупрессивной терапии, чтобы организм пациента не отторгал донорский орган. А у нее есть свои минусы, особенно в отдаленном периоде.
Главная идея проекта – пересадка не всей поджелудочной железы, а только островков, состоящих из тех самых бета-клеток.
– Островки будут выделяться из донорской железы специальным способом. Даже если целая железа не годится для трансплантации, из нее можно попытаться выделить островки и пересадить их, – поясняет Владимир Загайнов.
В мире эту идею пытаются реализовать разными способами и с разной степенью успешности. Введение островков от донора требует все той же небезопасной иммуносупрессивной терапии. В ПИМУ ученые разрабатывают вариант пересадки клеток, заключенных в специальные пористые капсулы. В теории клетки приживаются и начинают вырабатывать инсулин. Человек излечивается от диабета. А поры капсулы достаточно малы, чтобы предотвратить атаку иммунных клеток организма, поэтому никакой иммуносупрессивной терапии не требуется. Важно, что речь идет о малоинвазивных операциях, а не о сложной трансплантации. Возможных вариантов несколько: введение в брюшную полость путем пункции либо введение в печень по воротной вене.
Первые эксперименты ученых из НИИ экспериментальной онкологии и биомедицинских технологий ПИМУ вместе с Институтом металлоорганической химии РАН оказались успешными.
– В отдаленной перспективе планируем проработать выращивание бета-клеток из стволовых, – говорит Владимир Загайнов. – Параллельно вместе с коллегами из Национального медицинского исследовательского центра трансплантологии и искусственных органов имени Шумакова занимаемся легитимизацией технологии. Раньше в России за это никто не брался, поэтому трансплантация островков бета-клеток поджелудочной пока не вошла в список разрешенных, хотя в мире это уже существует. Надеемся, что в ближайшее время вопрос будет решен.
Планируем проработать выращивание бета-клеток из стволовых
В 2022 году проект, выполняемый по госзаданию Минздрава России, завершится. Можно будет испытывать метод на животных, а затем заниматься регистрацией. На мой вопрос, когда лечение будет доступно российским пациентам, профессор Загайнов ответил кратко:
– Деклараций в жизни хватает, давайте заниматься делом.
Комментарий
Ольга Занозина, доктор медицинских наук, заведующая отделением эндокринологии Нижегородской областной больницы имени Семашко:
– Наряду с совершенствованием самих инсулинов, способов их введения в организм пациента, улучшением терапевтического обучения больных сахарным диабетом развивается и другое направление – трансплантационные технологии, позволяющие вводить бета-клетки островков поджелудочной железы, которые вырабатывают инсулин, в организм больного человека.
Положительный эффект достигается при виртуозном заборе, хранении и введении островковых клеток больному человеку. При успешном результате – почти полный контроль за гликемией, отсутствие гипогликемий и потребности в экзогенном инсулине. Вся эта работа требует ювелирного мастерства.
Сахарный диабет первого типа, который обычно развивается у детей и подростков, является хроническим заболеванием. Последние два года в Израиле и других странах ведутся интенсивные исследования этого заболевания, результаты которых заставляют ученых полностью пересмотреть традиционный подход к лечению сахарного диабета.
Считается, что сахарный диабет первого типа является аутоиммунным заболеванием, при котором происходит разрушение бета-клеток поджелудочной железы, ответственных за выработку инсулина — гормона, с помощью которого сахар (глюкоза) проникает в клетки организма. При разрушении бета-клеток количество выделяемого инсулина уменьшается и уровень сахара в крови повышается, что приводит к поражению кровеносных сосудов и другим пагубным последствиям для организма.
Несмотря на долгие годы исследований, ученые пока что не могут объяснить, почему организм разрушает собственные бета-клетки. Одна из теорий гласит, что причиной является вирусное заражение, при котором на молекулярном уровне вирусы похожи на бета-клетки, таким образом защитная реакция организма может быть ошибочно направлена на данный вид клеток. Согласно другой теории, причиной аутоиммунной атаки организма является излишняя стерильность, в которой растут дети, что приводит к повышенной чувствительности иммунной системы к собственным бета-клеткам поджелудочной железы.

Классическая модель развития сахарного диабета первого типа
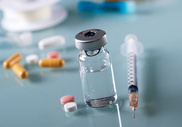
Принятая на сегодня теория развития сахарного диабета первого типа гласит, что первая стадия заболевания продолжается от нескольких месяцев до нескольких лет, в течение которых происходит постепенное разрушение бета-клеток поджелудочной железы. Заболевание не диагностируется на начальной стадии, потому что оставшиеся клетки начинают выделять больше инсулина, чтобы скомпенсировать его недостаток в крови. Сахарный диабет первого типа диагностируется, когда остается только 10 % бета-клеток, уже не способных выделять достаточно инсулина для поддержания требуемого уровня сахара в крови. На этом этапе пациент получает лечение — иньекции инсулина, параллельно с этим происходит полное уничтожение организмом оставшихся бета-клеток. Так как разрушение бета-клеток является необратимым процессом, пациент вынужден получать лечение на протяжении всей жизни.
Данная модель на протяжении многих лет оказывала огромное влияние на исследование сахарного диабета первого типа. Основным предположением было то, что на момент диагностики у пациента практически не остается бета-клеток поджелудочной железы. Старая модель основывалась на исследованиях, проведенных на одном виде мышей, развивающих болезнь, похожую на сахарный диабет первого типа у людей, а также на наблюдениях онкологических пациентов, у которых была удалена часть поджелудочной железы.
Новые исследования
В последние два года, благодаря значительным логическим усилиям, ученые получили возможность изучать десятки образцов тканей поджелудочной железы пациентов, страдающих сахарным диабетом первого типа, которые умерли незадолго после диагностики заболевания. Речь идет о редких и трагических случаях, когда пациенты (в основном дети) погибали при несчастных случаях, а семьи соглашались пожертвовать их органы для исследований.
Анализ образцов ткани этих пациентов показал неожиданные результаты. Оказалось, что в тканях поджелудочной железы имеется большое количество бета-клеток без видимых признаков поражения со стороны иммунной системы, а их количество значительно выше, чем 10 % здоровых клеток (согласно классической модели). Таким образом, ученые пришли к выводу, что на этапе диагностики сахарного диабета у человека имеется большое количество незатронутых иммунной системой бета-клеток.
Данное открытие проливает свет на известный в медицине эффект при начале лечения сахарного диабета первого типа с помощью инсулина, при котором в течение первых месяцев происходит временное «выздоровление», когда бета-клетки начинают вырабатывать инсулин в достаточном количестве. Классическая модель не может объяснить, каким образом такое небольшое количество бета-клеток выделяет достаточно инсулина. Новое исследование утверждает, что происходит функциональное поражение клеток, и при «разгрузке» с помощью инъекций инсулина их функции временно восстанавливаются, что было бы невозможно, если бы клетки были разрушены.
Важно отметить, что в организме происходит аутоиммунная реакция, направленная на разрушение бета-клеток поджелудочной железы. Однако, согласно новым исследованиям, происходит не уничтожение бета-клеток, а нарушение их функционирования, поэтому можно надеяться, что поражение такого рода может быть обратимым.
Какие последствия будет иметь данное открытие?
Теперь, когда известно, что на момент диагностики сахарного диабета первого типа имеется достаточно бета-клеток, пациент должен получать лекарства, нейтрализующие иммунную систему с целью предотвращения нарушения функционирования этих клеток. Разработка таких лекарств уже ведется. Другим направлением будут лекарства, которые смогут вернуть способность вырабатывать инсулин пораженным клеткам или обеспечить достаточную выработку инсулина оставшимися клетками. Ученые пока что далеки от создания подобных препаратов, но главное, что результаты последних исследований показали верный путь для лечения этого заболевания.
12931 просмотр
Представлены результаты международного клинического исследования EDITIONJUNIOR на Российской научно-практической конференции детских эндокринологов, которая прошла с 12 по 13 сентября в Санкт-Петербурге. Целью исследования была оценка применения базального инсулина последнего поколения инсулин гларгин 300 ЕД/мл у детей с 6 лет и старше, которые имеют сахарный диабет и требуют лечения инсулином.1 В исследовании приняли участие 463 пациента в возрасте от 6 до 17 лет, среди которых были пациенты и из России.
В нашей стране отмечаются высокие темпы роста заболеваемости и распространенности сахарного диабета. По данным федерального регистра сахарного диабета, в РФ на 01.01.2019 г. на диспансерном учете состояло 4,58 млн человек с этим заболеванием. Среди них более 38 000 составляют пациенты с сахарным диабетом в возрасте до 18 лет.2
Особенностью сахарного диабета 1 типа у детей и подростков является большая вариабельность глюкозы в крови, чем у взрослых. Детский организм более чувствителен к инсулину, потребность в котором может быстро меняться. Важно постоянно поддерживать динамическое равновесие между гипогликемией и гипергликемией. Именно поэтому по мнению специалистов для данной возрастной группы особенно необходима современная инсулинотерапия, обеспечивающая имитацию физиологической секреции инсулина.
«В течение последних лет мы достигли значительного прогресса в лечении сахарного диабета у детей и подростков: появляются новые технологии управления заболеванием, совершенствуются подходы к самоконтролю, все шире применяются системы мониторирования показателей здоровья. Однако основой терапии сахарного диабета остается инсулинотерапия. Одной из целей лечения юных пациентов с сахарным диабетом является достижение максимально близкого к норме уровня углеводного обмена. Достичь его непросто из-за необходимости соблюдения хрупкого баланса между оптимальным уровнем гликемии и риском гипогликемии. Появление нового поколения базальных аналогов инсулина, в том числе инсулина гларгин 300 ЕД/мл, позволяет расширить наши возможности управления сахарным диабетом у детей и подростков», – отметила Петеркова В.А., академик РАН, профессор, д.м.н., научный руководитель Института Детской эндокринологии, заведующая кафедрой детской эндокринологии-диабетологии ФГБУ «НМИЦ эндокринологии» Минздрава России, Главный внештатный детский специалист эндокринолог Минздрава России.
Препарат был одобрен к применению у пациентов 6 лет и старше в России в декабре 2019 г.3 на основании данных открытого рандомизированного, контролируемого клинического исследования по сравнению инсулинов гларгин 300 ЕД/мл и гларгин 100 ЕД/мл у детей и подростков с сахарным диабетом 1 типа EDITION JUNIOR.4
- Сайт Государственного реестра лекарственных средств. [Электронный ресурс] 07 февраля 2020 г. URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=424c4ad4-27fe-44e0-ad39-6b840d1de94c&t=
- Викулова О.К., Дедов И.И., Шестакова М.В., Железнякова А.В., Исаков М.А. Атлас регистра сахарного диабета РФ. Том 22, спецвыпуск 2. 2019. https://dia-endojournals.ru/dia/article/view/12208/9338
- Инструкция по медицинскому применению препарата Туджео СолоСтар®. РУ ЛП-003 653 от 30.05.2016
- Danne T et al.., Diabetes Care 2020;43:1512–1519 | https://doi.org/10.2337/dc19-1926.
